已知Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述正确的是( )

| A.a-b时沉淀的物质的量:Al(OH)3比BaSO4多 |
| B.c-d时溶液中离子的物质的量:AlO2-比Ba2+多 |
| C.a-d时沉淀的物质的量:BaSO4可能小于Al(OH)3 |
| D.d-e时溶液中离子的物质的量:Ba2+可能等于OH- |
使5.6LCO2气体迅速通过Na2O2固体后得到4.48L气体(标准状况下),这4.48L气体的质量为( )
| A.8.2g | B.8.8g | C.6.4g | D.6.2g |
在15g铁和氧化铁的混合物中,加入稀硫酸150mL,能放出H21.68L(标准状况)。同时铁和氧化铁均无剩余。向溶液中滴入KSCN溶液,未见颜色变化,为了中和过量的硫酸,而且使Fe2+完全转化成Fe(OH)2,共消耗3mol/L的NaOH溶液200mL,原硫酸溶液的物质的量浓度是( )
| A.1.5mol/L | B.2.5mol/L | C.2mol/L | D.3mol/L |
向100mL0.25mol/L的AlCl3溶液中加入金属钠完全反应,恰好生成只含NaCl和NaAlO2的澄清溶液,则加入金属钠的质量是( )
| A.3.45g | B.2.3g | C.1.15g | D.0.575g |
下表中对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是()
| |
陈述I |
陈述II |
判断 |
| A |
Fe3+具有氧化性 |
用KSCN溶液可以鉴别Fe3+ |
I对,II对,有 |
| B |
溶解度:CaCO3<Ca(HCO3)2 |
溶解度Na2CO3<NaHCO3 |
I对,II对,无 |
| C |
金属钠具有强氧化性 |
高压钠灯发出透雾性强的黄光 |
I对,II对,有 |
| D |
SiO2可与HF反应 |
氢氟酸不能保存在玻璃瓶中 |
I对,II对,有 |
有一块铝铁合金,将其溶解于足量盐酸中,再加入过量NaOH溶液,在空气中静置至红褐色沉淀不再增加时,将沉淀滤出再灼烧至恒重,得到残留物的质量与原合金质量相同,则合金中铝的质量分数( )
| A.52.4% | B.30% | C.70% | D.47.6% |
下列反应的离子方程式书写正确的是( )
| A.稀盐酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B.水玻璃中通入过量二氧化碳气体:SiO32-+CO2+H2O=H2SiO3+CO32- |
| C.浓烧碱溶液中加入铝片:Al+OH-+H2O=AlO2-+H2↑ |
| D.NaHSO4与足量Ba(OH)2溶液混合:H+ + SO42-+ Ba2++ OH- =BaSO4↓+H2O |
在浓硝酸中放入铜片发生反应:
(1)待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是 (用离子方程式表示)
(2)若将12.8g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6L(标况)。则所消耗硝酸的物质的量是 mol
(3)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2,使其充分反应,若要使水恰好充满容器,理论上需要参加反应的O2的物质的量是 mol
为研究浓硫酸的性质,某同学进行如下实验:
(1)称取铁和碳固体混合物12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。取896mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。据此推知气体Y 中SO2的体积分数为 。
(2)分析上述实验中SO2体积分数的结果,该同学认为气体Y中还可能含有H2和CO2
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
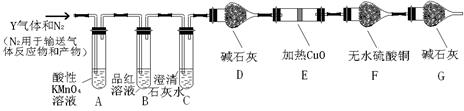
①写出产生CO2的化学方程式 。
②装置A中试剂的作用是 ,装置B的作用是 。
③简述确认气体Y中含有CO2的实验现象 。如果气体Y中含有H2,预计实验现象应是 。
下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
0.3molSO32-恰好将0.2molXO4-离子还原,则X元素在还原产物中的化合价是( )
| A.+1 | B.+2 | C.+3 | D.+4 |
向50mL18mol/L的浓H2SO4中加入足量铜片并加热,充分反应后,被还原的H2SO4的物质的量( )
| A.<0.45mol | B.=0.45mol | C.0.45mol—0.90mol之间 | D.>0.90mol |
两份铝屑,第一份与足量稀盐酸反应,第二份与足量氢氧化钠溶液反应,产生的氢气在相同条件下的体积比为1∶2,则第一份铝屑与第二份铝屑的质量比为( )
| A.1∶1 | B.1∶2 | C.1∶3 | D.2∶1 |
硝酸在有机合成、医药化工、化纤等行业应用非常广泛。工业上用氨催化氧化法可生产硝酸,其生产过程可表示为:
4NH3+5O2 4NO+6H2O ①
4NO+6H2O ①
4NO+3O2+2H2O→4HNO3 ②
完成下列计算:
(1)如果以一定量的氨气在一密闭容器中与足量氧气发生上述反应,冷却后所得溶液中溶质的质量分数是 (保留至1%)。
(2)某化肥厂以氨为原料通过题干中反应先产生硝酸,再利用氨气和硝酸反应制NH4NO3,已知由氨制 NO 的产率是 96%,NO 制硝酸的产率是 92%,氨被硝酸的吸收率为100%,则制备80吨 NH4NO3所需氨的体积(标准状况)为 m3(保留整数部分)。
工业上用铝土矿(主要成分SiO2、Al2O3、Fe3O4)提取氧化铝作冶炼铝的原料,提取的操作过程如下图所示:
(1)不溶物为___________(写化学式,下同),滤液甲中的溶质为______________________;
(2)滤液甲中含铝元素的溶质与过量NaOH溶液反应进入滤液乙,发生此反应的反应物的物质的量之比为_____________。若使用氨水能否达到上述目的__________(填“能”或“否”)。
(3)若向滤液甲中加入碘化钾溶液,相关的离子反应方程式为______________________,从该溶液中获得碘单质需要加入____________(填试剂名称),振荡、静置,再经______________(填操作名称),蒸馏后即得到碘单质。
(4)③步骤中通入二氧化碳是过量的,写出此步发生的离子反应方程式:_____________________;
(5)若将铝土矿用过量氢氧化钠溶液溶解,过滤后向滤液中通入过量CO2,再经过滤、加热得到的物质是______________________。
(6)②步骤得到的沉淀为灰绿色,沉淀变为红褐色需要较长时间,欲快速得到红褐色沉淀,可以向此沉淀中加入过量的_________(填字母)
| A.过氧化钠 | B.氯水 | C.稀硝酸 | D.酸性高锰酸钾溶液 |