将一定质量的镁铝合金投入100 mL 一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L 的NaOH 溶液,生成的沉淀跟加入的NaOH 溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)
求:
(1)加入NaOH 溶液0--20mL 过程中反应的化学方程式为_______________________。
160--180mL 过程中反应的离子方程式为__________________________。
(2)合金中Mg 的质量为____________g,所用HCl 的物质的量浓度为____________mol/L。
A、B、C、D、E 五种物质存在以下转化关系,已知A 为金属单质,在以下各步反应中E 是白色沉淀。
(1)试确定各物质的化学式:
A ________________B __________C__________ D________________ E____________
(2)写出以下反应的离子方程式:
A →C _________________________________
B →E _________________________________
用如下图所示装置证明浓硫酸的强氧化性,并检验产物的性质。请回答:
(1)装置①中反应的化学方程式_______________________。
(2)装置②中的现象是_______________________。
(3)装置③中的现象可证明SO2有______________性。
(4)装置④中反应的离子方程式_________________。
(5)装置⑤的作用是____________________。
某课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下3 组实验,如图Ⅰ~III 所示。
(1)Ⅰ所示的实验,若固体质量相同且稀盐酸足量时,气球鼓起较小的是___________(填化学式)。
(2)II、III 所示的实验均能鉴别这两种物质,相关反应的化学方程式是①_____________、②_________________。
③与II 相比, III 的优点是______________________(填选项序号)。
a.III 比II 复杂
b.III 比II 安全
c.III 可以做到用一套装置同时进行两个对比实验,而II 不行
(3)若用III 验证碳酸钠和碳酸氢钠的热稳定性,则试管B 中装入的固体应该是_______________。
实验室可用KMnO4固体和浓盐酸反应制氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)  2KCl+2MnCl2+5Cl2↑+8H2O。
2KCl+2MnCl2+5Cl2↑+8H2O。
(1)该反应中氧化剂是_____________,还原剂是__________________。
(2)若反应中有0.20 mol 电子发生转移,生成氯气的体积为____________(标准状况),被氧化的HCl的物质的量是___________________。
某科研小组探究工业废Cu粉(杂质可能含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用。他们进行了两组实验,过程如下:
过程Ⅰ:
过程Ⅱ:
(1)废Cu粉中一定含有的杂质是___________________(填化学式);
(2)写出过程①③中可能发生的所有反应的离子方程式:
①_______________________________________;
③_______________________________________;
(3)综合过程Ⅰ、II,计算该9.4g废Cu粉中,m(SiO2)=_________,m(Cu)= _________;
有人设计了如图所示的实验装置来探究钠与水反应(铁架台等仪器已略)。实验前在橡胶塞下端打一个小孔穴,将一大小适中的钠块固定于针头下端,向上抽动针头使钠块藏于孔穴内.在玻璃反应管内装入适量水(使钠块不与水接触).实验时,拔去橡胶乳头,按住橡胶塞,将针头缓缓向上拔起使钠与水接触,反应管内的液体被产生的气体压出,流入置于下方的烧杯中,气体则被收集在反应管内。
(1)钠与水反应的离子方程式为______________________;
(2)实验中“钠块熔化为闪亮的小球”说明____________________;向烧杯中的溶液中滴加________________,溶液变红,说明钠与水反应生成碱性物质;
(3)如果实验前加入反应管内水的体积为amL,欲使水最终全部被排出,则所取金属钠的质量至少为_______ g(设当时实验条件下气体摩尔体积为VmL/mol)。
类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中,错误的是
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色
④密度为1.1g•cm-3与密度为1.2g•cm-3的NaCl溶液等体积混合,所得NaCl溶液的密度介于1.1g•cm-3与1.2g•cm-3之间;NaK合金的熔点应介于Na和K熔点之间
| A.①② | B.①③④ | C.①②③④ | D.①②④ |
用NA表示阿伏加罗常数,下列叙述正确的是
| A.标准状况下,22.4LCCl4含有的分子数为NA |
| B.2.3gNa与足量的氧气发生反应,转移的电子数为0.2NA |
| C.通常情况下,32gO2与32gO3所含有的氧原子数均为2NA |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-数目为NA |
[化学——有机化学基础]
没食子酸丙酯简称PG,结构简式为 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
(1)PG的分子式为_________,请写出PG分子中所含官能团的名称______________,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是___________;
PG可发生如下转化:

(2)A的结构简式为_______________,1mol没食子酸最多可与_______mol H2加成;
(3)上图的有关变化中,属于氧化反应的有(填序号)____________;
(4)从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号)____________;
a.含有苯环 b.含有羧基 c.含有酚羟基 d.微溶于食用油
(5)反应④的化学方程式为_______________;
(6)B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式_______________;
i.含有苯环,且苯环上的一溴代物只有一种;
ii.既能发生银镜反应,又能发生水解反应。
[化学——物质结构与性质
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。回答下列问题:
(1)基态砷原子的电子排布式为 ;
(2)K3[Fe(CN)6]晶体中Fe3+与CN之间化学键类型为_________键,与CN互为等电子体的化合物分子式为 ;
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有0
NOx、O3、CH2=CHCHO、HCOOH、CH3—C—0—0—N02 (PAN)等二次污染物。
①N2O结构式可表示为N=N=O,N2O中中心氮原子的杂化轨道类型为 ;
1 mol PAN含σ键数目为 ;
②测定大气中PM2.5的浓度方法之一是 -射线吸收法,
-射线吸收法, -射线放射源可用85Kr。K晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则
-射线放射源可用85Kr。K晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则 = (填数字)。已知Kr晶体的密度为pg/cm3,摩尔质量为Mg/mol,阿伏伽德罗常数用Na表示,列式表示Kr晶胞参数a= nm。
= (填数字)。已知Kr晶体的密度为pg/cm3,摩尔质量为Mg/mol,阿伏伽德罗常数用Na表示,列式表示Kr晶胞参数a= nm。
[化学—化学与技术]
海洋是一个丰富的资宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河人海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和 池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用: (写一点即可)。
(2)电渗析法是近年发展起的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:
①海水不能直接通人到阴极室中,理由是 。
②A口排出的是 (填“淡水”或“浓水”).

(3)用苦卤(含Na+、K+、Mg2+CL-、Br-等离子)可提取溴,其生产流程如下:

①若吸收塔中的溶液含BrOf,则吸收塔中反应的离子方程式为: .
②通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化重新获得含Br2的溶液? 。
③向蒸馏塔中通人水蒸气加热,控制温度在90°C左右进行蒸馏的原因是 。
钼(Mo)是一种过渡金属元素,通常用作合金及不镑钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备 金属钼的主要流程图,已知钼酸难溶于水。
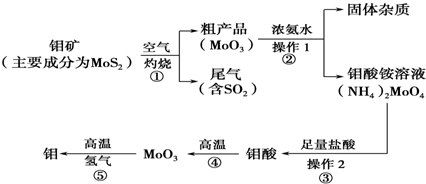
(1)写出反应①的化学方程式: 。
(2)写出反应②的化学方程式: 。
(3)反应①的尾气可以用碳酸钠溶液吸收。已知:根据表中提供的数据可知,在溶液中不能大量共存的微粒是______________;
| A.HCO3-、HSO3- | B.HCO3-、SO32- | C.HCO3-、H2S03 | D.HSO3- CO32- |
向过量碳酸钠溶液中通人少量二氧化硫,写出反应的离子方程式: 。
(4)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有 。
(5)工业上制备还原性气体CO和H2的反应原理为C02+CH4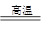 2CO + 2H2,CH4 + H2
2CO + 2H2,CH4 + H2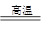 CO + 3H2,含甲烷体积分数为80%的10L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原Mo03制钼,理论上能生产钼的质量为g(小数点后保留1位,钼的相对原子质量为96)。
CO + 3H2,含甲烷体积分数为80%的10L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原Mo03制钼,理论上能生产钼的质量为g(小数点后保留1位,钼的相对原子质量为96)。
雾霾天气肆虐给人类健康带来了严重影响。燃煤和汽车尾气 是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为: 2NO(g)+2CO(g)= 2C02 (g)+N2 (g) △H<0 。
①该反应的速率时间图像如右图中左图所示。若其他条件不变,仅在反应前加人合适的催化剂,则其速率时间图像如右图中右图所示。

以下说法正确的是 (填对应字母)。
| A.a1>a2 | B.b1<b2 |
| C.t1>t2 | D.右图中阴影部分面积更大 |
E.左图中阴影部分面积更大
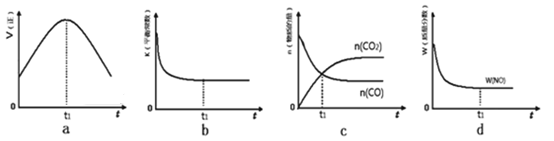
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) △H="-867" kJ/mol
2NO2(g)= N2O4(g) △H="-56.9" kJ/mol
H2O(g) = H2O(l) △H ="-44.0" kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(1)的热化学方程式: 。
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O CO+3H2 ,该反应在不同温度下的化学平衡常数如下表:
CO+3H2 ,该反应在不同温度下的化学平衡常数如下表:
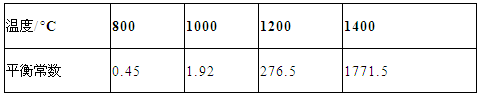
①该反应是 反应(填“吸热”或“放热”)。
②T℃时,向1L密闭容器中投入1mol CH4 和1mol H2Og),平衡时C(CH4)=0.5 mol·L- ,该温度下反应CH4 + H2O= CO+3H2的平衡常数K= 。
(4)甲烷燃料电池可以提升能量利用率。如图是利用甲烷燃料电池电解l00mLlmol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变)。

①甲烷燃料电池的负极反应式: 。
②电解后溶液的pH= ,(忽略氯气与氢氧化钠溶液反应)。
③阳极产生气体的体积在标准状况下是 L。