下列两种物质发生反应
①Na和O2 ②AlCl3与氨水 ③水玻璃与CO2 ④Fe与Cl2 ⑤Fe和稀HNO3,因反应物用量或反应条件的不同而生成不同产物的是()
| A.①②③④⑤ | B.①②③⑤ | C.①②⑤ | D.①③⑤ |
在体积相同的两个密闭容器中分别充满O2、O3气体,当两个容器内温度和气体密度相等时,说法正确的是 ( )
| A.两种气体的压强相等 | B.O2比O3质量小 |
| C.两种气体的分子数目相等 | D.两种气体的氧原子数目相等 |
某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液。下列说法正确的是( )

| A.a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O |
| B.外电路电子的流向是从a到b |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.b电极上发生还原反应 |
锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时的电极反应式为
负极反应:C6Li-xe-=C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成的复合材料)
正极反应:Li1-xMO2+xLi++x e-=LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是( )
| A.锂离子电池放电时电池反应为LiMO2+C6Li1-x=C6Li+Li1-xMO2 |
| B.锂离子电池充电时电池内部Li+向负极所连的电极移动 |
| C.锂离子电池放电时电池内部电流从负极流向正极 |
| D.锂离子电池充电时阳极反应为C6Li1-x+xLi++xe-=C6Li |
硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如下,该电池工作时反应为: 4VB2 + 11O2→4B2O3 + 2V2O5。下列说法正确的是( )

| A.电极a为电池负极 |
| B.VB2中V的化合价为+4价 |
| C.电子由VB2极经KOH溶液流向a电极 |
| D.VB2极发生的电极反应为:2VB2 + 22OH−-22e−=V2O5 + 2B2O3 + 11H2O |
以石墨电极电解200 mL CuSO4溶液,电解过程中转移电子的物质的量n(e—)与产生气体体积V(g)(标准状况)的关系如下图所示。下列说法中正确的是( )
| A.电解前CuSO4溶液的物质的量浓度为2mol/L |
| B.电解后所得溶液中c(H+)=2mol/L |
| C.当n(e—)=0.6mol时,V(H2)∶V(O2)=3∶2 |
| D.向电解后的溶液中先后加入16gCuO和3.6g水,则溶液可恢复为电解前的浓度 |
镁-空气电池的工作原理如右图所示。下列说法不正确的是( )

| A.工作一段时间后,c(Na+)变大 | B.电池工作时,OH-向a极移动 |
| C.气体X 中N2的百分含量与空气相同 | D.电池总反应为2Mg+O2+2H2O=2Mg(OH)2 |
原子总数相同、电子总数或价电子总数相同的互为等电子体,等电子体具有结构相似的特征,下列各对粒子中,空间结构相似的是( )
①CS2与NO2 ②CO2与N2O ③SO2与O3 ④PCl3与BF3
| A.①②③ | B.③④ | C.②③④ | D.②③ |
被称为“软电池“的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内为离子“流过”水和氯化锌组成的电解液。电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列有关说法中正确的是( )
| A.该电池的正极为锌 |
| B.该电池反应中二氧化锰起催化作用 |
| C.当0.1molZn完全反应时,流经电解液的电子个数为1.204×1023 |
| D.电池的正极反应式为2MnO2+2H2O+2eˉ=2MnO(OH)+2OHˉ |
某化学兴趣小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H2C2O4 + 3H2SO4 ="=" K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
| 实验编号 |
室温下,试管中所加试剂及其用量 / mL |
室温下溶液颜色褪至无色所需时间 / min |
|||
| 0.6 mol/L H2C2O4溶液 |
H2O |
0.2 mol/L KMnO4溶液 |
3 mol/L 稀硫酸 |
||
| 1 |
3.0 |
2.0 |
3.0 |
2.0 |
4.0 |
| 2 |
3.0 |
3.0 |
2.0 |
2.0 |
5.2 |
| 3 |
3.0 |
4.0 |
1.0 |
2.0 |
6.4 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1数据计算,用KMnO4的浓度变化表示反应速率 v(KMnO4)= 。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图甲所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图乙所示。 该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究。
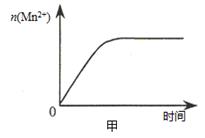
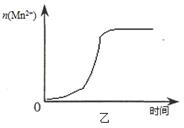
①该小组同学提出的假设是 。
②请你帮助该小组同学完成实验方案,并选择表中空白处应加入的物质。
| 实验编号 |
室温下,试管中所加试剂及其用量 / mL |
再向试管中加入少量固体 |
室温下溶液颜色褪至无色所需时间 / min |
|||
| 0.6 mol/L H2C2O4溶液 |
H2O |
0.2 mol/L KMnO4溶液 |
3 mol/L 稀硫酸 |
|||
| 4 |
3.0 |
2.0 |
3.0 |
2.0 |
|
 |
A.KMnO4 B.H2C2O4 C.K2SO4 D.MnSO4
③若该小组同学提出的假设成立,应观察到的现象是 。
BCl3是重要的化工原料,其沸点12℃。500℃时,向2L的密闭容器中按一定比例投入B2O3、C、Cl2,模拟工业制取三氯化硼的反应如下:B2O3(s) + 3C(s) + 3Cl2(g)  2BCl3 (g) + 3CO(g)。
2BCl3 (g) + 3CO(g)。
(1)反应起始至3min时固体质量减少了15.9克,则氯气的平均反应速率为_____________。
(2)反应至4min时达到平衡,则下列说法正确的是____________(填序号)。
A.3min时,CO的消耗速率大于氯气的消耗速率
B.2min至4min时BCl3的生成速率比0至2min时的快
C.反应起始至平衡,气体的密度不断增大
D.达到平衡后,容器内的压强不再变化
(3)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。
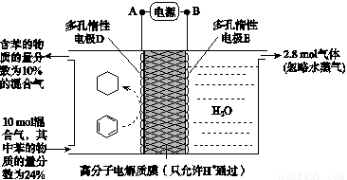
①A、D之间导线中电子移动方向为_______________。(用A、D表示)
②生成目标产物的电极反应式为__________________。
③该储氢装置的电流效率η=____________________。
(η= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)氧元素能形成繁多的氧化物,请写出一个与CO2等电子的化合物_________________;
(2)把Na2O、SiO2、P2O5三种氧化物按熔沸点由高到低顺序排列_________________;
(3)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为_________________;
(4)Se原子基态核外电子的排布式为_________________;
(5)SO32-离子中硫原子的杂化方式__________,该离子的立体构型为____________;
(6)元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。X与Y所形成化合物晶体的晶胞如图所示。

①在一个晶胞中,X离子的数目______,该化合物的化学式为______________;
②Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是 ;
③Y与Z可形成YZ42-。YZ42-的空间构型为_________(用文字描述);写出一种与YZ42-互为等电子体的分子的化学式____________;
④X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ 键的数目为________;
天然海水中含有非常丰富的化学元素,具有很大的利用价值。工业上对海水资源综合利用的部分工艺流程如下图所示。
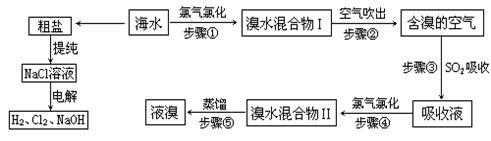
(1)请列举海水淡化的两种方法: 、 。
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入少量二氧化碳发生反应的离子方程式 。
(3)海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如上图。步骤①反应的离子方程式是 ;步骤③通入二氧化硫的目的是 ,其反应的化学方程式是 。
(4)步骤⑤蒸馏的过程中,温度应控制在80-90℃。温度过高或过低都不利于生产,请解释其原因: 。
某有机物A的红外光谱和核磁共振氢谱图如下图所示,下列说法中错误的是( )

| A.由红外光谱可知,该有机物中至少有三种不同的化学键 |
| B.若A的化学式为C2H6O,则其结构简式为CH3—O—CH3 |
| C.仅由其核磁共振氢谱图无法得知其分子中的氢原子总数 |
| D.由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子 |