下列叙述正确的是
| A.1.00 mol NaCl中含有 6.02×1023个 NaCl 分子 |
| B.1.00 mol NaCl中,所有Na+的最外层电子总数为 8×6.02×1023 |
| C.欲配制 1.00 L 1.00 mol·L-1的 NaCl 溶液,可将58.5 g NaCl 溶于1.00 L水中 |
| D.电解58.5 g 熔融的 NaCl,能产生22.4 L 氯气(标准状况)、23.0 g 金属钠 |
如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是
| A.所含原子数相等 |
| B.气体密度相等 |
| C.气体质量相等 |
| D.摩尔质量相等 |
根据表中信息判断,下列选项不正确的是
| 序号 |
反应物 |
产 物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4 |
| ② |
C12、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO4- |
C12、Mn2+ |
A.氧化性由强到弱顺序为MnO4-> C12>Fe3+>Br2
B.第①组反应的氧化产物为O2
C.第②组反应中参加反应的Cl2与FeBr2的物质的量之比为1:2
D.第③组反应中生成1mol Cl2,转移电子2mol
对下列各组中的实验步骤和现象,分析正确的一项是
| 选项 |
实验现象 |
原因分析 |
| A |
证明酸性条件下H2O2氧化性比I2强 |
碘化钠溶液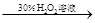 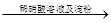 溶液变蓝色 溶液变蓝色 |
| B |
新制氯水中滴加石蕊试液,溶液先变红,后褪色 |
氯气与水反应生成HCl、HClO,HCl、HClO显酸性,使石蕊变红,Cl2具有强氧化性,使其褪色 |
| C |
SO2通人溴水中,溴水褪色 |
SO2具有漂白性,使其褪色 |
| D |
向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 |
在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
关于下列各装置的叙述正确的是
| A.装置①可用于实验室制备NO气体 |
| B.装置②可用于模拟海水蒸馏 |
| C.装置③可用于探究碳酸氢钠的热稳定性 |
| D.装置④为配制溶液过程中的定容操作 |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Fe3+、NO3-、SO42-、Na+ |
| B.使酚酞变红色的溶液中:Na+、Al3+、HCO3-、NO3- |
| C.能与金属铝反应生成氢气的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.无色透明的溶液中:K+、Cu2+、Cl-、NO3- |
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是
| A.元素形成的简单离子的半径Z<M |
| B.Y的最高价氧化物对应水化物的酸性比X的强 |
| C.X的最简单气态氢化物的热稳定性比Z的小 |
| D.Z位于元素周期表中第2周期、第ⅥA族 |
下列离子方程式书写正确的是
| A.Na与水反应Na+H2O=Na++OH-+H2↑ |
B.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O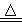 Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
| C.实验室盛装NaOH溶液的试剂瓶不能用玻璃塞SiO2+2OH-=SiO32-+H2O |
| D.向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O+CO32- |
若NA表示阿伏加德罗常数,下列说法正确的是
| A.标准状况下,6.72LNO2与水充分反应转移电子数为0.1NA |
| B.18gD2O中含有的质子数目为10NA |
| C.常温常压下,1mol氦气中含有的核外电子数为2NA |
| D.ag某气体含分子数为b,cg该气体在标况下的体积为22.4ab/(c NA)L |
下列叙述正确的是
| A.H2与T2互为同位素 |
| B.SO2、CO均属于酸性氧化物 |
| C.离子化合物中一定不含共价键 |
| D.氯化铵、氯化氢都属于强电解质 |
中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出)。单质A常作为食品包装材料,甲是两性氧化物。根据图示转化关系回答:

(1)写出反应①的离子方程式______________________。
(2)写出单质A与Fe2O3反应的化学方程式: ,除铝热剂外,该反应还需加入 ,利用该反应的原理,可用于___________。
(3)设计一个简单的实验方案,证明上述A与Fe2O3反应所得的块状熔融物中含有单质A .
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为 ,若有3mol FeS2参加反应,转移电子数为 .
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为 (用离子方程表示)
(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请写出相应的离子方程式
碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2, 该反应的离子方程式为 。
(2)氢氧化铁与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(3)从海带中提取碘的过程中,下列说法正确的是

某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中
| A.至少存在5种离子 |
| B.Clˉ一定存在,且c(Clˉ)≥0.4mol/L |
| C.SO42ˉ、NH4+一定存在,CO32-可能存在 |
| D.CO32ˉ、Al3+一定不存在,K+ 一定存在 |
下列有关实验装置的说法中正确的是
| A.图1装置可制取干燥纯净的NH3 |
| B.图2装置可以完成“喷泉”实验 |
| C.图3装置可测量Cu与浓硝酸反应产生气体的体积 |
| D.图4装置可用于实验室制备Fe(OH)2 |