下列离子方程式书写正确的是
| A.铁片放入稀盐酸中:2Fe + 6H+ = 2Fe3+ + 3H2↑ |
| B.大理石放入稀硝酸中 CO32- + 2H+ = CO2↑+ H2O |
| C.铁片插入硫酸铜溶液2Fe + Cu2+ =" Cu" + 2Fe2+ |
| D.硫酸铜与氢氧化钡溶液反应:Cu2+ + SO42- + Ba2+ + 2OH- = Cu(OH)2↓+ BaSO4↓ |
下列电离方程式错误的是
| A.KNO3 = K+ + NO3- |
| B.NaHSO4 = Na+ + H+ + SO42- |
| C.BaCl2 = Ba2+ + Cl2- |
| D.Na2SO4 = 2Na+ + SO42- |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.无色溶液中:Al3+、Cl—、MnO4—、SO42— |
| B.含有大量HCO3-的溶液中:Na+、Ca2+、NO3—、Cl— |
| C.0.1 mol·L-1AgNO3溶液:H+、K+、SO42—、Cl— |
| D.使石蕊变红色的溶液:CH3COO—、Cl—、NO3—、K+ |
标准状况下VL氨气溶解在1L水中(水的密度为1g/ml),所得溶液的密度为ρg/ml,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确的是
A. |
B.ω |
C.ω |
| D.c=1000Vρ/(17V+22400) |
科学家刚刚发现了某种元素的原子,其质量是ag,12C的原子质量是bg,NA是阿伏加德罗常数的值,下列说法不正确的是
| A.该原子的摩尔质量是aNAg/mol |
B.Wg该原子的物质的量一定是 mol mol |
C.Wg该原子中含有 个该原子 个该原子 |
D.由已知信息可得:NA= |
如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是
| A.所含原子数相等 |
| B.气体密度相等 |
| C.气体质量相等 |
| D.摩尔质量相等 |
下列叙述正确的是
①氧化还原反应的实质是元素的化合价发生改变
②若1 mol气体的体积为22.4 L,则它一定处于标准状况下
③标准状况下,1 L HCl和1 L H2O的物质的量相同
④在熔融状态下可以导电的物质就是电解质
⑤利用丁达尔现象区别溶液和胶体
⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑦在同温同体积时,气体物质的物质的量越大,则压强越大
⑧同温同压下,气体的密度与气体的相对分子质量成正比
| A.除③外 | B.④⑤⑥⑦⑧ | C.⑤⑦⑧ | D.①⑤⑦⑧ |
下列实验中,所选装置或实验设计合理的是
| A.图⑤所示装置中盛有饱和Na2CO3溶液除去CO2中含有的少量HCl |
| B.用乙醇提取溴水中的溴选择图③所示装置 |
| C.用图①和②所示装置进行粗盐提纯 |
| D.用图④所示装置分离酒精和水 |
下列实验操作和处理方法可能会引发安全事故的是
①将水沿着烧杯内壁缓慢加入浓硫酸中,并用玻璃棒不断搅拌
②给试管中的液体加热时,试管口不朝向任何人
③夜间厨房发生煤气泄漏时,立即开灯检查煤气泄漏原因,并打开所有门窗通风
④用氢气还原氧化铜时,先加热氧化铜,再通入氢气。
| A.④ | B.①③④ | C.①④ | D.①②③④ |
甲同学将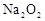 分别与H2O和浓盐酸反应,有如下现象:
分别与H2O和浓盐酸反应,有如下现象:
| 实验序号 |
使用药品 |
现象 |
| Ⅰ |
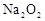 、 、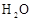 |
① 试管壁发热 ② 有无色无味气体产生 |
| Ⅱ |
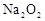 、浓盐酸 、浓盐酸 |
① 试管壁发热 ② 有刺激性气味的气体产生 ③ 反应后所得溶液呈浅黄绿色 |
请完成下列问题:
实验I中:
(1)该反应是_______________反应(填“放热”或“吸热”)。
(2)反应的化学方程式是__________________。
(3)证明无色无味气体是氧气的方法是 。
实验Ⅱ中:
(4)根据现象②、③,推测生成的气体中可能含有Cl2,产生Cl2的化学方程式是 。
(5)若往“浅黄绿色溶液”中加入FeCl3溶液,立即产生与实验Ⅰ相同的气体,原因是__________。
已知甲、乙、丙是中学常见的三种气体单质,相互间反应可制得化肥B。其转化关系如图所示:
(1)将B中所含元素填写在下表的恰当位置中(用元素符号表示)
(2)已知反应一是放热反应,画出能量关系示意图。
(3)为加快反应一的速率,可采取的措施有:适当升高温度、选用恰当的催化剂、增大某一反应物的浓度和______________。
(4)方法一的化学方程式是_________________。
(5)用方法二也能制得B:甲和丙反应的产物与A反应即可,这两种方法更好的是______(填“方
法一”或“方法二”),理由是______________。
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法表示更便于理解。下列表达正确的是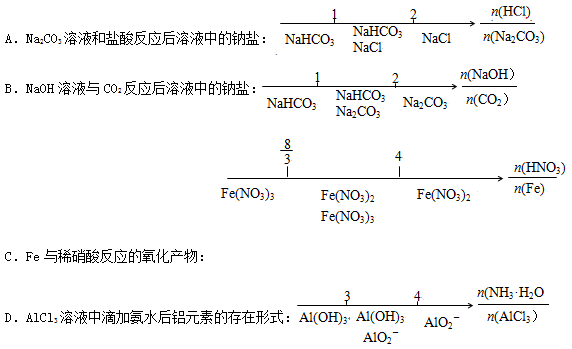
微电解法是利用原电池原理处理、净化高浓度有机废水的一种理想方法。在酸性、充入氧
气条件下的铁碳微电解法处理有机废水的过程中,有如下一些反应:
① O2+ 4H++4e-= 2H2O
② O2+ 2H2O+ 4e-= 4OH-
③ 4Fe2++O2+4H+= 2H2O+ 4Fe3+
......
下列有关这种铁碳微电解法处理有机废水说法不合理的是
| A.在处理废水的过程中,pH升高 |
| B.铁做负极,电极反应式是 Fe-2e-= Fe2+ |
| C.处理、净化过程中发生的反应都是氧化还原反应 |
| D.Fe(OH)3胶体,可净化除去废水中的悬浮物 |
CO和H2在ThNi5作用下可以合成CH4。
已知温度为T时:① CO(g)+H2O(g) === CO2(g)+H2(g) ΔH=-41 kJ·mol-1
② CH4(g)+2H2O(g) === 4H2(g) + CO2(g) ΔH=+165 kJ·mol-1
下列说法不正确的是
| A.催化剂不能改变该反应的ΔH |
| B.①中反应物的键能总和小于生成物的键能总和 |
| C.②中反应物的总能量高于生成物的总能量 |
| D.CO(g)与H2(g)合成CH4(g)的反应为放热反应 |
为了控制温室效应,工业上可用CO2来生产甲醇。一定条件下,在体积为1 L的恒容密闭容器中充入1 mol CO2和3 mol H2,发生如下反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH>0
CH3OH(g)+H2O(g) ΔH>0
下列说法正确的是
| A.升高温度,该反应的平衡常数增大 |
| B.当v(CO2):v (H2)=1:3时,反应达到平衡 |
| C.当 c(CH3OH) = 1mol·L-1时,反应达到平衡 |
| D.平衡后再充入一定量的CO2,甲醇的体积分数一定增大 |