某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
| 编号 |
实验目的 |
碳粉/g |
铁粉/g |
醋酸/% |
| ① |
为以下实验作参照 |
0.5 |
2.0 |
90.0 |
| ② |
醋酸浓度的影响 |
0.5 |
|
36.0 |
| ③ |
|
0.2 |
2.0 |
90.0 |
(2)编号①实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了 腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了 (填“氧化”或“还原”)反应,其电极反应式是 。
(3)经过相当长的一段时间,图1锥形瓶中混合物表面生成了一层红棕色的铁锈,取少量铁锈于试管中,加入稀盐酸,取少量反应之后的溶液检验其中的Fe3+,检验Fe3+最灵敏的试剂是大家熟知的KSCN,可以检验痕量的Fe3+。还可用KI来检验:2Fe3++2I- 2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
| 编号 |
实验操作 |
预期现象和结论 |
| ① |
在试管中加入少量该FeCl3溶液和 (填少量、过量)的KI溶液。 |
深红色如期出现 |
| ② |
将试管中的混合溶液转移至 (填仪器)中,倒入一定量的 , 塞住活塞,充分振荡(萃取),静置。 |
|
| ③ |
|
|
在城市中地下常埋有纵横交错的管道和输电线路,有些地面上还铺有地铁或城铁的铁轨,当有电流泄漏入潮湿的土壤中,并与金属管道或铁轨形成回路时,就会引起后者的腐蚀。原理简化如图所示。则下列有关说法不正确的是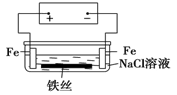
| A.原理图可理解为两个串联电解装置 |
| B.溶液中铁丝被腐蚀时,左侧有无色气体产生,附近产生少量白色沉淀,随后变为灰绿色 |
| C.溶液中铁丝左端电极反应式为:Fe-2e-=Fe2+ |
| D.地下管线被腐蚀,不易发现,维修也不便,故应将埋在地下的金属管道表面涂绝缘膜(或油漆等) |
在城市中地下常埋有纵横交错的管道和输电线路,有些地面上还铺有地铁或城铁的铁轨,当有电流泄漏入潮湿的土壤中,并与金属管道或铁轨形成回路时,就会引起后者的腐蚀。原理简化如图所示。则下列有关说法不正确的是
| A.原理图可理解为两个串联电解装置 |
| B.溶液中铁丝被腐蚀时,左侧有无色气体产生,附近产生少量白色沉淀,随后变为灰绿色 |
| C.溶液中铁丝左端电极反应式为:Fe-2e-=Fe2+ |
| D.地下管线被腐蚀,不易发现,维修也不便,故应将埋在地下的金属管道表面涂绝缘膜(或油漆等) |
用图示的方法可以保护钢质闸门。下列说法正确的是
| A.当a、b间用导体连接时,则X应发生氧化反应 |
| B.当a、b间用导体连接时,则X可以是锌或石墨 |
| C.当a、b与外接电源相连时,a应连接电源的正极 |
| D.当a、b与外接电源相连时,阴极的电极反应式:2Cl--2e→Cl2↑ |
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)原子序数为29的铜元素位于元素周期表中第周期。
(2)某青铜器中、
的质量分别为119
、20.7
,则该青铜器中
和
原子的数目之比为。
(3)研究发现,腐蚀严重的青铜器表面大都存在。关于
在青铜器腐蚀过程中的催化作用,下列叙述正确的是。
| A. | 降低了反应的活化能 | B. | 增大了反应的速率 |
| C. | 降低了反应的焓变 | D. | 增大了反应的平衡常数 |
(4)采用"局部封闭法"可以防止青铜器进一步被腐蚀。如将糊状涂在被腐蚀部位,
与有害组分
发生复分解反应,该化学方程式为。
(5)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是(填图中字母""或"
"或"
");
②环境中的扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
,其离子方程式为;
③若生成4.29 ,则理论上耗氧体积为
(标准状况)。
下列叙述中, 正确的是
①纯铁比碳素钢易生锈
②大量燃烧含硫燃料是形成酸雨的主要原因
③硅是光导纤维和制造太阳能电池的主要原料
④可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性Cl>C>Si
⑤氯水和过氧化钠都具有漂白作用,其漂白原理相似
⑥用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
⑦日本福岛核电站泄露的放射性核素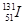 和
和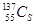 ,前者比后者少8个中子
,前者比后者少8个中子
⑧Al2O3在工业上用于制作耐高温材料,也用于电解法冶炼铝金属
| A.①⑤⑥⑦ | B.②③⑤⑦ | C.③④⑤⑥ | D.②⑤⑥⑧ |
有A、B、C、D四块金属片,进行如下实验,
①A、B用导线相连后,同时插入稀H2SO4中,A极为负极
②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D
③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡
④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,
则四种金属的活动性顺序为
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
下列对钢铁制品采取的措施不能防止或减缓钢铁腐蚀的是
| A.保持表面干燥 | B.表面镀锌 |
| C.表面镶嵌铜块 | D.与直流电源负极相连 |
如下图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是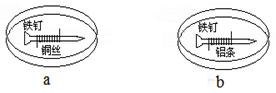
| A.a中铁钉附近呈现红色 |
| B.b中铁钉上发生还原反应 |
| C.a中铜丝上发生氧化反应 |
| D.b中铝条附近有气泡产生 |
下列有关电化学原理的说法中,错误的是
| A.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 |
| B.在铜的精炼装置中,通常用粗铜作作阳极,精铜作阴极 |
| C.氯碱工业,主要依托电解熔融的氯化钠来制取工业上重要的化工原料烧碱和氯气 |
| D.可充电的电池称“二次电池”,在充电时,是将电能转变成化学能,在放电时,又将化学能转化成电能 |
下列有关金属腐蚀与防护的说法不正确的是
| A.钢铁在弱碱性条件下发生电化学腐蚀的正极反应是:O2+2H2O+4e-===4OH- |
| B.当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
金属及其化合物在国民经济发展中起着重要作用。
(1)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:2Cu2O+ Cu2S=6Cu+SO2
该反应的氧化剂是_________,当生成19.2gCu时,反应中转移的电子为_____mol。铜在潮湿的空气中能发生吸氧腐蚀而生成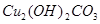 (碱式碳酸同)。该过程负极的电极反应式_______________。
(碱式碳酸同)。该过程负极的电极反应式_______________。
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(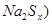 分别作为两个电极的反应物,固体
分别作为两个电极的反应物,固体 陶瓷(可传导
陶瓷(可传导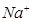 )为电解质,其原理如图所示:
)为电解质,其原理如图所示:
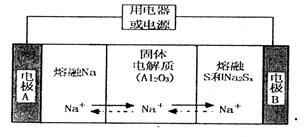
①根据下表数据,请你判断该电池工作的适宜温度应控制在_______。

②放电时,电极A为____极,S发生_______反应。
③放电时,内电路中的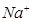 的移动方向为_______(填“从A到B”或“从B到A”)。
的移动方向为_______(填“从A到B”或“从B到A”)。
④充电时,总反应为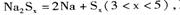 Na所在电极与直流电源_______极相连,阳极的电极反应式为________.
Na所在电极与直流电源_______极相连,阳极的电极反应式为________.
在生产生活中,金属腐蚀所带来的损失非常严重,所以防止金属腐蚀已经成为科学研究和技术领域的重大问题.兴趣小组的同学在实验室对金属腐蚀进行了探究.
(1)分别在三个洁净干燥的试管中各加一个洁净无锈的铁钉,再在其中两个试管中加入经煮沸迅速冷却的蒸馏水,其它操作请仔细观察图1:_________ 号试管中的铁钉最容易生锈.由此可见,铁制品生锈需要的条件是_________ .
(2)如图2所示,铁处于A、B、C三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号):_________ .
(3)据报道,全世界每年因为金属腐蚀造成的直接经济损失约达7000亿美元,我国因金属腐蚀造成的损失占国民生产总值(GNP)的4%.
①钢铁在发生电化学腐蚀时,负极反应为:_________ .
②请写出用稀硫酸除去铁锈的化学反应方程式为:_________ .
③请根据不同的原理,提出防止钢铁腐蚀的两条合理措施:_________ 、_________ .
用下列装置进行相应实验,能达到实验目的的是
| A.图1为牺牲阳极的阴极保护法,可以防止铁棒被腐蚀 |
| B.图2所示装置可以检验溴乙烷与NaOH醇溶液共热产生的乙烯 |
| C.图3所示装置可以用来制备氢氧化亚铁 |
| D.图4所示装置可以用来测定中和热 |
下图可设计成多种用途的电化学装置。下列分析正确的是
| A.当a和b用导线连接时,溶液中的SO42-向铜片附近移动 |
| B.将a与电源正极相连可以保护锌片,这叫牺牲阳极的阴极保护法 |
| C.当a和b用导线连接时,铜片上发生的反应为:2H++2e →H2↑ |
| D.a和b用导线连接后,电路中通过0.02mol电子时,产生0.02mol气体 |