上海市闸北区高三下学期期中练习(二模)化学试卷
化学与人们的日常生活密切相关,下列叙述正确的是
| A.二氧化硅是制造玻璃、光导纤维的原料 |
| B.纤维素、油脂是天然有机高分子化合物 |
| C.白菜上洒少许福尔马林,既保鲜又消毒 |
| D.NOx、CO2、PM2.5颗粒都会导致酸雨 |
下列化学用语正确的是
| A.聚丙烯的链节:—CH2—CH2—CH2— |
B.二氧化碳分子的比例模型: |
C. 的名称:1,3—二甲基丁烷 的名称:1,3—二甲基丁烷 |
D.氯离子的结构示意图: |
钐(Sm)属于稀土元素, Sm与
Sm与 Sm是钐元素的两种同位素。以下说法正确的是
Sm是钐元素的两种同位素。以下说法正确的是
A. Sm与 Sm与 Sm互为同素异形体 Sm互为同素异形体 |
B. Sm与 Sm与 Sm具有相同核外电子排布 Sm具有相同核外电子排布 |
C. Sm与 Sm与 Sm的性质完全相同 Sm的性质完全相同 |
D. Sm与 Sm与 Sm的质子数不同,但中子数相同 Sm的质子数不同,但中子数相同 |
单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点越高。下列溶液中沸点最高的是
| A.0.01 mol/L的蔗糖溶液 | B.0.02 mol/L的CH3COOH溶液 |
| C.0.02 mol/L的NaCl溶液 | D.0.01 mol/L的K2SO4溶液 |
下列有关能量的判断和表示方法正确的是
| A.由C(s,石墨)→C(s,金刚石)—1.9 kJ,可知:石墨比金刚石更稳定 |
| B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 |
| C.由H+(aq)+OH-(aq) →H2O(l)+ 57.3 kJ,可知:含1 mol CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量等于57.3 kJ |
| D.2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g) →2H2O(l)+285.8 kJ |
将少量SO2气体通入BaCl2和FeCl3的混合溶液中,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生。针对上述变化,下列分析正确的是
| A.该实验表明SO2有漂白性 | B.白色沉淀为BaSO3 |
| C.该实验表明FeCl3有还原性 | D.反应后溶液酸性增强 |
甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是
| A.丙与庚的原子序数相差3 |
| B.气态氢化物的热稳定性:戊>己>庚 |
| C.乙所在周期元素中,其简单离子的半径最大 |
| D.乙的单质在空气中燃烧生成的化合物只含离子键 |
用图示的方法可以保护钢质闸门。下列说法正确的是
| A.当a、b间用导体连接时,则X应发生氧化反应 |
| B.当a、b间用导体连接时,则X可以是锌或石墨 |
| C.当a、b与外接电源相连时,a应连接电源的正极 |
| D.当a、b与外接电源相连时,阴极的电极反应式:2Cl--2e→Cl2↑ |
某课外活动小组的同学从采集器中获得雾霾颗粒样品,然后用蒸馏水溶解,得到可溶性成分的浸取液。在探究该浸取液成分的实验中,下列根据实验现象得出的结论错误的是
| A.取浸取液少许,滴入AgNO3溶液有白色沉淀产生,则可能含有Cl- |
| B.取浸取液少许,加入Cu和浓H2SO4,试管口有红棕色气体产生,则可能含有NO3- |
| C.取浸取液少许,滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,则一定含SO42- |
| D.用洁净的铂丝棒蘸取浸取液,在酒精灯外焰上灼烧,焰色呈黄色,则一定含有Na+ |
常温下,0.2 mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示(a、b、d、e均为不超过1的正数),则下列说法正确的是
| A.该溶液pH=7 | B.该溶液中:c(A-)+c(Y)=c(Na+) |
| C.HA为强酸 | D.图中X表示HA,Y表示OH-,Z表示H+ |
甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g) +Q ,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
HCHO(g)+H2(g) +Q ,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
| A.Q>0 |
| B.600K时,Y点甲醇的υ(正) <υ(逆) |
| C.从Y点到Z点可通过增大压强实现 |
| D.从Y点到X点可通过使用催化剂实现 |
下列除杂方案错误的是
| 选项 |
被提纯的物质 |
杂质 |
除杂试剂 |
除杂方法 |
| A. |
C2H5OH(l) |
H2O(l) |
新制的生石灰 |
蒸馏 |
| B. |
Cl2(g) |
HCl(g) |
饱和食盐水、浓H2SO4 |
洗气 |
| C. |
NH4Cl(aq) |
Fe3+(aq) |
NaOH溶液 |
过滤 |
| D. |
Na2CO3(s) |
NaHCO3(s) |
— |
灼烧 |
下列反应所得溶液中,一定只含一种溶质的是
| A.向氯化铝溶液中加入过量的氨水 |
| B.向稀盐酸中滴入少量的NaAlO2溶液 |
| C.向稀硝酸中加入铁粉 |
| D.向硫酸酸化的MgSO4溶液中加入过量的Ba(OH)2溶液 |
下列装置不能完成相应实验的是
| A.甲装置可比较硫、碳、硅三种元素的非金属性强弱 |
| B.乙装置可除去CO2中少量的SO2杂质 |
| C.丙装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯 |
| D.丁装置可用于实验室制备氨气 |
部分弱电解质的电离平衡常数如下表,以下选项错误的是
| 化学式 |
NH3·H2O |
CH3COOH |
HCN |
H2CO3 |
| Ki(25℃) |
1.8×l0—5 |
1.8×l0—5 |
4.9×l0—10 |
Ki1= 4.3×l0—7 Ki2= 5.6×l0—11 |
A.等物质的量浓度的NaHCO3和NaCN溶液,前者溶液中水的电离程度大
B.0.1 mol/L CH3COONa 溶液显碱性,0.1 mol/L CH3COONH4溶液显中性
C.CN-+H2O+CO2→HCN+ HCO3-
D.中和等体积、等pH的CH3COOH和HCN消耗NaOH的量前者小于后者
下图为某燃煤电厂处理废气的装置示意图,下列说法错误的是
| A.使用此装置可以减少导致酸雨的气体的排放 |
| B.该装置内既发生了化合反应,也发生了分解反应 |
| C.总反应可表示为:2SO2 + 2CaCO3 + O2→2CaSO4 + 2CO2 |
| D.若排放的气体能使澄清石灰水变浑浊,说明该气体中含SO2 |
某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
关于该固体混合物,下列说法正确的是
| A.一定含有Al,其质量为4.5g |
| B.一定不含FeCl2,可能含有MgCl2和AlCl3 |
| C.一定含有MgCl2和FeCl2 |
| D.一定含有(NH4)2SO4和MgCl2,且物质的量相等 |
在实验室中,用下图所示装置(尾气处理装置略去)进行下列实验,将①中液体逐滴滴入到②中。实验结果与预测的现象一致的是
| 选项 |
①中的物质 |
②中的物质 |
预测②中的现象 |
| A. |
氢氧化钠 |
明矾溶液 |
开始时即产生白色沉淀 |
| B. |
浓硫酸 |
铜片 |
产生无色气体,溶液变蓝 |
| C. |
浓硝酸 |
用砂纸打磨过的铝条 |
产生红棕色气体 |
| D. |
稀盐酸 |
碳酸钠与氢氧化钠的混合溶液 |
开始时无明显现象 |
某药物中间体的合成路线如下:
下列说法正确的是
A.对苯二酚和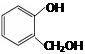 互为同系物 互为同系物 |
| B.1 mol该中间体最多可与7 mol氢氧化钠反应 |
| C.2,5-二羟基苯乙酮能发生加成、水解等反应 |
| D.该中间体分子含有羰基和羟基两种含氧官能团 |
氰氨化钙是一种重要的化工原料,其制备的化学方程式为:CaCO3+2HCN =CaCN2+CO↑+H2↑+CO2↑,下列说法正确的是
| A.CO为氧化产物,H2为还原产物 | B.CaCN2含有共价键,属于共价化合物 |
| C.HCN既是氧化剂又是还原剂 | D.每消耗10g CaCO3生成2.24L CO2 |
常温下,用0.1000 mol/L盐酸滴定25 mL 0.1000 mol/L Na2CO3溶液,滴定曲线如图。关于滴定过程中所得溶液相关微粒的浓度关系,下列说法正确的是
| A.a点:c(CO32-) >c(HCO3-) >c(Cl-) |
| B.b点:5c(Cl-)>4c(HCO3-)+4c(CO32-) |
| C.c点:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| D.d点:c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
已知:将C12通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且 的值仅与温度高低有关。当n(NaOH)=6amol时,下列有关说法正确的是
的值仅与温度高低有关。当n(NaOH)=6amol时,下列有关说法正确的是
| A.改变温度,反应中转移电子的物质的量n的范围:3amol≤n≤5amol |
| B.改变温度,产物中NaCl的最小理论产量为4amol |
| C.参加反应的氯气的物质的量3amol |
D.某温度下,若反应后 =6,则溶液中 =6,则溶液中 = = |
铝是地壳中含量最高的金属元素,其单质及其化合物在生产生活中的应用十分广泛。
23.铝原子最外层电子排布式是 ,铝原子核外有 种能量不同的电子。
24.1827年,德国化学家维勒用金属钾与无水氯化铝反应而制得了金属铝。不用钾与氯化铝溶液制铝的理由是_________;现代工业炼铝是以Al2O3为原料,与冰晶石(Na3A1F6)在熔融状态下进行电解,其阴极电极反应式为 。
25.用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:2Al+4BaO 3Ba↑+BaO·Al2O3,用化学平衡移动原理解释上述方法可制取金属Ba的原因是 。
3Ba↑+BaO·Al2O3,用化学平衡移动原理解释上述方法可制取金属Ba的原因是 。
26.LiAlH4由Li+、A1H4一构成,是有机合成中常用的试剂,LiAlH4在125℃分解为LiH、H2和Al。
(1)比较Li+、 H一、Al3+、H+离子半径大小 。
(2)写出LiAlH4分解的方程式(需配平) ,若反应生成3.36 L氢气(标准状况下),则有 g铝生成。
(3)LiAlH4与乙醛反应可生成乙醇,推断LiAlH4是反应的 剂。
物质的类别和核心元素的化合价是研究物质性质的两个基本视角。根据下图,完成下列填空:
27.上图中X的电子式为 ;其水溶液长期在空气中放置容易变浑浊,用化学方程式表示该变化 ;该变化体现出硫元素的非金属性比氧元素 (填“强”或“弱”)。用原子结构解释原因 。
28.Na2S2O3是一种用途广泛的钠盐。下列物质用于Na2S2O3的制备,从氧化还原反应的角度,理论上有可能的是______(填字母序号)。
a.Na2S+ S b.Z+ S c.Na2SO3 + Y d.NaHS + NaHSO3
29.SO2是主要大气污染物之一。工业上烟气脱硫的方法之一是用碱液吸收,其流程如图: 。
。
该法吸收快,效率高。若在操作中持续通入含SO2的烟气,则最终产物为________。室温下,0.1mol/L①亚硫酸钠 ②亚硫酸氢钠 ③硫化钠 ④硫化氢钠的四种溶液的pH由大到小的顺序是________。(用编号表示)
已知:H2S:Ki1=1.3×10-7 Ki2=7.1×10-15 H2SO3:Ki1=1.3×10-2 Ki2=6.2×10-8
30.治理含CO、SO2的烟道气,也可以将其在催化剂作用下转化为单质S和无毒的气体:
2CO(g) + SO2 (g) S(s) + 2CO2(g)。一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是 (填写字母序号)。
S(s) + 2CO2(g)。一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是 (填写字母序号)。
a.v (CO) ∶v(SO2) = 2∶1 b.平衡常数不变
c.气体密度不变 d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为 ,则SO2的转化率为 。
,则SO2的转化率为 。
铵明矾【NH4Al(SO4)2·12H2O】是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备。用芒硝(Na2SO4·10H2O)制备纯碱和铵明矾的生产工艺流程图如图1:

完成下列填空:
31.铵明矾溶液呈 性,它可用于净水,原因是 ;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是 。
32.写出过程Ⅰ的化学反应方程式 。
33.若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是 。
34.已知铵明矾的溶解度随温度升高明显增大。加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、 、过滤洗涤、干燥。
35.某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份。
(1)夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是 ;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是 (任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式 。
(2)该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)= 。
亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒。某学习小组针对亚硝酸钠设计了如下实验:
【实验一】制取NaNO2
该小组先查阅资料知:①2NO+Na2O2 →2NaNO2;2NO2+Na2O2 →2NaNO3;②NO能被酸性高锰酸钾氧化为NO3-,然后设计制取装置如下图(夹持装置略去):
36.装置D的作用是 ;如果没有B装置,C中发生的副反应有 。
37.就算在装置气密性良好的情况下进行实验,该小组发现制得的NaNO2的纯度也不高,可能的原因是 ;设计一种提高NaNO2纯度的改进措施 。
【实验二】测定NaNO2样品(含NaNO3杂质)的纯度
先查阅资料知:①5NO2-+ 2MnO4-+ 6H+ → 5NO3-+ 3Mn2+ + 3H2O;
②MnO4-+5Fe2++8H+→Mn2++5Fe3++4H2O
然后,设计如下方案测定样品的纯度。
38.取样品2.3g经溶解后得到溶液A 100 mL,准确量取10.00 mL A与24.00 mL 0.0500mol/L的酸性高锰酸钾溶液在锥形瓶中充分反应。反应后的溶液用0.1000mol/L (NH4)2Fe(SO4)2标准溶液滴定至紫色刚好褪去;重复上述实验3次,平均消耗(NH4)2Fe(SO4)2溶液10.00 mL,则样品中NaNO2的纯度为_________。
39.通过上述实验测得样品中NaNO2的纯度偏高,该小组讨论的原因错误的是 (填字母编号)。
a.滴定至溶液紫色刚好褪去,立即停止滴定
b.加入A与KMnO4溶液前的锥形瓶未经干燥
c.实验中使用的(NH4)2Fe(SO4)2溶液暴露在空气中的时间过长
已知:(Ⅰ)当苯环上已经有了一个取代基时,新引进的取代基因受原取代基的影响而取代其邻、对位或间位的氢原子。使新取代基进入它的邻、对位的取代基有—CH3、—NH2等;使新取代基进入它的间位的取代基有—COOH、—NO2等;
(Ⅱ)R—CH=CH—R′ R—CHO+R′—CHO
R—CHO+R′—CHO
(Ⅲ)氨基(—NH2)易被氧化;硝基(—NO2)可被Fe和盐酸还原成氨基(—NH2)
下图是以C7H8为原料合成某聚酰胺类物质(C7H5NO)n的流程图。
回答下列问题:
40.写出反应类型。反应① ,反应④ 。
41.X、Y是下列试剂中的一种,其中X是 ,Y是 。(填序号)
a.Fe和盐酸 b.酸性KMnO4溶液 c.NaOH溶液
42.已知B和F互为同分异构体,写出F的结构简式 。A~E中互为同分异构体的还有 和 。(填结构简式)
43.反应①在温度较高时,还可能发生的化学方程式 。
44.写出C与盐酸反应的化学方程式 。
氯吡格雷(clopidogrel)是一种用于抑制血小板聚集的药物。以芳香族化合物A为原料合成的路线如下:

45.写出反应C→D的化学方程式 ,反应类型 。
46.写出结构简式。B ,X 。
47.A属于芳香族化合物的同分异构体(含A)共有 种,写出其中与A不同类别的一种同分异构体的结构简式 。
48.两分子C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环,写出该反应的化学方程式 。
49.已知: ,设计一条由乙烯、甲醇为有机原料制备化合物
,设计一条由乙烯、甲醇为有机原料制备化合物 的合成路线流程图,无机试剂任选。(合成路线常用的表示方式为:
的合成路线流程图,无机试剂任选。(合成路线常用的表示方式为: )
)
钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化。
完成下列计算:
50.将7.8克Na2O2完全溶解于93.8克水中,所得溶液的质量百分比浓度为 。
51.将11.6克二氧化碳和水蒸汽的混合物与足量的Na2O2充分反应,固体质量增加了3.6克,则原混合气体的平均分子量为 。
52.向100 mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M(不含结晶水)。通入二氧化碳的体积V(标准状况下)与M的质量W的关系如下图所示。
(1)推断b点时M的组成成份(写出计算过程)。
(2)若向b点的盐溶液中只加入0.03mol某钠的化合物,充分反应后,减压低温蒸发得到无水Na2CO3 8.48g,则加入的物质可以是________或_______。
53.由31g NaOH和NaHCO3的固体混合物,在密闭密器中加热到250℃,经充分反应后排出气体、冷却,称得剩余固体的质量为N g,试分析不同N值时,剩余固体的组成成份(已知NaHCO3的分解温度低于250℃).
 粤公网安备 44130202000953号
粤公网安备 44130202000953号