38.4g铜跟一定量的浓硝酸反应,铜全部作用后共收集到混合气体22.4L(标准状况下),反应消耗的硝酸的物质的量为( )
| A.1mol | B.1.6 mol | C.2.2 mol | D.2.4 mol |
将1.92g铜粉与500mL一定浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况),此时,测得溶液中H+浓度为0.02mol/L,则原硝酸中溶质的物质的量是( )
| A.0.12mol | B.0.11mol | C.0.09mol | D.0.08mol |
当三份铜粉分别与足量的稀硝酸、浓硝酸、热的浓硫酸反应后,收集到的气体在相同状况下体积相等时,三份铜粉的质量比为( )
| A.3:1:2 | B.3:2:2 | C.1:1:2 | D.1:3:2 |
500mL 18.4 mol•L-1硫酸与足量的铜片加热反应,被还原的硫酸的物质的量是( )
| A.0.92mol | B.大于0.46mol 小于0.92mol |
| C.0.46mol | D.小于0.46mol |
聚合硫酸铝铁[AlaFeb(OH)n(SO4)m·xH2O]是一种新型高效净水剂,广泛应用于工业污染水的处理。
(1)聚合硫酸铝铁能够净水的原因是
(2)AlaFeb(OH)m(SO4)n•xH2O中a、b、m、n的代数关系式为_______________________。
(3)为了测定聚合硫酸铝铁的组成,进行如下实验:
步骤一:准确称取8.810g样品溶于150mL 0.100mol•L-1稀硫酸,恰好完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体10.485g;
步骤二:另取相同质量的样品,溶于过量的氢碘酸,以磁力搅拌机搅拌,充分反应后,以0.500mol•L-1Na2S2O3溶液滴定至浅黄色,滴入几滴淀粉溶液,再滴定至终点,消耗Na2S2O3溶液20.00mL.(已知:I2+2Na2S2O3=2NaI+Na2S4O6)
①步骤二中使用磁力搅拌器进行搅拌的目的是________________________。
②通过计算确定聚合硫酸铝铁的化学式(写出计算过程)。
氮化硅(Si3N4)是一种具有耐高温等优异性能的新型陶瓷,工业上可用下列方法制取:
工业上可用下列方法制取:3SiO2+6C+2N2 Si3N4+6CO.下列说法正确的是
Si3N4+6CO.下列说法正确的是
| A.氮化硅晶体属于分子晶体 |
| B.氮化硅中氮元素的化合价为-3 |
| C.上述反应中,N2是还原剂,SiO2是氧化剂 |
| D.上述反应中,每生成1mol Si3N4,N2得到6mol电子 |
12 ml 0.1mol/L的亚硫酸(H2SO3)溶液,恰好跟20ml浓度为0.02mol/L的重铬酸钾(K2Cr2O7)溶液完全反应,产物之一为H2SO4,则元素铬(Cr)在还原产物中的化合价是( )
| A.+1 | B.+2 | C.+3 | D.+6 |
实验室常利用反应:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O来制取氯气。
MnCl2+Cl2↑+2H2O来制取氯气。
(1)用双线桥法标出反应中电子转移的方向和数目。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)该反应中氧化剂是(填化学式,下同) ,氧化产物是________。
(3)该反应中氧化剂与还原剂物质的量之比为 。
(4)若有0.5 mol MnO2完全反应,则转移的电子的物质的量是 mol。
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO- 与ClO3-的离子个数比为3∶1,则Cl2与NaOH反应时被还原的氯原子与被氧化的氯原子的个数比为 ( )
| A.21∶5 | B.2∶1 | C.4∶1 | D.11∶3 |
有关KClO3+6HCl=KCl+3Cl2↑+3H2O的反应,下列说法正确的是
| A.被氧化的元素原子个数与被还原的元素原子之比为6:1 |
| B.还原产物与氧化产物的质量之和为287.5g |
| C.KClO3失去6mol电子,HCl得到6mol电子 |
| D.ClO3-和Cl-在酸性环境中可能不能共存 |
(1)用单线桥表示下列反应中电子转移方向和数目:
KIO3+6HI =KCl+3H2O+3I2
(2)钙元素是人体必需的常量元素,所有的细胞都需要钙元素,测定人体血液中钙元素的含量常用到如下两个反应:
①CaC2O4+H2SO4=H2C204+CaSO4
②2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
上述反应②的还原剂是__________;若收集到44.8mL(标准状况)的CO2时,消耗氧化剂__________ mol,有__________mol电子发生转移,相当于测出含钙元素的质量是_____g。
某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中ClO-的物质的量随时间变化的曲线如图所示。下列判断不正确的是( )

| A.反应的氧化剂是ClO- |
| B.消耗1mol还原剂,转移电子3mol |
| C.氧化剂与还原剂的物质的量之比为2:3 |
| D.反应后溶液的酸性明显增强 |
在含有nmolFeI2的溶液中通入Cl2,有xmolCl2发生反应,下列说法正确的是( )
| A.当x≤0.5n时,反应的离子方程式为:2Fe2++Cl2===2Fe3++2Cl- |
| B.当x≥n时,反应的离子方程式为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| C.当Fe2+和I-都被氧化时,x的最小值须大于0.5n |
| D.当x=n时,反应后氧化产物的物质的量为nmol |
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(主要成分为FeS2)是生产硫酸的冶炼钢铁的重要原料。高温下可发生反应:其中一个反应为:3FeS2+8O2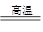 6SO2+Fe3O4,该过程若有1.5mol FeS2参加反应,则反应过程中转移_____ mol电子;
6SO2+Fe3O4,该过程若有1.5mol FeS2参加反应,则反应过程中转移_____ mol电子;
(2)氯化铝溶液显酸性,原因是_________________________(用离子方程式稀释);
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素(CO(NH2)2;它易被氧化),原理如下图所示。
①电源的负极为_________(填“A”或“B”)。
②阳极室中发生的反应依次为_________、_________。
③电解结束后,阴极室溶液的pH与电解前相比将_________;若阴极共收集到气体6.72L(标准状况),则除去的尿素为________ g(忽略气体的溶解)。
(4)为了减少CO对大气的污染,某研究性学习小组拟研究利用CO和H2O反应转化为绿色能源H2。已知:2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•moL-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•moL-1
H2O(g)═H2O(l)△H=-44.0kJ•moL-1
写出CO和H2O(g)作用生成CO2和H2的热化学方程式:_________。