化学课上老师表演了一个小魔术——“无中生有”:相同条件下,向A、B两个体积相同的集气瓶中分别充满无色干燥的硫化氢(H2S)气体和二氧化硫气体。如图所示,抽开毛玻璃片,瓶口对紧,颠倒几次,使两种气体充分混合。一会儿,观察到两瓶内壁附着淡黄色固体颗粒,同时瓶壁上有小水珠出现。请根据现象回答下列问题:
(1)上述反应的化学方程式为_________________.
(2)如果这两个瓶子是质地较软的塑料瓶,会观察到 ,原因是_______。
(3)已知:相同条件下,相等体积的气体所含的分子数目相等。反应完毕,瓶中剩余的气体为____________(填化学式)。
(5分)某化学小组的同学欲对某种塑料的组成进行分析研究(资料显示该塑料只含C、H两种元素),他们设计了如下图所示的实验装置。目的是通过测量有关数据,推算塑料组成元素的含量(图中字母A至G均表示装置序号)。
请根据实验装置,回答下列问题:
(1) A装置制取的氧气中混有少量CO2和水蒸气,为使D装置中塑料试样在纯氧中燃烧,用于除去CO2的装置为 (填装置序号);反应的化学方程式为 。
(2)气体的吸收装置E中的试剂为 。
(3)碱石灰的成分是氢氧化钠和氧化钙,G装置的作用是 。
某课外小组研究“影响H2O2生成O2快慢的因素”的课题。通过查阅资料,他们提出如下猜想。
【提出猜想】催化剂和反应物浓度都会影响H2O2生成O2 的快慢
【实验过程】实验装置图如下:

实验操作:检查装置气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录
| 实验编号 |
① |
② |
③ |
| 反应物 |
5%H2O2 100 mL |
5%H2O2 |
3%H2O2100 mL |
| 加入固体 |
0.5 g氯化钠固体 |
0.5 g二氧化锰 |
|
| 收集气体的时间 |
165 s |
46s |
80 s |
(1)H2O2溶液和二氧化锰制取氧气的化学方程式为 。
(2)实验②中加入H2O2的体积为 mL。
(3)实验③中加入的固体和用量为 。
【结论】该探究过程得出的结论是 。
【反思】H2O2在常温下分解缓慢,加入MnO2 后反应明显加快。小红提出,为了更好的证明二氧化锰和氯化钠是否对H2O2生成O2快慢有影响,还应该增加一组对比实验。该实验选用的药品和用量为 。
【实验拓展】小红用收集的气体进行氧气的性质实验。
(1)检验氧气的方法是 。
(2)小红发现用该气体进行氧气的性质实验,现象都不明显。造成这种结果的原因是 。
某校化学兴趣小组的同学设计实验验证红热的铁与水蒸气反应生成氢气,设计的实验装置图如下图。
请回答下列问题。
(1)若干燥从a导管出来的气体,应从 (选填“b”或“c”) 端管口通入。
(2)点燃生成的气体,产生 色火焰。点燃前应进行的操作名称是 。
(3)已知试管内湿棉花不参加化学反应,它的作用是 。
(4)该小组同学用生成的氢气与氧化铁反应,反应的化学方程式是: 3H2 + Fe2O3 2Fe + 3H2O实验装置如右图。该实验观察到的现象有 。
2Fe + 3H2O实验装置如右图。该实验观察到的现象有 。
根据下图回答问题。
A B C D E
(1)实验仪器a的名称是 。
(2)实验室用高锰酸钾制取氧气的化学方程式为 ,所选用的发生装置是 (填字母序号,下同)。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气时,二氧化锰起 作用。
(4)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____。实验室制取氧气和制取二氧化碳都可选用的收集装置是_____。
轻质碳酸钙可用作牙膏摩擦剂。工业上常用石灰石(含有少量杂质)来制备比较纯净的轻质碳酸钙。
已知:①石灰石高温煅烧可以生成生石灰和二氧化碳,此外还有少量不反应的杂质剩余。
②生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆。
某实验小组同学设计了2种转化流程,如下图所示。
请回答下列问题:
(1)石灰石高温煅烧反应的化学方程式是 。
(2)物质B为 。
(3)反应④的化学方程式是 。
(4)操作Ⅱ应采用的方法是 。
(5)采用反应①②③制备轻质碳酸钙的方法优点有(写出一种即可) ;采用反应①②④制备轻质碳酸钙的方法优点有(写出一种即可) 。
现有三种常见的矿石,分别是铁矿石、硫酸铜和石灰石中的一种。某化学兴趣小组对这三种矿石的成分产生兴趣,进行以下研究。请根据初中所学知识,回答下列问题:
(1)三种矿石中只有一种为白色固体,放入水中后不溶解,初步判断该矿石可能为 。为了进一步证明,取少量该矿石于试管中,加入稀盐酸,产生大量气泡,该气体可使澄清石灰水变混浊。反应的化学方程式是 、 。
(2)第二种矿石放入水中,矿石逐渐溶解,并形成了蓝色溶液。向所得溶液中插入一根铁丝,一段时间后,铁丝上有红色物质析出,该反应的化学方程式为 。
(3)第三种矿石的主要成分X由两种元素组成。已知120 g X和氧气充分反应,生成一种无色有刺激性气味的气体128 g,该气体会导致酸雨。X的化学式为 。
根据下图回答问题。
(1)仪器a的名称是 ,装置A中是用 法收集气体。
(2)实验室用装置B完成的实验是 (填字母序号)。
a.加热高锰酸钾制取氧气
b.过氧化氢溶液与二氧化锰混合制取氧气
c.大理石与稀盐酸反应制取二氧化碳
(3)装置C中玻璃管内可以观察到的现象为 ,发生反应的化学方程式为 ,澄清石灰水中发生反应的化学方程式为 。
某化学小组同学利用以下三组装置探究燃烧条件。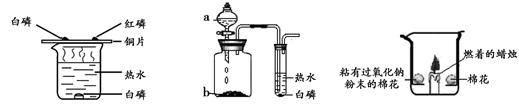
图1 图2 图3
(1)如图1所示,能燃烧的物质是 (填字母序号),燃烧反应的化学方程式为 。
A.水中的白磷 B.铜片上的白磷 C.铜片上的红磷
(2)如图2所示,将液体a滴入瓶中并与固体b接触,能观察到白磷燃烧,则瓶内发生反应的化学方程式为 。
(3)如图3所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:① ;②粘有过氧化钠的棉花燃烧;③未粘有过氧化钠的棉花不燃烧。通过上述实验的对比分析,写出产生现象②的原因 。
完成三组实验之后,同学成功探究出了燃烧所需要的条件。
为探究四瓶未知无色溶液的成分,甲、乙、丙三组同学分别设计了如下实验。已知四种溶液分别是Na2CO3、NaOH、Ca(OH)2和稀盐酸中的一种。
【实验过程】
甲组实验方案:将四瓶溶液标号分别为1、2、3、4,只利用紫色石蕊溶液进行实验。
| 实验步骤和操作 |
实验现象和结论 |
||
(1)如图所示: |
① 2号溶液由无色变为红色, 则2号溶液是 ② 另三支试管中溶液均由无色变蓝色 |
||
(2)另取1、3、4号溶液,分别滴加2号溶液
|
① 3号溶液中有气泡放出, 则3号溶液是 ② 另外二支试管中溶液无明显变化 |
||
| (3)另取1、4号溶液,分别滴加 |
①1号溶液中有白色沉淀析出, 则反应的化学方程式为 ② 另一支试管中溶液中无明显变化 |
乙组实验方案:不用其他试剂进行实验。
| 实验操作 |
实验现象 |
实验结论 |
| 任取三种溶液于三支试管中,分别滴加第四种溶液 |
①一支试管中有气泡放出 其余二支试管中溶液无明显变化 |
① 第四种溶液为稀盐酸 |
| ② 一支试管中有白色沉淀析出, 其余二支试管中溶液无明显变化 |
② 第四种为Na2CO3溶液 |
|
| ③ 三支试管中溶液均无明显变化 |
③ 第四种为NaOH溶液 |
【实验分析】
经过交流后,发现实验结论 (填序号)是不正确的;若该结论作正确,对应的实验现象应是 。
丙组实验方案:将四种溶液编号为1、2、3、4,不用其他试剂进行实验。
| 实验操作 |
实验现象 |
实验结论 |
||
如图所示:
|
①A、B、C均无明显变化 ②D中有沉淀析出 |
标号为1、2、3、4的溶液依次为(用化学式表示): 或 |
某化学小组对“SO2能否与H2O反应生成酸”的课题开展探究。
【查阅资料】
(1)SO2有毒,常温下是一种无色气体,易溶于水。
(2)酸能使蓝色的石蕊试纸变成红色。
【实验过程】
(1)常温下,实验室用稀硫酸与固体亚硫酸钠反应制取SO2。下列气体的制备装置能用于制备SO2的是 (填序号)。
A.加热高锰酸钾制氧气
B.稀盐酸与大理石反应制二氧化碳
C.过氧化氢分解(二氧化锰作催化剂)制氧气
(2)右图A中,实验时,A中蓝色石蕊试纸的颜色始终没有变化,由此得出的结论是 。
(3)右图B中,在通入SO2之前,将滴管内的水滴到试纸上, 试纸颜色没有发生变化,
由此得出的结论是 ,当有SO2通过时,湿润的蓝色石蕊试纸变红,由此得出的结论是 。
(4)该实验中尾气处理的方法是:将其通入 溶液中。
根据下列三组实验回答问题。
(1)图中仪器a的名称是 ;三组实验都用到的玻璃仪器是 。
(2)指出甲实验中不正确的操作 。
(3)乙实验中,燃烧匙中装入的药品应为 ,其反应的实验现象是 。
(4)丙实验中,正确的操作顺序为(填序号):⑤→ → → → ②。
通过半年的化学学习,你对化学实验有了一些认识,请你解答下列问题:
(1)在电解水的实验中,两电极相连的玻璃管上方产生的气体是 和 ,两者的体积比约为 ,这个实验证明了水是由 组成。该反应的化学方程式为 。
(2)根据下图所示实验装置回答下列问题:
①用氯酸钾和二氧化锰混合加热制取O2应选用的发生装置(填序号,下同)____;若用高锰酸钾加热制取O2该装置还需做的一点改动是 ;用过氧化氢溶液和二氧化锰混合制取O2应选用_________;制取H2应选用__________;
制取CO2应选用_______,反应的化学方程式为 。 ②收集O2可选用________, 理由是 ; 收集CO2应选用 。(3).过滤操作中的要点常简记为“一贴二低三靠”,请你解释“三靠”的具体含义:。
“三靠”:① ,② ,
③ 。
过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水。分液漏斗可以通过调节活塞控制液体滴加速度。回答下列问题: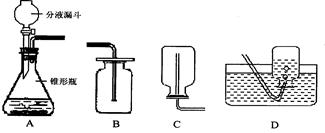
⑴分液漏斗中应放入的物质是 ,锥形瓶中应放入的物质是 。
⑵要收集一瓶纯净的氧气应选择上图中的装置 (填字母)
⑶某同学在观察到锥形瓶内有大量气泡时,开始用C装置收集氧气,过一断时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃。其原因是 。
⑷若实验时用此法代替高锰酸钾加热制氧气,优点是 (填序号)
A.生成物中只有氧气 B.不需加热 C.需加热
⑸装置A中反应剧烈,据此提出实验安全注意事项是( )
A.控制液体的滴加速度 B.用体积小的锥形瓶 C.加热反应物