金属材料的使用,推动了人类文明的快速发展。

(1)铝是现代文明不可缺少的物质基础。
①铜、铁、铝在自然界中均主要以化合物的形式存在,但人类大量冶炼和使用金属铝的时间较晚,主要原因是 (填字母)。
A.地壳中铝元素含量较低
B.铝较活泼,难以寻找到合适的物质将其从矿物中还原出来,冶炼技术要求高
②将未经砂纸打磨和打磨过的铝片同时放入盛有稀硫酸的同一烧杯中,发现一段时间内未经打磨的铝片表面没有明显现象,原因是 ;经打磨过的铝片表面有气泡产生,反应的化学方程式为 。
(2)中国高铁技术令世界瞩目。如果你是未来的一名高铁设计师,请根据下表给出的信息,选择制造高铁轨道的金属材料。你选择 ,理由是 。
|
金属硬度(以金刚石的硬度10作为标准) |
铬 铁 银 铜 金 铝 铅 |
|
(大)9 4~5 2.5~4 2.5~3 2.5~3 2~2.9 1.5(小) |
|
|
地壳中金属元素含量 |
铝 铁 钾 镁 铬 铜 |
|
(高)7.73% 4.75% 2.47% 2.00% 1×10﹣2% 5×10﹣3%(低) |
|
|
金属材料市场价格 (万元/吨) |
银 铜 铬 铝 锌 铅 生铁 |
|
(高)496 6.87 6.6 2.276 2.267 1.43 0.485 (低) |
(3)某学习小组对实验室制得的一种蓝色固体物质产生了浓厚的兴趣,老师告诉同学们该物质的化学式可表示为 ,其受热分解生成 、 和 。他们设计如图装置进行实验,通过测定 和 的质量,确定 中 、 的比值。(已知:碱石灰能吸收 和 ,不能吸收 ;B、C、D中药品均足量)
①实验开始前,应先检查 。
②装置中B和C的位置 (填“能”或“不能”)调换。
③ 解完全后需再通入一定量的 ,目的是 。
④B、C反应前后质量增加分别为m g和n g,则 = (用含m、n的代数式表示)。
化学课上,某小组同学利用老师提供的实验器材,设计了一套简易“供氧器”。
【反应原理】根据设计的“反应器”,制取氧气的反应原理 (用化学方程式表示)。
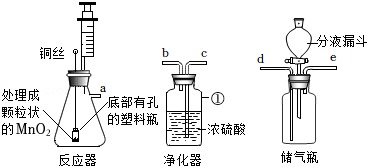
(1)图中标号①仪器的名称 。
(2)为制取干燥的氧气,装置接口连接的正确顺序为 (填选项)。
A.a→b→c→d
B.a→b→c→e
C.a→c→b→d
D.a→c→b→e
(3)制取氧气的过程中,检验“储气瓶”氧气已存满的方法是 。
(4)反应发生后,使反应停止的操作是 。
(5)当反应停止,取出“储气瓶”中氧气的操作为 。
【拓展】图装置还可制取 气体,反应的化学方程式为 。
金属材料的使用与生产、生活和社会发展密切相关。
(1)金属冶炼。利用 与 的反应炼铁,反应的化学方程式为 。
(2)金属材料的使用和保护。
①“贵州桥梁”闻名世界。桥梁建造中使用大量钢材作支架,钢是铁的合金,钢的硬度比纯铁的 (填“大”或“小”)
②铁制品在潮湿的空气里容易生锈,防止铁生锈的措施有 。铁也易被酸腐蚀,写出铁与盐酸反应的化学方程式 ,该反应的基本类型是 。
(3)比较 、 、 的金属活动性。

①将一定量的硫酸铜溶液加入锌粉和铁粉的混合固体中,反应的示意图如图所示,分析可知,实验中发生反应的化学方程式为 ,可得结论: 。
②在上述实验中继续添加一定量硫酸铜溶液,微粒种类和数量的变化情况为 时,可得结论:金属活动性 。
水是生命之源,是人类生产、生活中不可缺少的重要物质。
(1)生活中使用活性炭净化水,利用了活性炭的 性。
(2)化学实验室中经常用到水,如溶液的配制。配制50g溶质质量分数为6%的氯化钠溶液,需要氯化钠质量为3g,需要水的质量为 g。
(3)水常用作物质溶解的溶剂。

① 与 在水中的溶解度曲线如图1所示,20℃时, 的溶解度为 g。
② 中混有少量 ,提纯 可采用的方法是 。
③10℃时,将等质量的 、NaCl固体,分别加入到盛有100g水的两个烧杯中,搅拌,充分溶解,现象如图2所示。烧杯中一定是饱和溶液的是 (填“ ”或“ ”)溶液。
④ 溶解度曲线如图3所示,将A点对应的 溶液溶质质量分数增大,采取的方法是 。
完成下列实验并解决实际问题。

(1)探究燃烧的条件。如图1所示实验,甲中白磷不燃烧,乙中白磷燃烧,则可知燃烧的条件之一是 。
(2)实验室制取气体。根据图2,回答问题。
①若制取 ,请填写如表
|
制取气体 |
反应原理(用一个化学方程式表示) |
反应原理对应的制取装置(填字母) |
检验该气体方法 |
|
|
②若制取 ,发生反应的化学方程式为 ,制取装置可选用 (填字母)。
(3)北京冬奥会火炬采用氢气为燃料,首次实现冬奥会火炬零碳排放、首次开展机器人与机器人之间水下火炬传递。水下火炬传递上演极富美感的“水火交融”景象,从燃烧条件角度分析,你认为实现火炬水下燃烧,需要解决的问题有 。
如图是我国古代钱币之一,其“外圆内方”应“天圆地方”之说,寓意和谐顺畅。某同学构建了如钱币模型的常见不同物质关系图。H为农业上配制波尔多液的盐,A、C、D属于不同类别的物质,H、E、F物质类别相同(“一”表示相连两种物质或其溶液能发生化学反应,“→”表示物质或其溶液间存在相应的转化关系,部分反应物、生成物及反应条件已略去)。
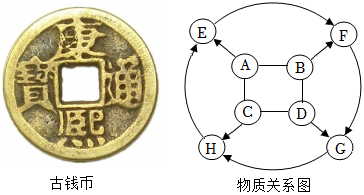
(1)H的化学式是 。
(2)A﹣C反应的化学方程式为 。
(3)D→G反应的化学方程式为 ,写出D物质的一种用途 。
为防止全球温室效应的加剧,我国承诺在2060年实现“碳中和”, 的捕捉是减少碳排放的有效措施。如图是实际生产中采用足量 溶液来“捕捉” 的工艺流程:
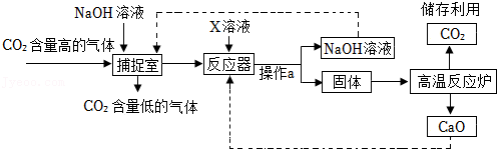
(1)操作a的名称是 。
(2)“捕捉室”中 溶液采用喷雾方式加入,目的是 ,发生反应的化学方程式为 。
(3)“捕捉室”中的 溶液与“反应器”中的X溶液可否互换?原因是 。
(4)整个流程中可以循环使用的物质是 (填化学式)。
将二氧化碳转化为有机物是实现“碳中和”的途径之一,我国科学家研制了全球首套捕集二氧化碳合成甲醇( )的装置,有利于实现“碳中和”。以下是将二氧化碳在一定条件下转化成 的工艺流程图。
查阅资料:甲醇常温下是一种无色液体,易溶于水,熔点﹣97.8℃,沸点64.7℃。

(1)实验室进行过滤操作需要用到的玻璃仪器有 (填一种即可)。
(2)请写出铁和水蒸气发生反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
(3)
合成
的化学方程式:
 。该反应使用过量
的原因是 。
。该反应使用过量
的原因是 。
(4)请你设计分离出 的一种方案: 。
(5)我国“天问一号”抵达火星,发现火星低层大气中二氧化碳含量很高,其成分如下:
|
气体成分 |
|
|
Ar |
|
其他 |
|
体积分数/% |
95.32 |
2.7 |
1.6 |
0.13 |
0.25 |
人类生活离不开空气和水,若为满足人类未来在火星上生活需求,请你提出一种合理的研究设想 。
氮化镓是生产5G芯片的关键材料之一。图1是元素在元素周期表中的相关信息图,图2是氮原子和原子的原子结构示意图。请回答下列问题:

(1)由图1可知镓原子的原子序数是 。
(2)图2中的x是 。氮化镓的化学式为 。
(3)镓( )与常见金属铝有相似的化学性质。两种金属的活动性比较,镓 铝(填“>”或“<”),请从原子结构的角度分析原因 。
(4)写出镓( )与稀盐酸反应的化学方程式 。
根据 和 的溶解度表和溶解度曲线,回答下列问题:
温度/ |
|
|
|
|
溶解度/ |
|
|
|
|
|
|
|
|
|
(1) 时, 的溶解度为_____ ;
(2) 和 两种物质的溶解度受温度影响较小的是_____;
(3)按照如图进行实验,各步操作均已充分溶解,忽略实验过程中溶剂的挥发。下列说法正确的是_____。

| A. | 烧杯a和b内,溶液中溶质的质量分数: |
| B. | 烧杯a和d内,溶剂质量: |
| C. | 烧杯c和f内,上层清液中溶质的质量分数: |
| D. | 烧杯c和f内,剩余固体质量: |
| E. | 烧杯b内,溶液中溶质的质量分数约为 |

如图是实验室制取气体的常用装置,回答下列问题:
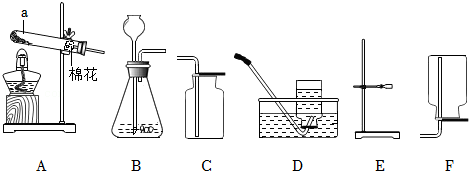
(1)玻璃仪器a的名称是_____;
(2)实验室用加热高锰酸钾固体的方法制取氧气。
①写出该反应的化学方程式__________;
②用该方法制取氧气的发生装置应选择_____(填图示中的序号);
③氧气的收集装置可选择_____(填图示中的序号)。
钢铁的生产和使用是人类文明和社会进步的一个重要标志。回答下列问题:
(1)赤铁矿(主要成分是 )可用于炼铁。 中铁、氧元素质量比为_____;
(2)钢是一种铁合金。钢和纯铁相比硬度较大的是_____;
(3)将打磨后的铁丝放入硫酸铜溶液中,铁丝表面有红色物质生成,说明铁比铜的金属活动性_____(填“强”或“弱”)。
人类的日常生活、工农业生产和科学研究都离不开水。回答下列问题:
(1)生活中区分硬水和软水,常用的物质是_____;
(2)自来水厂常利用活性炭的_____性,除去水中的异味;
(3)农业和园林浇灌时,改大水漫灌为喷灌、滴灌,主要目的_____;
(4)实验室用氢氧化钠固体和水配制溶液,其中作溶剂的是_____。
如图是某牙膏成分表的一部分。回答下列问题:
X X牙膏 成分:二氧化硅、水、纤维素胶、 碳酸钠、香精、单氟磷酸钠、碳酸氢钠...... |
(1)牙膏属于_____(填“混合物”或“纯净物”);
(2)含氟牙膏能预防龋齿,这里的“氟”指的是_____(填“分子”“原子”或“元素”);
(3)二氧化硅( )中硅元素的化合价为_____;
(4)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使人产生痛痒感。在叮咬处涂抹牙膏就可减轻痛痒,说明该牙膏呈_____(填“酸性”“碱性”或“中性”)。