某实践小组参观本地矿泉水厂,该厂矿泉水含钙、钾等矿物质,其生产流程示意图如图。回答下列问题。
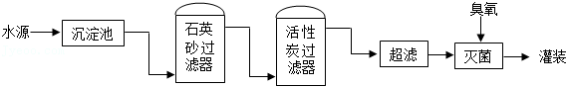
(1)矿泉水中的钙、钾指的是_____(填“元素”或“单质”)。
(2)活性炭过滤器中活性炭的作用是_____。
(3)超滤是利用薄膜(仅允许小分子和离子通过)进行物质分离的技术。若水源中含有下列物质,推测该流程中“超滤”的主要作用是除去_____(填字母序号)。
| A. | 难溶性大颗粒 |
| B. | 可溶性无机盐 |
| C. | 可溶性高分子化合物 |
(4)臭氧的化学式 的微观意义是_____(写出1点即可)。
(5)生活中,你提倡饮用白开水还是矿泉水,理由是_____。
实验室现有高锰酸钾、块状石灰石、稀硫酸、稀盐酸、浓盐酸、棉花以及下列仪器及装置。请你回答有关问题。

(1)仪器①的名称是____。
(2)利用上述仪器和药品制取氧气,反应的化学方程式为____________,利用装置A制氧气还需改进的地方是____________,在上述收集气体的装置中,不能用于收集氧气的是____(填代号)。
(3)实验室常用装置B和________(填药品名称)制取 ,其反应的化学方程式为________。若使用装置F作为制取 的发生装置,与装置B比较,除了利用废物的优点外,请写出其他一个优点________,该装置使用铜丝网而不使用铁丝网盛放固体的原因是____________(用化学方程式表示)。
(4)若用装置G来干燥制取的二氧化碳,则气体应从____(填“a”或“b”)口进入。
用如图所示实验研究金属的性质。

(1)①中有气体生成,生成的气体为_______。
(2)③中反应的化学方程式为 ______________。
(3)下列实验组合中,能得出铁、铜、银的金属活动性顺序的是 _______(填序号)。
| A. | ①④ |
| B. | ③④ |
| C. | ①②④ |
如图所示,向井穴板的孔穴 中滴加稀盐酸, 中滴加无色酚酞溶液。
(1) 中所得溶液的颜色为_______。
(2)从 中任选一个,写出发生反应的化学方程式:_____________________。
(3) 中无明显现象的是_______(填序号)。

用如图所示实验验证可燃物燃烧的条件。
已知:白磷和红磷的着火点分别为 。
(1)铜片上的白磷燃烧而红磷不燃烧,说明可燃物燃烧的条件之一是______________。
(2)能验证可燃物燃烧需要与 接触的现象是______________。
(3)热水的作用是______________。

用如图装置进行实验,向瓶中依次加入 和稀硫酸,塞紧胶塞。
(1)瓶中发生反应的化学方程式为_____________________。
(2)观察到干纸花不变色,湿纸花变红。湿纸花变红的原因是 ____________________________。

根据如图所示实验回答问题。

(1) 中,仪器 的名称是_______; 分解的化学方程式为_____________________。
(2) 中,铁丝燃烧生成的黑色固体是_______。
(3) 中,电解水反应的化学方程式为______________;一段时间后,关闭电源,将带火星的木条放在 口处,打开活塞,观察到______________,说明有 生成。
铜制品长期露置在潮湿的空气中会因锈蚀生成“铜绿”[化学式为 ]而使其表面变成绿色。
(1)小花同学根据铜绿成分做出猜想:金属铜锈蚀的条件除了有氧气和水外,还必须有二氧化碳,为了证明“必须有二氧化碳”,需要进行下列实验中的 _____(选填实验编号)。

(2)小花和同学们利用废旧品中锈蚀严重的废铜屑为原料(假设不含其他杂质)设计了两个方案回收铜。
【查阅资料】a.

b.

【分析评价】
①X为碳的氧化物时,步骤Ⅱ中发生反应的化学方程式为_____________。
②步骤Ⅴ过程中观察到的实验现象为____________________。
③以上两个方案中,你认为哪一个方案更优越并说明理由__________(理由写一点)。
【拓展探究】
(3)氢气也能将氧化铜还原为铜。小红和小强各取 氧化铜用氢气还原,反应一段时间后,两份固体均全部变红。小红和小强所得红色固体质量分别为 和 。
提出问题:红色固体中含有哪些物质?
查阅资料:c.氢气还原氧化铜时也可产生氧化亚铜( )。
d.氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。
分析推断:小红得到的红色固体中含有的物质为_____(填化学式)。
实验检验:请设计简单实验检验小强得到的红色固体的成分 __________________________________________________。
如图为实验室常用的实验装置,请回答:

(1)写出标号仪器的名称:①_____,②_____。
(2)实验室常用一种固体和一种液体制取氧气,该反应的化学方程式为____________________,氧气能用 装置收集是因为氧气 _____溶于水。
(3)若用 装置干燥二氧化碳气体, 装置中应盛装的试剂为_____。
(4)氯气是一种有毒的气体,密度比空气大,能溶于水并与水发生反应。实验室常用浓盐酸和二氧化锰共热制取氯气。为了便于连接尾气处理装置,实验室制取并收集氯气应选择的装置为 _____(填装置序号)。
掌握实验室制取气体的方法是初中生必备的实验技能。如图是制取气体的常用装置,回答下列问题。

(1)仪器a的名称为_____。
(2)实验室制取氧气,可选择的发生装置和收集装置是__________(写一种组合),该反应的化学方程式为_________________________。
(3)用装置D收集二氧化碳时,其验满的方法是_________________________。
化学是一门以实验为基础的科学。回答下列问题:
(1)实验室中常见的气体发生装置及收集装置如图。

①选用装置 制取气体时,对药品和反应条件的要求是_______________。
②仪器 的名称是_____,实验时为防止气体从该仪器的上口逸出,应采取的措施是__________。
③铁和稀盐酸反应制取氢气的化学方程式是__________,若用排空气法收集氢气,气体应从装置 的_____(填“b”或“c”)端进入。
(2)向试管中加入 蒸馏水,滴入 滴石蕊溶液(图Ⅰ),按图Ⅱ、Ⅲ依次进行实验。

①Ⅲ中观察到的实验现象是_____。
②由于 的干扰,该实验不能直接证明使石蕊溶液变色的物质一定是 。设计实验方案排除 的干扰 _________________________。
某化学兴趣小组研究影响化学反应快慢的因素。
(1)下图是实验室中常用的仪器
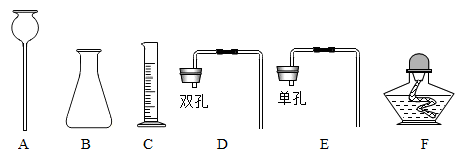
①仪器A的名称是_______。
②从上图中选择合适的仪器组装一套 发生装置,要求添加盐酸无需拆开装置,需要用到的仪器有哪些?_______(填标号)
(2)该小组的实验设计和数据记录如下表。每个实验均在反应开始后,就立即用排水法连续收集多瓶 ,表中“—”表示气泡太少,不再收集。
序号 |
反应物 |
收集每瓶气体所用时间(单位:秒) |
|||||||
盐酸 浓度 |
盐酸 体积 |
大理石 形状 |
第1瓶 |
第2瓶 |
第3瓶 |
第4瓶 |
第5瓶 |
第6瓶 |
|
实验1 |
|
|
小颗粒 |
|
|
|
|
|
|
实验2 |
块状 |
|
|
|
|
|
|
||
实验3 |
|
|
小颗粒 |
|
|
|
|
|
|
实验4 |
块状 |
|
|
|
|
|
|
||
实验5 |
|
|
小颗粒 |
|
|
|
|
|
— |
实验6 |
块状 |
|
|
|
— |
— |
— |
||
①该小组研究了哪些因素对反应快慢的影响?_______
②为了分析浓度对反应快慢的影响,可对比表中实验_______(填标号)。
| A. |
|
B. |
|
C. |
|
D. |
|
③根据实验数据反映出的规律,表中数值 的合理范围是:_______< <_______。
(3)该小组在反应开始后立即收集第1瓶气体,你认为该做法合理吗?说出你的观点并阐述理由。__。
镓( )及其化合物应用广泛,常用于半导体、合金、磁性材料等领域。已知镓在化合物中常为 价,金属活动性顺序: 。
(1)镓的氧化物的化学式为_______。
(2)氢氧化镓是难溶于水的白色固体。
①上述信息中能用于推测氢氧化镓化学性质的是_______(填标号)。
| A. | “氢氧化镓” |
B. | “难溶于水” |
C. | “白色固体” |
②取少量氢氧化镓固体于试管中,加入无色溶液X,充分振荡后固体完全溶解。溶液 可能是____或______。(填化学式)
(3)设计金属镓转化为氢氧化镓的一种方案:_______(依次写出化学方程式)。
某兴趣小组用氯酸钾和二氧化锰制取氧气。可能用到实验装置如图所示:

请回答下列问题:
(1) 仪器的名称_____。
(2)写出用该方法制取氧气的化学方程式_______________,其中二氧化锰的作用是_____,制取并收集干燥的氧气应选用_____(填实验装置图字母序号)。
(3)氯酸钾完全分解后,为了回收二氧化锰和氯化钾,又进行了如下实验操作:

实验操作中,操作①的名称是_____;实验操作②应选择上述图中的_____(填实验装置图字母序号)。
(4)实验结束后,同学们在拆卸装置时闻到刺激性气味。他们将回收得到的 称量,发现其质量小于加热前 的质量。查阅资料后发现,加热 和 混合物的反应过程如下:
第一步:

第二步:
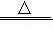
第三步:

拆卸装置时闻到刺激性气味的气体是_____,根据以上信息写出加热后剩余固体中 质量小于加热前 质量的原因_______________。
某同学欲用 固体配制溶质质量分数为 的 溶液 ,用于制作“叶脉书签”。回答下列问题:
(1)为完成实验,除下列仪器外,还须用到的仪器(如图1)名称是_____。

(2)该同学称量 固体质量之前,先用托盘天平称量烧杯的质量。称量时,他把烧杯和砝码的位置放反了,天平平衡后,砝码的总和是 ,游码的位置如图2所示,则烧杯的实际质量为_____ 。

(3)该同学用 量筒量取实验所用的蒸馏水,读数视线如图3所示,量筒中水的实际体积为_____ ;若其他操作均正确,该同学所配 溶液中溶质的质量分数 _____(填“>”“<”或“=”) 。(水的密度为 )
(4) 溶液长时间露置于空气中会变质生成 ,发生反应的化学方程式为 _______________;实验室里用于盛装 溶液的试剂瓶是____________________(填“带磨口玻璃塞的广口瓶”或“带橡胶塞的细口瓶”)。
(5)氢氧化钠有强烈的腐蚀性,如果不慎沾到皮肤上,要先用大量的水冲洗,再涂上_____溶液。