定律是对自然现象或关系的描述,通常可用数学方式加以表达。在学习“质量守恒定律”时,小丽查阅到以下材料:
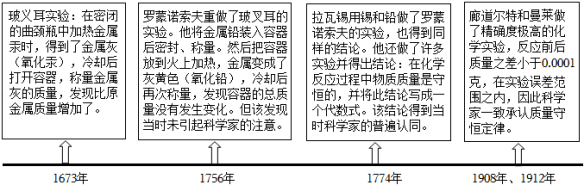
(1)玻义耳实验中,金属灰增加的质量是 ;
(2)质量守恒定律的发现过程,带给我们的启示有 (填字母);
A.要善于总结前人的成果和经验
B.实验的成功与否,取决于药品的选择
C.定量方法是科学研究的重要方法
受上述研究启发,小丽对相关实验进行了深入探究。
(3)在白磷燃烧前后质量测定实验中(如图),气球的作用有 ;

(4)小丽认为,蜡烛燃烧后剩下的固体质量比燃烧前少了,因此该现象不符合质量守恒定律。请你设计一个能说服小丽的简明实验思路 。
化学是一门以实验为基础的科学。请结合图示回答问题:

(1)仪器①的名称为 。
(2)实验室用高锰酸钾制取氧气的化学方程式为 。用B、E装置制取并收集氧气,实验操作步骤有:①点燃酒精灯,待气泡连续均匀放出时收集气体;②熄灭酒精灯;③装入药品,放置棉花并固定仪器;④连接好装置,检验装置的气密性;⑤从水槽中撤出导管。正确的操作顺序是 (填标号)。
a.③④①②⑤
b.④③①⑤②
c.④③①②⑤
d.③④①⑤②
(3)进行铁丝在氧气中燃烧的实验,集气瓶底部加入水或细沙的目的是 。
(4)实验室用锌粒和稀硫酸制取氢气,应选择的发生装置是 (填标号,下同),可选择的收集装置是 (填一种即可)。
(5)现有一新制的碳酸钙产品,某同学设计如图所示的实验,通过测定反应生成的 的质量来确定该产品中 的含量(图中夹持仪器已略去,杂质不与盐酸反应,碱石灰是 和 的固体混合物)。

①关闭止水夹,打开分液漏斗活塞,缓慢滴加盐酸至不再有气泡产生,关闭分液漏斗活塞;打开止水夹,缓缓通入空气。通入空气的作用是 。
②装置D的作用是 。
③实验时,称取的碳酸钙产品的质量为 ,反应后得到 的质量为 ,则该产品中 的质量分数为 (用含 和 的代数式表示)。
“对比实验”是科学探究中的常用方法。甲、乙、丙三组对比实验如图所示,请回答下列问题:
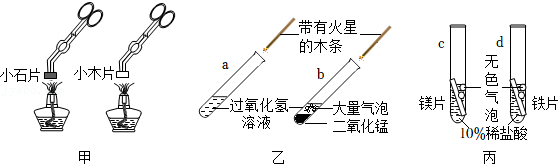
(1)甲:观察到小木片燃烧,小石片不燃烧,说明燃烧需要 。
(2)乙:b试管中观察到的实验现象为产生大量气泡和 。通过a和b试管中的现象对比,可知二氧化锰在过氧化氢的分解中作 剂。
(3)丙:对比c和d试管中的现象,可知金属活泼性较强的是 (填元素符号)。
化学实验是学习化学的重要方法,实验室常用的部分实验装置如图所示,请回答下列问题:
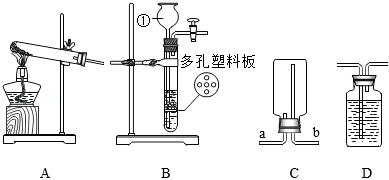
(1)装置B中仪器①的名称是 。
(2)用大理石和稀盐酸制取 的化学反应方程式为: ,应选择的发生装置为 (填字母)。
(3)若用装置C收集 ,气体应从 端进入(选填“a”或“b”)。
根据如图实验装置,回答问题:
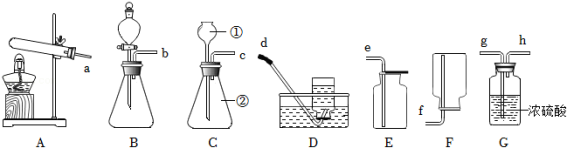
(1)C装置中标有①的仪器名称为 。
(2)实验室某小组同学用过氧化氢溶液和二氧化锰制取氧气,请写出化学方程式 ;根据该反应原理,从控制反应速率的角度考虑,请从如图中选择发生装置和收集装置制取一瓶干燥的氧气,所选装置接口字母连接顺序为 (连接顺序全对才得分)。
如图是中学化学实验中常用的一些装置,请回答下列问题:
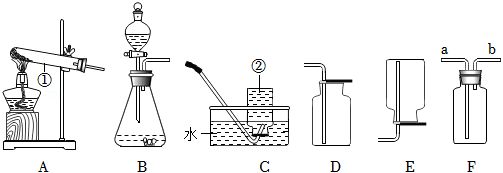
(1)写出标注仪器的名称:① ,② 。
(2)实验室用双氧水和二氧化锰制取氧气时应选用 (填字母序号,下同)作发生装置,反应的化学方程式为 ;若要收集较为纯净的氧气最好选用 装置。
(3)①实验室用B装置制取 时,装入块状石灰石的操作方法是 ;
②收集 不选用C装置的理由是 。
(4)通常情况下氯气是一种黄绿色有刺激性气味的气体,密度比空气大。实验室用固体高锰酸钾和浓盐酸反应制取氯气,若用F装置收集氯气,则气体应从图中的 (选填a或b)端进入,收集到的氯气中含有的杂质气体是 。
化学是一门以实验为基础的学科。根据如图装置回答问题:
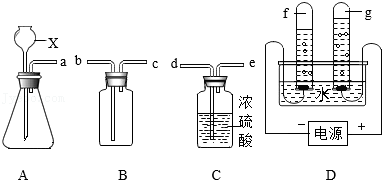
(1)仪器X的名称是 。
(2)实验室用A装置可以制备 气体,反应的化学方程式为 。要除去制得的 气体中混有的杂质,可用饱和 溶液洗气,发生反应的化学方程式为 。
(3)实验室用A、B装置组合制取 。A装置中发生反应的化学方程式为 ,在该反应中 的质量和 在反应前后保持不变。若要对B装置收集的 验满,带火星的木条应置于 端(填“b”或“c”)。
(4)实验室要制取干燥的H2,装置接口的连接顺序为a→ → → 。电解水也可制得H2,装置如图D,收集到氢气的试管是 (填“f”或“g”)。
农场需用熟石灰改良酸性土壤,为了确保改良效果,需要对库存的熟石灰是否变质进行检测。农场实验室取了一定量的熟石灰样品,对其成分进行如下探究。
【提出问题】熟石灰样品的成分是什么?
【作出猜想】猜想一:
猜想二: 和
猜想三:
【资料查阅】氢氧化钙微溶于水
【实验步骤与现象】
|
步骤 |
操作 |
现象 |
|
1 |
取1g样品于试管中,加入10mL蒸馏水充分振荡 |
得到上层清液和下层固体 |
|
2 |
向步骤1后的试管中滴加几滴酚酞 |
溶液变红 |
|
3 |
向步骤2后的试管中逐滴滴加稀盐酸 |
溶液由红色变为无色,固体物质消失并产生气泡 |
【实验分析】
(1)实验人员根据步骤1认为猜想三正确。其实该结论并不严密,请说明理由 。
(2)解释步骤3有气泡产生的原因(用化学方程式表示) 。
【实验结论】通过以上实验可以知道猜想 正确。
【评价与反思】熟石灰存放时应密封保存。农业上使用库存较久的熟石灰时要检测其成分。
化学兴趣班的同学准备分组进行气体的制取与性质的探究实验,实验员准备了如图仪器,同学们根据所学知识完成下列题目。

(1)请写出如图中对应字母编号为“e”的仪器名称 。
(2)甲小组的同学准备利用过氧化氢溶液制得较多量的氧气,同时便于添加液体试剂,应选择如图中的 (选填字母编号)来组成发生装置,生成氧气的化学方程式为 。
(3)乙小组的同学利用甲小组组装的发生装置制得了二氧化碳气体,并将气体从如图a端通入以探究二氧化碳的性质,其中1、4为湿润的石蕊棉球,2、3为干燥的石蕊棉球。同学们观察到2、3棉球不变色,1、4棉球变红且4棉球先变红,根据实验现象可得出二氧化碳的物理性质是 ,二氧化碳的化学性质是(用化学方程式表示) 。

某课外化学兴趣小组到华蓥山石林研学旅行,震惊于溶洞内千姿百态的石笋、钟乳石。回校后查阅教材,知道溶洞都分布在石灰岩组成的山洞中。石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙,其反应方程式为: 。当溶有碳酸氢钙的水遇热或压强突然变小时,溶解在水里的碳酸氢钙就会分解,重新生成碳酸钙沉积下来。
【提出问题】兴趣小组在研究溶洞成因后提出:
在碳酸钠溶液中通入二氧化碳气体也会发生类似的反应吗?
推测反应方程式为:
【猜想与假设】同学们做出了如下猜想:
猜想一:碳酸钠、二氧化碳和水会发生反应。
猜想二: 。
【查阅资料】①碳酸氢钠受热会分解产生碳酸钠、水和二氧化碳;
②碳酸钠与碳酸氢钠相互不反应。
【实验方案设计】
第一步:制备检测样品。向盛有 溶液的烧杯中通入一定量的二氧化碳后,通过系列的操作制得了固体,并干燥固体待用。
第二步:将第一步制得的固体加热,以检验固体中是否有碳酸氢钠。

实验装置如图一所示,在加药品前应先检查装置 。
完成上述操作后,将固体样品放入试管并加热。
【证据和推理】一段时间后,观察到烧杯内澄清石灰水变浑浊,这说明猜想 成立。请写出澄清石灰水变浑浊的化学方程式 。
【实验反思】同学们实验后讨论认为此实验设计不严密,使澄清石灰水变浑浊的二氧化碳或许来自碳酸钠分解。于是补充设计了图二的实验装置进行探究。
同学们在大试管里放碳酸钠(直接受热),小试管里放碳酸氢钠(间接受热)。一段时间后,出现 (选填下列选项中编号)的现象,则证明碳酸氢钠受热分解,碳酸钠受热不分解。由此推出图一装置产生的二氧化碳来自于碳酸氢钠的分解。
| A. |
烧杯A中澄清石灰水变浑浊,烧杯B中澄清石灰水不变浑浊 |
| B. |
烧杯A中澄清石灰水不变浑浊,烧杯B中澄清石灰水变浑浊 |
| C. |
烧杯A和烧杯B中澄清石灰水均变浑浊 |
| D. |
烧杯A和烧杯B中澄清石灰水均不变浑浊 |
【探究结论】碳酸钠、二氧化碳和水会发生反应。
二氧化碳是温室气体之一,“节能减排”“碳达峰”“碳中和”等关键词成为热搜。
(1)某化学兴趣小组设计实验验证二氧化碳温室效应。如图一所示,他们选用体积大小相等的两个塑料瓶,分别盛满同条件下的空气、二氧化碳与空气的混合物(体积比 ),并用一个小塑料管连接(在塑料管中间有一滴红墨水),置于阳光下。一段时间后红墨水滴会 移动。(选填“向右”“向左”或“不”)

(2)实验室用大理石与稀盐酸反应制备二氧化碳气体,其气体发生装置应选用图二中的 (填序号),收集二氧化碳气体时,验满的方法是 。
(3)若实验室选用A装置制备氧气,其反应的化学方程式为 。
(4)氨气通常情况下是无色、有刺激性气味、极易溶于水、密度比空气小的气体。若用如图二中D装置收集氨气,进气口应是 。(选填“a”或“b”)
化学是以实验为基础的学科。回答下列问题。
Ⅰ、如图是实验室制取气体可能用到的仪器。

(1)图中仪器D的名称是 。
(2)实验室制取氧气的化学反应方程式为 ,根据此反应选择图中仪器 (填仪器下对应字母)与H组合制取并收集氧气。
(3)用H装置收集(2)中制得的 ,则 应从 (填“a”或“b”)端通入。
Ⅱ、探究一瓶失去标签的白色固体的组成。
有一瓶失去标签的白色固体可能为 、 和 中的一种或多种,小明同学设计以下实验探究其组成。
取少量白色固体于两支试管A、B中,加蒸馏水使其溶解,向A试管中加入足量 溶液,溶液中有白色沉淀生成,再加入足量稀盐酸,沉淀全部消失,同时有气体生成;向B试管中加入足量 溶液,有白色沉淀生成,再加入足量稀 溶液,沉淀部分溶解,并有气体生成。
(4)由此证明这瓶白色固体的成分是 (填化学式),向A试管加入足量 溶液发生反应的化学方程式为 。
劳动实践课上同学们用草木灰给农作物施肥。课后同学查阅资料,得知草木灰是一种重要的农家肥,碳酸钾含量高。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
Ⅰ.常见草木灰钾含量(以碳酸钾表示)如下表:
|
草木灰种类 |
小灌木灰 |
稻草灰 |
小麦秆灰 |
棉壳灰 |
棉秆灰 |
向日葵秆灰 |
|
K2CO3(%) |
8.66 |
2.63 |
20.26 |
32.28 |
16.44 |
51.97 |
Ⅱ.提取碳酸钾主要过程是:秸秆→草木灰→滤液→固体
(1)表格中钾含量最高的草木灰是 ,同学们选用这种秸秆灰提取碳酸钾。
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。

(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是 。
(3)根据图2,搅拌器转速控制在每分钟 转,浸取时间为 分钟,比较适宜。
实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。

(4)实验中需缓慢滴入稀硫酸,原因是 。
(5)装置B的作用是 。
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为 %,与表格中数据相比明显偏低,原因可能是 (填序号)。
a.烧杯中溶液与空气接触
b.固体含有其它钾盐
c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有 (写一条)。
某兴趣小组利用图一装置探究 浓度、温度等条件对物质燃烧的影响,进行了以下操作。
浓度、温度等条件对物质燃烧的影响,进行了以下操作。
①点燃蜡烛后伸入广口瓶,立即塞紧橡皮塞,观察到蜡烛在瓶内燃烧,白磷不燃烧。
②待蜡烛自动熄灭,装置冷却后,在 时,将滴管中的水全部滴入广口瓶,铝盒中的白磷开始燃烧。
时,将滴管中的水全部滴入广口瓶,铝盒中的白磷开始燃烧。

图二是广口瓶内 浓度随时间变化的图像。
浓度随时间变化的图像。
(1)图二中 时间内,曲线下降的原因是 。
时间内,曲线下降的原因是 。
(2)生石灰的作用是 。
(3)盛放在铝盒中的白磷燃烧,说明金属铝具有良好的 性。
(4)本实验能得出的结论是 (填序号)。
A.可燃物燃烧氧气必须充足
B.白磷燃烧结束后广口瓶内没有 存在
存在
C.蜡烛燃烧需要 的最低浓度高于白磷燃烧需要
的最低浓度高于白磷燃烧需要 的最低浓度
的最低浓度