在实验室,我们通常用块状大理石与稀盐酸反应来制取二氧化碳气体,供选用的装置如图所示:
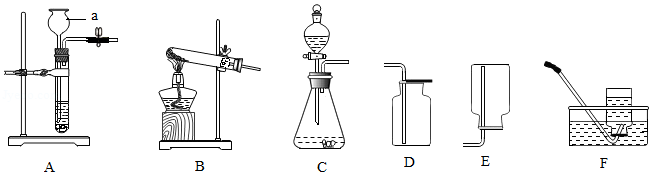
(1)写出仪器a的名称为 。
(2)若要制取并收集一瓶CO2,不可以选择的装置是 (填图中装置对应的字母)。
(3)CO2是一种酸性氧化物(能与碱起反应生成盐和水的氧化物)。为探究CO2确实能和NaOH发生化学反应,华雪同学选用了下列两种装置进行实验,都证明了CO2和NaOH确实发生了化学反应。请回答下列问题:

①选择装置I时,可观察到的实验现象为: 。
②选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原因是: 。
③CO2和NaOH溶液反应的化学方程式为 。
化学课堂上学生探究了如图所示的几个实验:
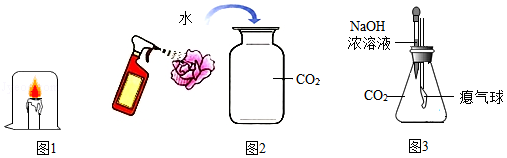
(1)图1实验中,蜡烛熄灭的原因是 。
(2)图2实验中,使紫色干花(用石蕊溶液浸泡过)变红的物质是 (填化学式)。
(3)图3实验中,滴入氢氧化钠浓溶液后,可观察到的实验现象是 ,发生反应的化学方程式是 。
实验室制取、收集、干燥气体的常用装置如图所示。请回答下列问题:
(1)实验室制取二氧化碳所选用的收集装置是 ,反应的化学方程式是 。
(2)若用高锰酸钾制取氧气,并用排水法收集,实验操作步骤如下:①点燃酒精灯并收集气体②熄灭酒精灯③加入药品并固定仪器④检查装置的气密性⑤从水槽中撤出导管。正确的操作顺序是 (填字母)。
A.③④①②⑤
B.④③①②⑤
C.④③①⑤②
D.①②③④⑤
(3)若要除去氧气中混有的水蒸气,气体应从F装置的 端进入。
根据如图所示实验回答问题。

(1) 中,仪器 的名称是_______; 分解的化学方程式为_____________________。
(2) 中,铁丝燃烧生成的黑色固体是_______。
(3) 中,电解水反应的化学方程式为______________;一段时间后,关闭电源,将带火星的木条放在 口处,打开活塞,观察到______________,说明有 生成。
在老师的指导下,化学兴趣小组利用下列装置进行了“可燃物燃烧的条件”的探究实验。

[实验目的]探究可燃物燃烧的条件
[实验步骤]
①将所需仪器按照装置图连接起来;
②打开K1和K2,向上拉动任意一支注射器的活塞;
③将实验所需药品加入对应的仪器中;
④将装有适量白磷的具支试管放入冷水中;
⑤打开K1,关闭K2,往装置甲中加入适量的双氧水,氧气进入具支试管中;
⑥关闭K1,打开K2,往装置乙中加入适量的盐酸,二氧化碳进入具支试管中;
⑦将装有适量白磷的具支试管放入80℃的热水中;
⑧打开K1,关闭K2,往装置甲中加入适量双氧水,氧气进入具支试管中;
⑨关闭K1,打开K2,往装置乙中加入适量的盐酸。
[问题解答]
(1)实验步骤②的目的是 。
(2)装置乙中发生反应的化学方程式是 。
(3)在实验步骤⑥中,具支试管中氧气已经排尽的实验现象是 。
(4)能看到白磷燃烧起来的实验步骤是 。
[实验结论]
可燃物燃烧必须同时满足两个条件:可燃物与氧气接触;温度达到可燃物的着火点。
(1)从图中选择合适的仪器,组装成制取氧气的发生装置,且能够随时添加药品,所选仪器应是 (填序号)。适用于这种装置制取氧气的化学方程式为 。

(2)生活中,有许多物品的使用与实验室中仪器的作用相似。请在图中选择作用相似的仪器,将其名称填入下表中对应的位置。
| 生活物品 |
物品的使用 |
作用相似的仪器名称 |
| 酒瓶 |
盛放白酒 |
|
| 洗脸盆 |
盛放清水 |
|
| 两根筷子 |
夹取盘中的青菜 |
|
| 一根筷子 |
水中放入白糖,搅拌 |
|
在某些食品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”(如图)。如果将小纸袋拿出来放在空气中,经过一段时间后,会发现纸袋内的白色固体颗粒黏在一起成为块状。同学们在老师的指导下,对纸袋内的物质进行了探究。

【提出问题】白色块状固体的成分是什么?
【猜想假设】同学们猜想该固体有 、 中的一种或两种。你认为还可能有 。
【实验验证】
|
序号 |
实验操作 |
实验现象 |
实验结论 |
|
实验1 |
取样品于试管中,加水溶解,用手触摸试管外壁。 |
试管外壁 ,试管底部有白色固体 |
样品中一定含有 |
|
实验2 |
将实验1中液体过滤,取少量滤液于试管中,向其中通入 气体。 |
滤液变浑浊 |
样品中一定含有 |
|
实验3 |
取少量实验2中的滤渣,加入足量的稀盐酸。 |
|
样品中含有你猜想的物质 |
【反思评价】同学们经过讨论,认为滤液中一定含有 ,样品中不一定含有 。理由用化学方程式表示为 。
【拓展应用】(1)若证明实验2滤液中 的存在,选用下列物质中的 (填字母)也可达到实验目的。
A.稀硝酸
B.酚酞溶液
C.碳酸钠溶液
(2)实验室中,易与空气中某些物质反应的药品更要 保存。
图1是实验室制取常见气体的装置,图2是探究铁生锈条件的实验装置,回答下列问题。
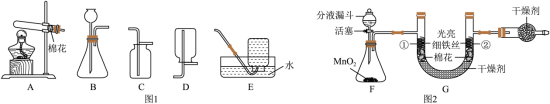
(1)用大理石和稀盐酸制取 的化学方程式为__________,发生装置是_____(填字母序号)。
(2)加热高锰酸钾制取 的化学方程式为__________,收集装置是_____(填字母序号),检验 的方法是_____。
(3)装置F中分液漏斗内的试剂是_____,打开活塞,缓慢滴加试剂,持续反应5分钟后,装置G中的现象是_____,达到实验目的。
(4)火星的大气中含有大量 ,科学家认为人类未来建设火星基地时,能利用火星大气中的 制取 ,理论依据是_____。
小明按如图所示进行趣味实验,将U形管开口端放入烧杯内,观察到溶液进入U形管并流入另一端。
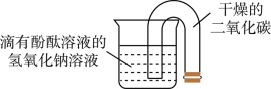
(1)烧杯内的溶液呈_____色。
(2)二氧化碳与氢氧化钠溶液反应的化学方程式为_____。
(3)U型管开口端放入烧杯后,管内气体压强_____(选填“增大”“不变”或“减小”),溶液在管内上升并流入另一端。
电解水制氢联合碳酸钙分解制备氧化钙,能减少碳排放,助力碳中和。该新方法的示意图如图所示。
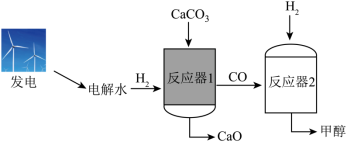
(1)传统方法: 在 以上完全分解生成 和__________(填化学式)。
(2)新方法:
i.电解水属于_____反应(填基本反应类型),反应前后氢元素的化合价_____(填“升高”“降低”或“不变”)。
ii.反应器1:一定的 环境及较低温度下 可与 反应生成 和 。 与 的分子个数比为_______。
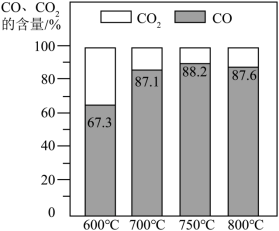
还可以直接分解。反应器1中 、 的含量随反应温度的变化如下图所示。________ 时,抑制 生成的效果最好。
iii.反应器2:一定条件下, 与 发生化合反应生成甲醇( ),化学方程式为_________ 。
(3)与传统方法相比,新方法的优点有__________________________(写两条)。
定律是对自然现象或关系的描述,通常可用数学方式加以表达。在学习“质量守恒定律”时,小丽查阅到以下材料:
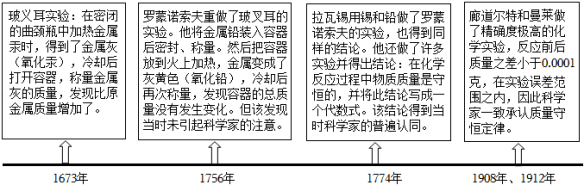
(1)玻义耳实验中,金属灰增加的质量是 ;
(2)质量守恒定律的发现过程,带给我们的启示有 (填字母);
A.要善于总结前人的成果和经验
B.实验的成功与否,取决于药品的选择
C.定量方法是科学研究的重要方法
受上述研究启发,小丽对相关实验进行了深入探究。
(3)在白磷燃烧前后质量测定实验中(如图),气球的作用有 ;

(4)小丽认为,蜡烛燃烧后剩下的固体质量比燃烧前少了,因此该现象不符合质量守恒定律。请你设计一个能说服小丽的简明实验思路 。
实验是科学探究的重要手段。如图是实验室制取气体的常用装置,请回答有关问题:

(1)仪器①的名称 。实验室利用高锰酸钾制取氧气的装置中,试管口略向下倾斜的原因是 。
(2)实验室里,在常温下用硫化亚铁固体和稀硫酸反应来制取硫化氢气体。通常情况下,硫化氢是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,密度比空气的大。实验室制取硫化氢气体应选用的发生装置是 (填序号),收集装置是 (填序号)。
如图是实验室常用气体制备装置,据图回答问题:
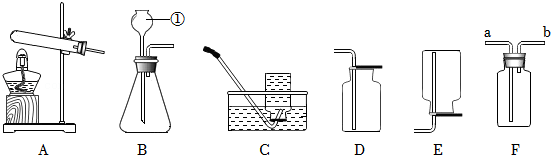
(1)图中仪器①的名称是 ;
(2)实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式是 ;
(3)实验室制取二氧化碳,可选用的收集装置是 ,若将产生的二氧化碳通入紫色石蕊溶液中,溶液变红色,其原因是 (写出化学方程式);
(4)实验室常用无水醋酸钠固体和碱石灰固体在加热条件下制取甲烷,应选用的发生装置是 ;若用 F 装置收集甲烷,则气体从导管口 进(填“a”或 b )。
有一瓶因久置而失去标签的无色溶液、为鉴定该溶液的成分,小亮进行了下面的实验:
(1)取一支洁净试管,倒入3~5mL待测溶液,滴加2~3滴石蕊试液,石蕊试液变红色,该溶液呈 (填“酸性”“碱性”);
(2)另取一支洁净试管,倒入3~5mL待测溶液,加入几粒锌粒后有气泡冒出,该溶液一定是 溶液;
(3)要确定该溶液是稀硫酸还是稀盐酸,小亮还需要补充的实验是:
实验步骤 |
现象 |
实验结论 |
|
|
|
根据下列装置,结合所学化学知识,回答下列问题。
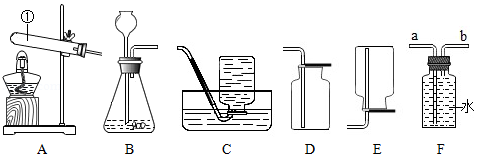
(1)仪器①的名称是 。
(2)若用氯酸钾和二氧化锰混合加热制备并收集干燥的氧气,你应选择 装置组合(填序号),该反应的化学方程式为 ;其中二氧化锰是该反应的 。
(3)某同学用石灰石与稀盐酸反应制取气体,他应该选择的发生装置为 (填序号),他想知道该气体是否是二氧化碳,正确的检验方法是 。
A.将该气体通入澄清石灰水观察是否变浑浊
B.将燃着的小木条放在导管口看是否熄灭
(4)某同学用F装置收集氢气。他应该将氢气的发生装置与F装置的 端相连(填"a"或"b"),请你分析能用F装置收集氢气的原因 。