化学兴趣小组的同学们在老师的带领下走进实验室,开展实验活动。
(1)实验室依次编号为1、2、3、4的药品柜中,分别存放常见的酸、碱、盐和酸碱指示剂。小刚欲使用熟石灰,他需从 号柜中取出。
(2)小刚发现盛放Na2CO3与NaCl两种溶液的试剂瓶标签脱落,为鉴别两种溶液,分别取样于试管中,加入无色酚酞溶液,若为Na2CO3,则观察到溶液变为 色。
(3)小文从柜中取出标有“10% NaOH溶液”的试剂瓶,取少量样品加入试管中,向其中滴入稀盐酸,发现产生气泡,判断该NaOH溶液中有Na2CO3,用化学方程式表示NaOH溶液变质的原因: 。
小文同学对变质的NaOH溶液进行如下一系列实验,实现药品再利用。
I.测定NaOH溶液中Na2CO3的质量分数
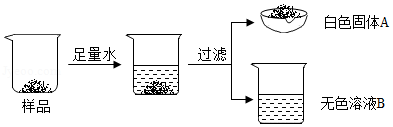
[实验操作]取40.0g 10%的NaOH溶液样品进行如图所示的实验。

[数据处理]
①所取用盐酸(溶质质量分数7.3%)的质量理论上不少于 g。
②如图中,反应前后天平示数相差1.1g,计算NaOH溶液中Na2CO3的质量分数(写出计算过程)。
Ⅱ.变质的NaOH溶液再利用
小文将剩余NaOH溶液倒入烧杯中,加入经计算所需的熟石灰粉末,充分搅拌、静置,过滤,得到NaOH溶液和滤渣。充分搅拌的主要目的是 。
(4)实验结束后,同学们将实验产生的废液和废渣倒入指定的烧杯中,得到无色溶液和白色沉淀,溶液中除一定存在的溶质外,可能存在的溶质是 。
同学们再次实验,确认成分后,对废液回收利用,绿色排放。
2019年春节起,常州大部分地区禁止燃放烟花爆竹,开启了龙城环保新时代。
(1)“禁止燃放烟花爆竹”的安全标志是 。

(2)禁止燃放烟花爆竹不仅可以减少噪声污染、火灾等,还以减少SO2和 等空气污染物的排放,提升空气质量。
(3)爆竹中常含有硫、硝酸钾和木炭的混合粉末,点燃后生成硫化钾(K2S)、氮气和二氧化碳,该反应的化学方程式为 。含硫燃料燃烧产生的SO2会形成 型酸雨,酸雨的pH (填序号)。
A.小于5.6 B.等于7 C.大于7
某白色固体由BaSO4、BaCO3、Na2CO3、Ba(OH)2中的三种物质组成。为确定其成分,某同学设计并完成如下实验,请把表格中的内容补充完整。(已知:BaSO4不溶于稀盐酸)
序号 |
Ⅰ |
Ⅱ |
Ⅲ |
操作 |
|
|
|
现象 |
有气泡产生,固体有剩余 |
有气泡产生 |
产生白色沉淀,溶液最终显 色 |
结论或解释 |
原白色固体中含有
|
原白色固体中含有Na2CO3:生成气体的化学方程式为
|
原白色固体中含有BaCO3. |
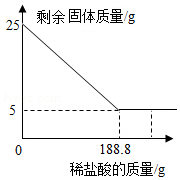
实验室常用大理石和稀盐酸制取二氧化碳。现取25g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图。求:
(1)25g大理石中碳酸钙的质量。
(2)恰好完全反应时所得溶液中溶质的质量分数。
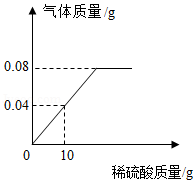
向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据该图信息计算:
(1)铁粉反应完时,产生氢气的质量为 g。
(2)原稀硫酸中溶质的质量分数(写出计算过程)。
文文想通过实验测定稀盐酸的溶质质量分数,他分四次向182.5g稀盐酸中加入含有杂质的锌粉(杂质不溶于盐酸也不与盐酸发生反应),记录所加锌粉质量与产生氢气的质量如下表所示:
次数 |
1 |
2 |
3 |
4 |
锌粉质量/g |
5 |
5 |
5 |
5 |
氢气质量/g |
0.15 |
0.15 |
0.1 |
0 |
请帮文文计算稀盐酸的溶质质量分数。
有镁和氯化镁固体混合物,取一定量的该混合物放入烧杯中,然后取稀盐酸200g,平均分五次加入其中,充分振荡,实验所得数据如下表:
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
加入稀盐酸的质量/g |
40 |
40 |
40 |
40 |
40 |
生成气体的总质量/g |
0.16 |
m |
0.48 |
0.5 |
0.5 |
(1)表中m的值为 。
(2)所用稀盐酸的溶质质量分数为多少?
实验室有一瓶含杂质的氯酸钾。某兴趣小组利用该药品和二氧化锰制取氧气(杂质不参加反应)。实验数据记录如图:

请回答下列问题:
(1)a= 。
(2)计算受热分解的氯酸钾的质量(精确到0.1g)。
现有一种稀盐酸和氯化铝的混合溶液,取100g该溶液于烧杯中,向其中逐滴加入氢氧化钾溶液,至氯化铝正好完全转化为沉淀,停止滴加氢氧化钾溶液,经测定,生成沉淀的质量为7.8g。请回答:
(1)据观察,产生沉淀前,消耗了一定量的氢氧化钾溶液,请写出该反应的化学方程式 。
(2)100g混合溶液中氯化铝的质量分数是多少?(写出计算过程,计算结果精确到小数点后两位。产生沉淀的化学方程式:AlCl3+3KOH=Al(OH)3↓+3KC1)
科学探究是学习化学重要而有效的学习方法。某校化学兴趣小组的同学做实验,向盛有少量NaOH溶液的试管中通入CO2,未看到明显的实验现象。同学们对NaOH与CO2能否反应进行验证,并对废液的成分进行探究。
活动一
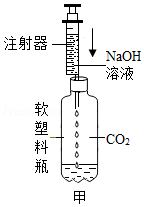
同学们经过讨论,设计了甲装置并进行实验,请你把实验现象补充完整。
实验步骤 |
实验现象 |
猜测 |
如图甲,向集满二氧化碳的软塑料瓶中滴加足量的氢氧化钠溶液,振荡 |
|
①CO2溶于NaOH溶液中 ②CO2与NaOH反应 |
活动二
兴趣小组的同学对猜测②进行如下探究实验
(1)取软塑料瓶中的液体于三支试管中,三位同学分别完成如图所示实验。
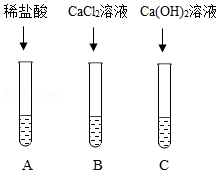
(2)同学们观察到A试管中有气泡冒出,B、C试管中均有白色沉淀生成。请你写出A试管中生成气体的化学反应方程式 。
(3)以上三个实验均能证明CO2与NaOH发生了反应。请写出甲装置中发生反应的化学方程式 。
活动三
实验结束后,同学们将三支试管中反应后的剩余物倒入一个洁净的大烧杯中(如图),充分搅拌、静置,观察到烧杯内上层是无色溶液,下层有白色沉淀。请你分析烧杯上层溶液中一定不含有的离子是 (填离子符号)。小组同学对烧杯内上层溶液中可能含有的离子进行如下探究。
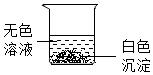
[提出问题]烧杯内上层溶液中可能含有哪些离子?
[猜想与假设]上层溶液中可能含有OH﹣、CO32﹣、Ca2+中的一种或几种。
[进行实验]
实验步骤 |
实验现象 |
实验结论 |
①取烧杯内无色溶液少许于试管中,滴加 滴加过量的氯化钙溶液 ,静置 |
有白色沉淀生成 |
有CO32﹣、无Ca2+ |
②取①中反应后的上层清液少许于试管中,滴加 硫酸铜溶液 (指示剂除外) |
蓝色沉淀生成 |
有OH﹣ |
[反思评价]
(1)经过综合分析,最终确定烧杯内上层溶液中一定存在的离子有 (填离子符号)。
(2)将烧杯内的物质过滤,滤渣回收,向滤液中加入适量的 (填名称)进行处理后再排放,可以有效防止水体污染。
将20.0g铜锌合金置于烧杯中,向其中逐渐加入稀硫酸。当加入148.4g稀硫酸时,不再有气体生成,此时测得烧杯中混合物的质量为168.0g。
(1)反应中生成气体的质量是 g;
(2)求反应后烧杯溶液中溶质的质量分数。(写出计算过程)
现有一种稀盐酸和氯化铝的混合溶液,取100g该溶液于烧杯中,向其中逐滴加入氢氧化钾溶液,至氯化铝正好完全转化为沉淀,停止滴加氢氧化钾溶液,经测定,生成沉淀的质量为7.8g。请回答:
(1)据观察,产生沉淀前,消耗了一定量的氢氧化钾溶液,请写出该反应的化学方程式 。
(2)100g混合溶液中氯化铝的质量分数是多少?(写出计算过程,计算结果精确到小数点后两位。产生沉淀的化学方程式:AlCl 3+3KOH=Al(OH) 3↓+3KC1
现有一种稀盐酸和氯化铝的混合溶液,取100g该溶液于烧杯中,向其中逐滴加入氢氧化钾溶液,至氯化铝正好完全转化为沉淀,停止滴加氢氧化钾溶液,经测定,生成沉淀的质量为7.8g。请回答:
(1)据观察,产生沉淀前,消耗了一定量的氢氧化钾溶液,请写出该反应的化学方程式 。
(2)100g混合溶液中氯化铝的质量分数是多少?(写出计算过程,计算结果精确到小数点后两位。