为测定某实验废液中硫酸铜和硫酸的质量分数,分别在三只烧杯中倒入50g废液,并在烧杯中依次加入一定量的铁粉。实验结束后,测得的数据见如表:
|
第一组 |
第二组 |
第三组 |
|
|
反应前加入铁粉质量/g |
5.6 |
8.4 |
11.2 |
|
反应后剩余固体的质量/g |
3.2 |
3.2 |
6.0 |
|
反应后质量( )损失/g |
0.1 |
0.2 |
0.2 |
请回答:
(1)对比第一、二组数据,第一组实验结束后,废液中的 (填化学式)已全部参加反应;
(2)通过分析第二、三组数据,50g废液与铁粉反应生成氢气质量最多为 ;
(3)经计算,50g废液中所含硫酸的质量为 ,硫酸铜的质量分数为
为测定某石灰石矿中碳酸钙的含量,现称取12.5g石灰石矿样品与足量的稀盐酸反应(杂质不溶于水,也不参与反应),得到二氧化碳气体4.4g(假设生成的气体全部逸出)。请计算:该石灰石样品含CaCO3的质量分数?
在氢气还原氧化铜实验后的固体中含有 和 ,为了测定固体中 的含量,取3.0g固体样品,逐滴加入稀硫酸,剩余固体质量与稀硫酸的质量关系如图所示。
已知:
(1)固体样品中 的质量为 g。
(2)固体样品与稀硫酸恰好完全反应时所得溶液的溶质质量分数为多少?(写出计算过程)

请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),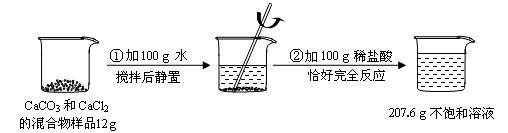
回答下列问题:计算原混合物样品中CaCl2的质量(写出计算过程)。
根据《羊城晚报》报道:今年8月,有十几个民工饮用散装酒后双目失明,继而死亡。据调查,散装酒中含有超标的有毒物质甲醇,其化学式为:CHXO,求:
(1)已知甲醇的相对分子质量为32,则X为 ;
(2)甲醇完全燃烧时,生成二氧化碳和水,发生如下反应:2CHXO + 3O2 CO2+4H2O
CO2+4H2O
则生成二氧化碳和水的质量比为 。
(3)如果甲醇在氧气中不完全燃烧可发生如下反应:8CHXO + nO2 mCO2+2CO+16H2O
mCO2+2CO+16H2O
若反应生成3.6g水,请计算:
①m值是 ;
②参加反应的氧气质量是多少克?(写出规范步骤并计算)
【2015年辽宁省丹东市】取锌、铜的混合物8g与154.7g稀硫酸恰好完全反应,称得剩余物质的总质量为162.5g。请计算:
(1)产生氢气的质量是多少?
(2)反应后所得溶液中溶质的质量分数是多少?
【2015年甘肃省武威市、白银市、定西市、酒泉市、临夏州】某补钙剂说明书的部分信息如右下图所示。现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g。

(1)青少年缺钙出现的疾病是 。
(2)该品牌补钙剂每片含的CaCO3质量为多少?
(3)该盐酸中溶质的质量分数是多少?(精确到0.1%)。
一个碳12原子的质量为akg,若某原子的相对质量为M 则该原子的实际质量为多少?若该原子的核外有m个电子,则其核内有多少个中子?
乙醇( )俗称酒精,可通过高粱、玉米和薯类等发酵、蒸馏而得到,属于可再生能源。
(1)乙醇中碳、氢元素的原子个数比是 。
(2)乙醇中碳元素的质量分数是 (计算结果精确到0.1%)。
在抗击新型冠状病毒肺炎疫情中,过氧乙酸(化学式为C 2H 4O 3)是一种常用的消毒剂。试计算:
(1)过氧乙酸中C、H、O三种元素的质量比为 。
(2)过氧乙酸中碳元素的质量分数是 (精确到0.1%)。
称取5.8g某生铁样品放入94.6g稀盐酸中,恰好完全反应(生铁样品中的杂质不溶于水也不与盐酸发生反应),产生0.2g氢气.试计算反应后所得溶液中溶质的质量分数.
我国科学家屠呦呦因为发现青蒿素(化学式为C15H22O5),一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获2015年诺贝尔生理学或医学奖。
(1)青素的蒿相对分子质量为________________;
(2)青蒿素中各原子的原子个数比C:H:O=_____________;
(3)青蒿素中碳、氢两种元素的质量比为_________________;
(4)青蒿素中氧元素的质量分数为_____________(计算结果保留一位小数);
(5)在1972年发现青蒿素前治疗疟疾的药物主要是金鸡纳霜,又叫奎宁(化学式为C20H24N2O2,相对分子质量为324),求141g青蒿素中所含氧元素的质量与多少克金鸡纳霜中所含氧元素质量相等?(写出计算过程)
硝酸铵(NH4NO3)是我们常用的氮肥,现在请你根据化肥硝酸铵(NH4NO3)的化学式求:
(1)NH4NO3的相对分子质量;
(2)NH4NO3中氮、氢、氧元素的质量比;
(3)NH4NO3中氮元素的质量分数(保留一位小数)。
实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示。已知:BaCl2+Na2CO3=BaCO3↓+2NaCl 请计算:
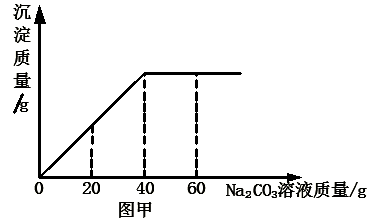
(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体 g。
(2)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)