铝作为食品污染源之一,广泛存在于各种膨化食品中,成人每日摄入量应控制在4mg以下。炸油条时需加入明矾晶体作为膨松剂。已知明矾晶体的化学式为KAl(SO4)2·12H2O,相对分子质量为474。在1kg炸成的油条中,含有明矾晶体2g,试通过计算说明成人每日食用100g油条,铝元素是否超过安全摄入量?
为了消除人体碘缺乏病,我国政府规定食用盐必须是加碘食盐。所谓碘盐就是在食盐中加入一定量的碘酸钾(KIO3)。计算:(1)计算碘酸钾(KIO3)的相对分子质量。(2)碘酸钾中碘元素的质量分数。(精确到0.1﹪) (3)若成人每天食用6克食盐,从中摄取0.15毫克碘,那么1千克碘盐中含碘多少毫克?
下图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:
为了测定此食盐中的钙元素含量,取10g这种食盐溶于水,加入足量的稀盐酸,生成0.132g二氧化碳,请计算此加钙食盐中钙元素的质量分数是否达标。(注:成分中只有碳酸钙与盐酸反应)
某同学发现他家菜园中蔬菜生长迟缓,便施用了一种氮肥(一种化肥),下图是氮肥包装标签的部分文字。求:
(1)硝酸铵的相对分子质量是多少?
(2)硝酸铵中各元素的质量比是多少?
(3)硝酸铵中氮元素的质量分数是多少
氮是农作物生长需要的营养元素,尿素是其中的一种,其化学式为CO(NH2)2, 请计算:
(1)尿素的相对分子质量是 ;其中氢和氧元素质量比为 _____________。
(2)张明家的水稻田需要56千克的氮,请你计算,他至少购买尿素[CO(NH2)2 ]多少千克?
2013年5月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚。将30克邻叔丁基苯酚完全燃烧,生成88克
和25.2克
(无其他产物)。已知邻叔丁基苯酚的相对分子质量为150,求:
(1)30克邻叔丁基苯酚中含碳元素克,氢元素克。
(2)邻叔丁基苯酚的化学式为。
下图是某钙片的说明书,请阅读解答下列问题。
| X X 钙片 主要成分:葡萄糖酸钙C6H11O72Ca 药品规格:2.5g每片含C6H11O72Ca 0.2g 用 量:每日2次,每次一片 |
①葡萄糖酸钙中含有种元素。
②葡萄糖酸钙中碳与钙的质量比是;
③按说明书服用此钙片,每天补充钙的为:。(只写算式,不算结果)。
友情告知:
的相对分子质量为430
(2)现有废硫酸
。废硫酸中
的质量分数为20%与足量的废铁屑反应,可生产
的质量是多少?
最近媒体报道油炸含有淀粉的食品会产生有毒的丙烯酰胺【化学式为C3H5NO】,食用后有害健康。试计算(要求写出计算过程,注意解题格式!):
(1)丙烯酰胺的相对分子质量是多少?
(2)丙烯酰胺中各元素的质量比m(C) :m(H) :m(N):m(O)是多少?
(3)丙烯酰胺中碳元素的质量分数是多少(计算结果精确至0.1%)?
某同学用下图装置做炼铁的原理实验。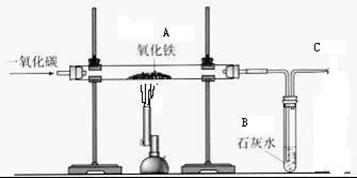
反应之前应先 _________ 后加热,A处的现象是_________________;该同学取氧化铁样品10克(杂质不反应),按正确的步骤完全反应后测量反应管中固体剩余物为7.6克。则样品中氧化铁的质量分数是多少?(写出计算过程)
敏敏同学为探究石灰石中碳酸钙的质量分数(杂质不与稀盐酸反应),向6.0g石灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体的体积为1.11L(该条件下二氧化碳的密度为1.977g/L)
(1)该反应生成二氧化碳的质量为多少克(精确到0.1g)
(2)该石灰石样品中碳酸钙的质量分数为多少?(精确到0.1%)
已知可作为相对原子质量标准的一个碳原子的质量为1.993×10-26 kg,铁的相对原子质量为56,现有重1 g的铁钉,其中含有的铁原子个数大约是多少?
把5g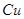 、
、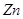 混合物加入到盛有50g稀硫酸的烧杯中,恰好完全反应,反应后烧杯内物质的总质量为54.8g,求
混合物加入到盛有50g稀硫酸的烧杯中,恰好完全反应,反应后烧杯内物质的总质量为54.8g,求
(1)加入稀硫酸的过程中会看到什么现象_________________________
(2)产生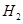 g?
g?
(3)最后所得溶液中溶质的质量为多少?
在20℃时,向质量均为50g的5份水中分别加入一定质量的氯化钾固体,然后搅拌至完全溶解得到溶液。加入氯化钾的质量与所得溶液的质量如下表:
| 实验编号 |
① |
② |
③ |
④ |
⑤ |
| 加入氯化钾的质量/g |
5 |
10 |
15 |
20 |
25 |
| 溶液的质量/g |
55 |
60 |
65 |
67 |
67 |
(1)③中所得溶液是氯化钾的 溶液;(填“饱和”或“不饱和”)
(2)20℃时,50g水中最多能溶解 g氯化钾;
(3)请认真分析上表数据,计算20℃时氯化钾饱和溶液中溶质的质量分数。(要求写出完整的计算过程,结果精确到小数点后一位)