某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2.
小明说:不可能含有N2,因为_________________.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO______________.
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
将气体通入澄清的石灰水中 |
澄清石灰水变浑浊 |
| ② |
将带火星的木条伸入该气体中 |
带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________,写出该反应的文字表达式为______________.
(2)由实验②_____________(填“能”或“不能”)确定该气体中不含氧气,理由是_________________________.
已知甲、乙、丙为三种不同的单质,A、B、C为三种不同的氧化物。其中A为黑色粉末,B为主要的温室气体,乙为使用最广泛的金属。请回答:
(1)B的化学式是 ;
(2)乙→甲的化学方程式为_______________________________。
下图是利用缺铁性氧化物
进行
再资源化研究的示意图。下列说法正确的是( )

| A. | 如该研究成熟并广泛应用,能缓解温室效应 |
| B. | 反应①为置换反应,反应②为分解反应 |
| C. | 反应①提高了铁的氧化物中铁的质量分数 |
| D. | 整个转化反应的化学方程式可表示为: |
右图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明 密度大于空气且能与水反应的现象是( )
密度大于空气且能与水反应的现象是( )

| A.①变红,③不变红 | B.④变红,③不变红 |
| C.①、④变红,②、③不变红 | D.④比①先变红,②、③不变红 |
甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图。下列叙述中正确的是 
| A.乙图炼铁中原料焦炭的作用是只提供热量 |
B.炼铁的主要原理是:3CO+ Fe2O3 2Fe + 3CO2 2Fe + 3CO2 |
| C.甲图中实验开始时应先点燃加热氧化铁的酒精喷灯,再点燃酒精灯 |
| D.两图中得到的铁是完全相同的 |
某同学为研究相同条件下一氧化碳和氢气哪个还原氧化铁的量更多,将一氧化碳和氢气等体积混合后先通过图甲装置,再通过图乙中的仪器组合。为达到实验目的,图乙中仪器选择和连接最好的是
| A.cba | B.cda | C.cbd | D.bca |
常温下
、
、
、
是四种常见的无色气体,它们之间转化关系如图所示(图中反应条件已省略,X在常温下为无色液体),请回答以下问题:
(1)写出下列物质的化学式
;
;
;
;
(2)
与
反应的化学方程式;该反应属于(填"放热"或"吸热")反应.

以下是实验室常用的部分仪器。

① ② ③ ④ ⑤ ⑥ ⑦ ⑧
(1)仪器③的名称是 ;
(2)用过氧化氢溶液和二氧化锰混合物制氧气时,选用的发生装置是 ,反应的化学方程式为 。要收集0.64g氧气,需要H2O2的质量是 g
(3)同学们用浓盐酸和块状石灰石反应制取二氧化碳,并将得到的气体通入澄清石灰水中,始终没有发现澄清石灰水变浑浊。小英认为澄清石灰水已经变质;小青认为得到的CO2中混有 气体。他们为了证明自己的猜想进行了如下实验:
①小英将气体通入到新制的澄清石灰水中,但仍未发现澄清的石灰水变浑浊;
②小青取 与块状石灰石反应制取的CO2,并将产生的气体通入原澄清石灰水中,变浑浊,请写出石灰水变浑浊的化学方程式 。
(4)乙炔是一种无色、无味、难溶水的气体,密度和空气接近,收集乙炔气体可选用的装置是 。
水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实险的基础上得出的。
(1)实验室中常用锌粒和稀硫酸反应来制备氢气。请从图1装置中选择并组装一套制取干燥氢气的装置,正确的连接顺序为 (用接口处字母填写)。

(2)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要 。
②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是 。在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为 L。
(3)科学家们又用“电解法”证明了水的组成(装置如图2所示,电极不与水及生成的气体反应)。电解时,水中需加入少量的NaOH,其作用是 。 通电一段时间后,发现甲、乙两量筒中收集的气体体积比略小于1:2,其原因可能是 (写出一条即可)。
(4)拉瓦锡还用另一实验证明了水的组成。
他让水蒸气通过一根烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(磁铁矿的主要成分)生成。该反应的化学方程式为 。
(5)用“氢气还原氧化铜”实验也可以证明水的组成(图3)。装置A中的玻璃管和其中物质在反应前后的质量差为m1,装置B和其中物质在反应前后的质量差为m2,据此可计算出水中O、H元素的质量比为 (用含 m1、m2的代数式表示)。实验时该比值往往略小于8:1,原因可能是 (写出一条即可)。
(6)碘与锌在常温下反应速度很慢,若滴入几滴水则反应剧烈,水在此的作用是 。
同学们对实验“煅烧石灰石”展开了探究。资料:石灰石中的杂质高温不分解且不与稀盐酸反应

①为证明石灰石已分解,三位同学设计方案如下:
I.甲同学按图一所示进行实验(煤气灯能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 (1) 。
II.乙同学按图二所示进行实验,观察到B中液体变 (2) 色,A实验的作用 (3) 。
III.丙同学取一定质量的石灰石煅烧,一段时间后发现固体质量减轻,证明石灰石已分解。
你认为哪位同学的方案不合理?并写出理由 (4) 。
②为证明石灰石是否完全分解?丁同学对丙同学煅烧后的固体又进行了如下探究
| 实验步骤 |
实验现象 |
结 论 |
| (5) |
有气泡产生 |
石灰石未完全分解 |
某学习小组准备探究气体的测定和数据处理方法。
【提出问题】利用碳酸钙与稀盐酸反应来测定生成CO2的量。
【实验设计】通过下列两个实验分别测定CO2的质量和体积。

实验一 实验二
【分析处理】
实验一:
① 将小烧杯中的稀盐酸分几次加入到大烧杯中,并不断搅拌,判断反应后盐酸过量的依据是 。
② 若稀盐酸足量,计算理论上能产生二氧化碳的物质的量 。(根据化学方程式进行计算)
实验二:
③ 先连接好装置,再 (填操作),然后装好药品,最后将20mL稀盐酸快速推入锥形瓶中。若缓慢推入,则可能造成的后果是 。
④ 实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
| 注射器读数/mL |
60.0 |
85.0 |
88.0 |
89.0 |
89.5 |
89.8 |
89.9 |
90.0 |
90.0 |
90.0 |
根据以上实验过程和数据综合分析,最终生成CO2的体积是 mL。
【反思与评价】
⑤ 经过分析,下列说法错误的是 。
A.实验一的操作简单,便于读数
B.实验一最终得到的数据和通过计算得出的理论值完全相等
C.实验二在密闭体系内反应,更环保
D.实验二中若将碳酸钙粉末改成块状的大理石,更安全
草酸钙(化学式为CaC2O4,相对分子质量为128)是一种难溶于水的白色固体,受热能分解。小红同学为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量随时间变化如下图所示。请回答下列问题:

(1)t1~t2时问段内固体质量减少的原因是产生了一种极易与血红蛋白结合的有毒气体,该气体的化学式为 ;同时生成一种白色固体,它与大理石的主要成分相同,则该段时间内反应的化学方程式为 。
(2)t2~t3时间段内固体质量不变的原因是 。
(3)t3~t4时间段内反应的化学方程式为 。
(4)小强和小明另取12. 8g草酸钙固体加热一段时间后,对剩余固体的成分进行探究。
【查阅资料】CaC2O4能与稀盐酸反应,其反应的化学方程式为:CaC2O4+2HCl=CaCl2+H2C2O4;草酸(H2C2O4) 是一种可溶于水的酸;澄清的石灰水能使紫色石蕊变蓝。
【设计方案并实验】
| 同学 |
实验操作 |
实验现象 |
结论 |
| 小强 |
取少量固体放入烧杯中,加适量水并搅拌。静置后,取上层清液于试管中,滴加紫色石蕊溶液 |
溶液变蓝色 |
剩余固体中一定含有 。 一定不含有 。 可能含有 。 |
| 小明 |
另取少量固体放入试管中,加足量稀盐酸 |
有气体产生 |
剩余固体中一定含有 。 |
【交流与讨论】三位同学经交流后认为,该剩余固体与图中 时间段的物质成分相同。
如图所示,A瓶盛有澄清的石灰水,B瓶盛有紫色石蕊试液,C杯有高低不同的燃着的蜡烛。回答下列问题:
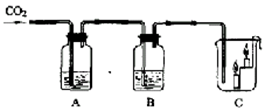
(1)A处澄清石灰水变浑浊了,写出这个过程发生的反应(用化学方程式表示)_____ ___
(2)B处紫色石蕊试液变红,这是因为( )
| A.二氧化碳使紫色石蕊变红 |
| B.水使紫色石蕊变红 |
| C.二氧化碳可使澄清石灰水变浑浊 |
| D.二氧化碳与水反应生成的碳酸使紫色石蕊变红 |
(3)C处出现的现象_____ ______;由此总结二氧化碳具有的性质:
①_____ _ _____;②_______ ____。