某化学兴趣小组利用如图装置进行氧气的制取和性质实验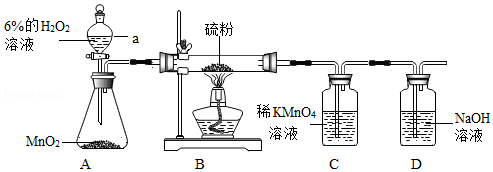
(1)仪器a的名称是 ;
(2)实验中,点燃酒精灯后,可观察到硫粉在氧气中燃烧呈现 色火焰;装置C中的现象是 ;
(3)装置D的作用是 (用化学方程式表示);
(4)为了证明装置C中出现的现象不是由氧气造成的,在不改变装置的情况下,操作方法是 ,并观察装置C中的现象;
(5)实验时加入6%的过氧化氢溶液51g,理论上可生成多少克氧气?(写出计算过程)
为了测定某纯碱样品中Na 2CO 3的质量分数。某化学兴趣小组的同学称取该纯碱样品11.0g,加入到足量的稀盐酸的烧杯中,充分反应后,称取烧杯内物质的总质量,发现比反应前物质的总质量减少了4.4g(纯碱样品中杂质不溶于水,不与酸反应)。求该纯碱样品中Na 2CO 3的质量分数(精确到0.1%)。
下列图象能正确反映对应变化关系的是

A.加热等质量的氯酸钾
B.通电分解水
C.向一定量的氢氧化钠溶液中逐渐加入稀盐酸
D.将一定量含有盐酸的氯化钙溶液中逐渐加入碳酸钾溶液,则图中物质R是 。
“湖北氢能源汽车研发生产取得重大突破”被评为2016年度湖北十大科技事件之一。其原理是将传统汽车改装为醇氢汽车,安装甲醇(CH4O)裂解器。据查甲醇与水蒸气在一定温度和催化剂作用下生成二氧化碳和氢气,1升甲醇可替代1升汽油,有利于减少雾霾。请完成下列问题:
(1)甲醇属于 (填“无机物”或“有机物”)。
(2)由甲醇制取氢气的化学方程式为 。
(3)64g甲醇完全反应可制得氢气 g。
为了测定某铜、锌合金的组成,称取10g该合金粉末,在粉末中连续6次加入稀硫酸反应,每加一次稀硫酸,记录完全反应后所得剩余固体的质量,实验数据如下:
| |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
第6次 |
| 加入稀硫酸的质量(g) |
10 |
10 |
10 |
10 |
10 |
10 |
| 剩余固体的质量(g)[ |
8.7 |
7.4 |
6.1 |
4.8 |
3.5 |
3.5 |
(注意:以下各题,只要求填写计算结果,不要求写计算过程)
(1)据表中数据,计算该合金中锌的质量为 ;
(2)计算所加稀硫酸的溶质的质量分数为 (精确到0.1%);
(3)计算恰好完全反应后所得溶液的溶质的质量分数为 (精确到0.1%)。
人类对材料的发现和使用经历了从石器、青铜器、铁器到铝的大规模使用等漫长的征程。请回答:
(1)我国最早使用的合金是 ;
(2)我国是最早采用湿法冶铜的国家。文献记载“胆铜法”:用铁与“胆水”(含CuSO4)反应获得铜。铁与硫酸铜溶液反应的化学方程式为 ;
(3)下列金属矿物中,可以用来炼铁的是 (填正确选项前的字母);
A.赤铜矿(Cu2O) B.赤铁矿(Fe2O3) C.软锰矿(MnO2)
(4)19世纪初,铝的发现得益于电解技术的应用。如图为用铝土矿炼制铝的生产流程。

现有含Al2O351%的铝土矿200t,经上述反应后可制得铝 t (假设上述各步反应中,铝元素一共损失10%.计算结果精确到小数点后一位)。
(1)自然界中吸收大气中CO2的环节是 .
(2)由于人类消耗化石燃料的增加和森林的乱砍滥伐,使空气中CO2的含量上升,从而导致温室效应增强,全球气候变暖.请写出一条因气候变暖给人类生存环境带来影响的情况: .
(3)科学家研究得到:海洋是吸收大量CO2的地方.如果工业生产产生的CO2排放量继续增加,海洋将被“酸化”.请写出酸化原因的化学方程式 。
(4)科学家目前正在研究将空气中过量的CO2和H2在催化剂和适量条件下转化成液态甲醇和水,反应的化学方程式:CO2+3H2 甲醇+H2O.则甲醇的化学式是 .
甲醇+H2O.则甲醇的化学式是 .
中国古代四大发明之一的"黑火药"是由木炭(C)、硫粉(S)和硝酸钾(KNO 3)按一定比例混合而成。
(1)分类。下列关于"黑火药"说法正确的是 。
a."黑火药"由"黑火药分子"构成
b."黑火药"中的KNO 3属于复合肥料
c."黑火药"中的C、S不再保持各自的化学性质
(2)变化。"黑火药"爆炸时发生的主要反应是:S+2KNO 3+3C═K 2S+N 2↑+3 ↑。
①依据质量守恒定律,空格上缺少的物质是 (填化学式)。
②"黑火药"爆炸时能闻到刺鼻的火药味,是因为爆炸时除了有硫化物,还有硫的氧化物生成。硫在空气中燃烧的化学方程式为 。
(3)制备。古代曾用硝土(含有Ca(NO 3) 2、少量NaCl等)和草木灰(含有K 2CO 3)作原料制取KNO 3.某化学兴趣小组设计了如图实验流程:
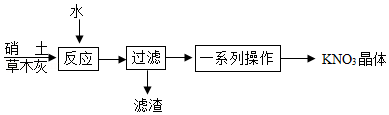
①"反应"过程中的化学方程式为 。
②"过滤"操作必须用到的玻璃仪器有烧杯、玻璃棒和 。
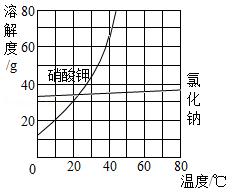
③如图是硝酸钾和氯化钠的溶解度曲线。"一系列操作"包括"加热蒸发浓缩、再冷却到一定温度、过滤"等步骤。其中"冷却到一定温度"能获得纯度较高的硝酸钾晶体的原因是 。
(4)发展。现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C 3H 5O 9N 3)。
①硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。该氧化物中氮为+2价,其化学式为 。
合成硝化甘油的化学方程式为C 3H 8O 3+3HNO 3═C 3H 5O 9N 3+3H 2O.现用46kg甘油(C 3H 8O 3)和足量硝酸反应,理论上能生成多少硝化甘油?(写出计算过程)
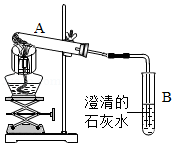
某燃料X在7.2g氧气中燃烧,得到9.2g混合气体(可能含有一氧化碳、二氧化碳、水蒸气)。化学兴趣小组的同学利用下图所示装置验证混合气体的成分。
资料:①浓硫酸具有吸水性。②浓氢氧化钠溶液能吸收二氧化碳。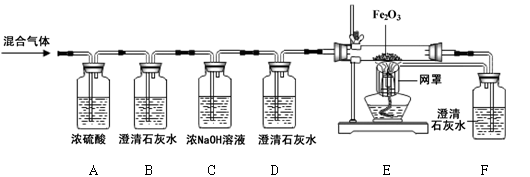
(1)通过混合气体后,A装置增重4.5g,说明混合气体中含有________________________。
(2)B装置中澄清石灰水变浑浊,发生反应的化学方程式为 。D装置的作用是 。
(3)当观察到 ,证明混合气体中有CO。
(4)实验结束后,同学们称量B、C装置共增重3.3g,根据以上数据可确定燃料X中所含元素及元素质量比为_________________。
实验室常用无水醋酸钠(CH 3COONa)固体和碱石灰混合加热的方法制取甲烷。

(1)写出图A中标有序号的仪器名称:① ,② 。
(2)甲烷属于 (填"有机"或"无机")化合物。
(3)实验室制取甲烷应选择的发生装置是 (填字母)。用C装置收集甲烷,发生装置的导管口应与 (填"a"或"b")端相连。
(4)点燃甲烷前需先检验 甲烷完全燃烧的化学方程式是 。
(5)用上述方法收集8g甲烷CH 3COONa+NaOH Na 2CO 3+CH 4↑)理论上至少需要无水醋酸钠的质量是多少?
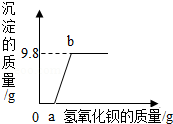
某溶液中可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,取一定质量的该溶液,向其中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。请回答下列问题。
(1)该溶液中一定含有的溶质是 ,可能含有的溶质是 。(均填化学式)
(2)请写出上述过程中发生中和反应的化学方程式 。
(3)当滴加氢氧化钡溶液至图中b点时,溶液中一定含有的溶质是 。(填化学式)
(4)所取溶液中含有氯化铜的质量为 。
现有MgCO 3和BaCO 3组成的固体混合物6g,放入到100g某浓度的稀盐酸中恰好完全反应,得到不饱和溶液的质量为103.8g,则原固体混合物中Mg、Ba两种元素的质量分数总和为 。
如图为木炭还原氧化铜的实验装置。请回答下列问题。
(1)试管A中发生反应的化学方程式是 。
(2)酒精灯加网罩的作用是 。
(3)实验中,试管B中发生反应的化学方程式是
(4)若要使80g氧化铜完全被还原,试管A中实际加入的碳的质量应 6g。(选填">""<"或"=")
波尔多液是一种农药,由Ca(OH) 2溶液和CuSO 4溶液混合而成。某农场需要大量的波尔多液,农场工人就地取材,利用农场废弃的铜渣(只含有铜和一定量的铁)和附近的石灰石来制作波尔多液。下面是制作波尔多液的工艺流程图:

请回答下列问题:
(1)CaO的俗名是 ,写出由CaO生成Ca(OH) 2的化学方程式 。
(2)请说出如何由铜渣得到纯净的铜 。
(3)B物质是 ,写出由B物质生成CuSO 4的化学方程式 。
(4)将铜渣与Zn按质量比10:1的比例分别加入到足量的盐酸溶液中,产生H 2的质量恰好相等,铜渣中铜的质量分数是 。(精确到0.1%)