某兴趣小组同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,测得实验数据如下表所示:
| |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
| 氢氧化钠溶液的质量/g |
20 |
20 |
20 |
20 |
20 |
| 沉淀质量/g |
4.9 |
9.8 |
m |
19.6 |
19.6 |
(1)表格中m的值为多少。
(2)计算恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程)
二氧化硫属于空气污染物,应处理后排放。32g硫与足量的氧气完全反应,生成二氧化硫的质量是多少?
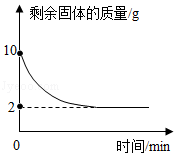
某课外兴趣小组同学取一定量含铜粉的氧化铜粉末,放入烧杯中,加入192g稀硫酸,搅拌,恰好完全反应后过滤(损耗忽略不计),烧杯中固体的质量随时间变化情况如图所示。
(1)所取粉末中氧化铜的质量为 g;
(2)计算反应后所得溶液溶质质量分数。(规范写出计算过程)
欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取30g稀硫酸样品于烧杯中,将15%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示。回答下列问题:
(1)a点溶液中的溶质是 (填化学式)。
(2)计算该稀硫酸的溶质质量分数。(写出计算过程,结果精确到0.1%)

某学生将二氧化锰粉末制成颗粒。放入100g溶质的质量分数为10%的过氧化氢溶液中。一段时间后,取出二氧化锰,共收集到3.2g氧气。
(1)利用化学方程式计算,参加反应的过氧化氢的质量。
(2)向反应后的溶液中加入30%的过氧化氢溶液,使其质量分数重新达到10%备用。计算最终可得到10%的过氧化氢溶液的质量。
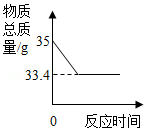
我市覃塘区石灰石资源丰富,某石灰厂为了测定某石灰石样品中CaCO3的质量分数,往盛有300g稀盐酸的烧杯中依次加入粉碎后的石灰石样品(杂质不与盐酸反应),充分反应后,实验数据记录如表:
实验次数 |
第一次 |
第二次 |
第三次 |
石灰石样品/g |
25 |
15 |
10 |
烧杯中物质总质量/g |
316.2 |
326.8 |
m |
请回答:
(1)CaCO3中钙、碳、氧三种元素的质量比为 ;(写最简比)
(2)表中m= ;
(3)所用稀盐酸的溶质质量分数为 ;
(4)求该石灰石样品中CaCO3的质量分数。(写出计算过程)
实验室用34g过氧化氢溶液和2g二氧化锰混合制取氧气。完全反应后剩余物质总质量为35.2g。请计算:
(1)生成氧气的质量为 g。
(2)求所用过氧化氢溶液溶质的质量分数。(根据化学方程式进行计算,写出计算过程)
用光卤石为原料提取的氯化钾产品中含有氯化镁杂质,产品等级中氯化钾指标为:
指标名称 |
优良品 |
一级品 |
二级品 |
氯化钾质量分数(≥) |
93.00% |
90.00% |
87.00% |
为确定某氯化钾产品等级进行了以下实验:
步骤一(溶解):取40.0g氯化钾产品溶于水,配制成溶液。
步骤二(沉淀):向步骤一所得溶液中加入过量的质量分数为10%的氢氧化钾溶液112.0g,充分反应后过滤,得2.9g沉淀和一定质量的滤液。
步骤三(回收):向步骤二所得滤液中加入盐酸至溶液呈中性,得到400.0g溶液,将所得溶液蒸发结晶,回收氯化钾固体。
回答下列问题:(提示:KCl溶液呈中性;不考虑实验过程中的损失)
(1)通过计算判断该产品的等级。(写出解题过程)
(2)步骤三所得溶液中氯化钾的质量分数为 。
实验室用34克过氧化氢溶液和1克二氧化锰制取氧气,实验的相关数据如图。请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的 都没有发生变化。
(2)反应生成氧气的质量为 g。
(3)计算过氧化氢溶液中溶质的质量分数。(此问必须要有计算过程)
工业合成氨的相关反应式为:N2+3H2 2NH3
(1)合成氨的原料气中可以通过分离空气直接得到的是 。
(2)当前,原料气H2可用天然气来制取,理论上每生产1吨H2会同时产生5.5吨CO2,有科学家正在研究一种不生成CO2的新方法来制取原料气H2.若需要合成8.5万吨氨,改用新方法制取原料气H2可以减少排放多少万吨CO2?
实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验中非气态物质的总质量随时间变化如图所示。回答下列问题:
(1)反应中二氧化锰的作用是 。
(2)计算过氧化氢溶液中溶质的质量分数。(写出计算过程)

酸、碱、盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出 (填字母)。
a.H2O b.H2 c.H+ d.OH﹣
(2)检验敞口放置的氢氧化钠溶液是否变质,可以选用的一种试剂是 。
(3)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图1,当滴入溶液为V2mL时,所得溶液中溶质的化学式为 ,所得溶液能使紫色石蕊溶液变成 色。
(4)氯化钠是生活中常见的盐。为除去某粗盐水中的MgSO4、CaCl2杂质,得到NaCl溶液,某化学小组设计了如图2实验方案:
①过滤操作中所用到的玻璃仪器有烧杯、漏斗和 。
②以上方案中有关反应的化学方程式为 (写一个即可)。
③写出溶液乙中含有的杂质,并将以上方案补充完整
。
(5)某实验室用20%的NaOH溶液洗涤一定量石油产品中残余的H2SO4,消耗NaOH溶液40g,洗涤后的溶液呈中性,请计算该一定量石油产品中H2SO4的质量。
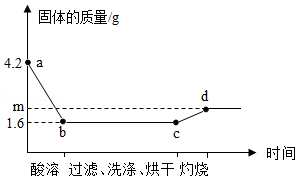
取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图。(1)b点时溶液中溶质的化学式为 。
(2)原粉状混合物中铁粉的质量为 g。
(3)求m的值。(写出计算过程)
有一包白色粉末,可能含氯化钠、氢氧化钠、碳酸钠中的一种或几种,为了确定其组成,小明称取了9.3克粉末,向其中加入100克7.3%的稀盐酸充分反应,生成的二氧化碳气体完全逸出(忽略其他物质逸出),所得溶液的质量为107.1 克。用pH试纸检测溶液呈中性。
(1)产生二氧化碳气体的化学反应方程式为 。
(2)这包白色粉末的成分为 。
(3)求所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)