鸡蛋壳的主要成分是碳酸钙.小明同学为了测定鸡蛋壳中碳酸钙的质量分数,分别设计了如下实验并进行计算.将鸡蛋壳洗净、干燥并捣碎后放入锥形瓶里,加入足量的稀盐酸充分反应(假设其他杂质不与盐酸反应).
测得相关数据如图所示:

【数据处理】
(1)反应生成二氧化碳的质量为 g.
(2)请帮小明计算鸡蛋壳中碳酸钙的质量分数,并写出计算过程:
实验过程如果有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比 (填“偏大”、“偏小”或“不变”)
已知某氯化钠样品中含有少量的碳酸钠。某课外小组对其成分进行实验测定。甲、乙、丙三位同学分别进行实验,实验数据如下表:
| |
甲 |
乙 |
丙 |
| 所取混合物的质量/g |
4 g |
4 g |
5 g |
| 加入稀盐酸的质量/g |
50 g |
40 g |
40 g |
| 反应后产生气体的质量/g |
0.44 g |
0.44 g |
0.44 g |
(1)所取混合物与稀盐酸恰好完全反应的是________同学的实验。
(2)该同学所取的混合物中碳酸钠的质量。
(3)计算该同学所取混合物与稀盐酸恰好完全反应后,所得溶液中溶质的质量分数。
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液.某课外活动小组想测定20g该
品牌洁厕灵溶液中H2SO4和HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如下所示:
滴加氢氧化钡溶液的质量/g5 10 25
烧杯中产生沉淀的质量/g1.165 2.33 4.66
(已知BaCl2溶液的pH=7;Ba的相对原子质量137)
求:20g该品牌洁厕灵溶液中H2SO4的质量和HCl的质量.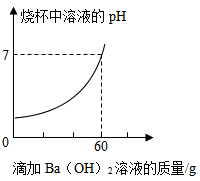
要测定MgCl2(杂质是NaCl)的质量分数,取样品10g溶于100g水中,向其中加入50g NaOH溶于至恰好完全反应,得到沉淀5.8g.已知:MgCl2+2NaOH═Mg(OH)2↓+2NaCl,求:
(1)样品中MgCl2的质量分数.
(2)所用NaOH溶液的溶质质量分数.
用100t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?(要求根据化学方程式进行计算,计算结果精确到1t)
实验室有一瓶未知浓度的盐酸,小华为测定该盐酸中溶质的质量分数,取10g溶质的质量分数为16%的氢氧化钠溶液,逐滴滴加该盐酸至恰好完全反应,共消耗盐酸20g,请计算:
(1)10g氢氧化钠溶液中溶质的质量为 g.
(2)该盐酸中溶质的质量分数.
通常认为CO2是引起温室效应的主要气体,但它也是一种重要的资源,关键是人类要采取适当技术对其进行利用,变废为宝.生产车用甲醇汽油中甲醇(CH4O)的反应之一为:CO2+3H2=CH4O+H2O.如按此反应,消耗88吨CO2,可生产多少吨甲醇?
某化工厂排放的废水中含有一定量的氢氧化钾,为了回收利用,欲用2%的稀盐酸测定废水中的氢氧化钾含量(废水中其他杂质不与盐酸反应),现取50g废水于锥形瓶中,逐滴加入2%的稀盐酸至恰好完全反应时,消耗稀盐酸7.3g,求废水中氢氧化钾的质量分数。
某校化学兴趣小组用一瓶含有少量氯化钠的硫酸钠固体样品,进行如图所示的实验.

请根据以上信息计算(结果保留到小数点后两位):
(1)反应生成沉淀的质量为。
(2)样品中氯化钠的质量。
(3)滤液中溶质的质量分数。
在氯化钙和氯化钠的混合物中加入一定量的水,全部溶解得到50克混合溶液,向该溶液中逐滴加入一定溶质质量分数的碳酸钠溶液,生成沉淀与加入碳酸钠溶液的质量关系如图所示.计算:
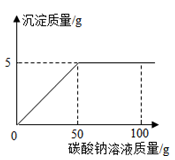
(1)所加碳酸钠溶液的溶质质量分数.
(2)若恰好完全反应时所得溶液的溶质质量分数为10%,则原固体混合物的质量是多少?
用5%的过氧化氢溶液和二氧化锰混合制取氧气,请计算。
(1)制取0.8g氧气,需要这种过氧化氢溶液的质量。
(2)要配制这种过氧化氢溶液60g,需要30%的过氧化氢溶液的质量。
碳和氧化铜反应生成铜和二氧化碳.现有碳和氧化铜的混合物20g.其中氧元素的质量分数为18%,高温加热该混合物一段时间后,产生4.4g二氧化碳。计算:
(1)参加反应的氧化铜的质量。
(2)剩余固体中氧元素的质量分数(计算结果保留到0.1%)。
50g硝酸钙溶液与56g碳酸钾溶液混合后,恰好完全反应,过滤得到硝酸钾的不饱和溶液101g,反应的化学方程式为
.
(1)生成碳酸钙沉淀的质量为g。
(2)计算反应后硝酸钾的不饱和溶液中溶质的质量分数。
铝合金的生产与销售是潍坊市一条重要的产业链,为测定某种铝铜合金中铝的质量分数,探究小组进行了如下实验:
| 实验编号 |
铝铜合金的质量(g) |
加入稀硫酸的质量(g) |
生成H2的质量(g) |
| 实验1 |
30 |
392 |
2 |
| 实验2 |
30 |
588 |
3 |
| 实验3 |
30 |
600 |
3 |
(1)所用稀硫酸溶质的质量分数为.
(2)该铝铜合金中铝的质量分数是多少?
实验室中有一瓶含有少量氯化钠和可溶性杂质的硫酸钠样品.某化学兴趣小组对该样品成分进行定量测定,甲、乙、丙三位同学分别称取一定质量的样品放入烧杯中,溶入足量水后过滤得到滤液;再向滤液中加入一定质量的氯化钡溶液,充分反应后过滤,将沉淀洗涤、干燥并称量.相关实验数据记录如下:
| 称量项目 |
甲 |
乙 |
丙 |
| 所取样品的质量/ | 15 |
15 |
20 |
| 加入氯化钡溶液的质量/ | 150 |
100 |
100 |
| 反应后所得沉淀的质量/ | 23.3 |
23.3 |
23.3 |
请回答下列问题:
(1)同学(选填"甲""乙"或"丙")所取用的样品与氯化钡溶液恰好完全反应。
(2)计算该样品中硫酸钠的质量分数.(写出计算步骤,计算结果保留到0.1%)
(3)若欲计算出样品与氯化钡溶液恰好完全反应时所得溶液的溶质质量分数,上述实验过程中还需要测定的数据是。