化肥对提高农作物的产量具有重要的作用,碳铵(碳酸氢铵)就是农民朋友经常使用的一种氮肥,碳铵易溶于水、受潮时常温分解,温度越高分解越快,遇碱时放出氨气。某校化学兴趣小组为测定某碳铵肥料样品的纯度,将8.5g样品加入足量的浓氢氧化钠溶液中共热,(碳铵中的杂质不与氢氧化钠反应,反应的方程式为
,把产生的所有
用足量的硫酸溶液吸收,同时测量两分钟内硫酸溶液增加的质量,结果如下表所示。
时间/S
|
0
|
20
|
30
|
40
|
60
|
80
|
100
|
120
|
增加质量/g
|
0
|
0.7
|
m
|
1.2
|
1.5
|
1.6
|
1.7
|
1.7
|
试回答下列问题:
(1)根据碳酸氢铵的性质,你认为在使用碳铵肥料时应注意的问题是。
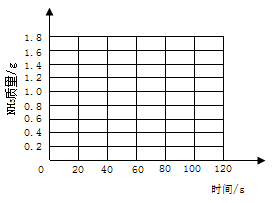
(2)请在坐标纸上,以反应时间为横坐标,以产生
质量为纵坐标,画出产生气体的质量随时间变化的关系曲线,并判断表中m约为。
(3)试计算该样品中碳酸氢铵的质量分数(写出计算过程,计算结果保留一位小数)。