金属材料在生产、生活中应用广泛。
(1)铝制成铝箔是利用了铝的 性;灯泡的灯丝用钨制而不用锡制,是因为 。
(2)钢铁是使用最多的金属材料。生铁和钢的性能不同,主要是因为它们的 不同
(3)沙漠地区的铁制品锈蚀较慢的原因是 。工业上用稀盐酸除铁锈的化学方程式为 。
水是一种宝贵的资源。
(1)水能参与很多化学反应。水通电分解的化学方程式为 ,该实验说明了水是由 组成的。
(2)水能溶解许多物质,是最常见的 。加入洗涤剂的水可洗掉餐具上的油污是因为洗涤剂能使油污发生 现象。
(3)爱护水资源一方面要 ,另一方面要防治水体污染。磷酸二氢铵(NH4H2PO4)是一种化肥,当其含有的 两种元素排入水体,可能导致水体富营养化。
金属材料在生活中随处可见回答下列问题:
(1)钢和生铁都属于金属材料,它们都是 的合金。
(2)钢铁很容易生锈,用盐酸除铁锈的化学方程式为 。
(3)向一定量的硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后过滤,得滤渣和滤液。向滤渣中加入稀盐酸有气泡产生。则滤液中包含的基本粒子是 (用符号表示)。
如图是某品牌的风味酸牛奶及每100g酸牛奶中主要营养成分数据。请回答下列问题。
营养成分 |
蛋白质 |
脂肪 |
糖类 |
钠 |
钙 |
质量 |
3.2g |
3.6g |
11.9g |
60mg |
80mg |
(1)人体必需的六大类基本营养素中,除水外,表中没有标示的营养素是 。
(2)表中能为人体提供能量的营养素有 种。
(3)该酸牛奶的外包装是一种塑料制品,随意丢弃会造成“白色污染”。为减少“白色污染”,可采取的措施是 (答一点)。
(4)酸牛奶中的蔗糖,在胃肠内转化为葡萄糖(C6H12O6)。葡萄糖在酶的催化作用下,与氧气反应生成水和二氧化碳,请写出该反应的化学方程式 。

阅读下面二氧化硫的相关信息,并回答问题:
二氧化硫是无色、有刺激性气味的气体,密度比空气大,容易液化,易溶于水。二氧化硫与水反应生成亚硫酸(H2SO3),溶液显酸性。亚硫酸不稳定,容易分解成水和二氧化硫。二氧化硫在一定条件下,可以被氧气氧化成三氧化硫。实验室通常用亚硫酸钠(Na2SO3)和70%的硫酸反应来制取二氧化硫。
(1)通过以上信息可知二氧化硫的化学性质有 (答出一条即可)
(2)二氧化硫和二氧化碳既有相似性,又有差异性。通过以下实验进行比较:
实验一:在水槽中滴入紫色石蕊溶液将收集满两种气体的试管同时倒立于其中,一段时间后实验现象如图所示,同时观察到左侧试管内溶液变红,右侧试管内溶液 (填“变红”或“不变红”)。该实验说明相同条件下二氧化硫的溶解性 (填“大于”或“小于”)二氧化碳的溶解性。
实验二:将少量二氧化碳和二氧化硫分别通入澄清石灰水中,都出现白色浑浊。请用化学方程式解释二氧化硫使澄清石灰水变浑浊的原因: 。

家用燃料使用的发展历程(括号内表示主要成分)是我国能源结构调整的缩影。结合所学知识回答下列问题
(1)蜂窝煤被加工成多孔形状的目的是 。
(2)天然气通常被称为“清洁能源”,主要是因为甲烷的含碳量较低,燃烧较完全,燃烧产生的二氧化碳相对较少,对大气的污染较轻。甲烷充分燃烧的化学方程式为CH4+2O2 CO2+2H2O,丙烷充分燃烧的产物与甲烷充分燃烧的产物相同,请写出丙烷充分燃烧的化学方程式: 。通过家用燃料由液化石油气发展到天然气,表明我国的能源结构正在向多元和 转型。
根据如图实验,回答问题:
(1)FeSO4中硫元素的化合价为 。
(2)生成红褐色固体的总反应的化学方程式为 。
提示:①Fe(OH)2在空气中极易被氧化。②方程式中FeSO4的配平系数为4。

下列指定反应的化学方程式正确的是( )
A.酸雨形成的原因CO2+H2O═H2CO3
B.证明铜的活动性大于银:Cu+2AgCl═2Ag+CuCl2
C.用含氢氧化铝的药物治疗胃酸过多:Al(OH)3+3HCl═AlCl3+3H2O
D.超氧化钾(KO2)与二氧化碳反应生成碳酸钾和氧气:2KO2+CO2═K2CO3+O2
MgO在医药建筑等行业应用广泛。硫酸镁和木炭高温煅烧的产物为MgO(固体)、SO2、CO2、CO、硫蒸气。
(1)工业上,SO2的任意排放会引起的环境问题是 。化石燃料燃烧是产生SO2的主要原因,下列做法能减少SO2排放的是 (填字母)。
a.开发新能源替代化石燃料 b.向高空排放SO2
(2)在高温、催化剂条件下,CO和H2可化合成燃料甲醇(CH3OH),该反应中CO和H2的分子个数比为 。若CO和H2中混有H2S气体,H2S会与催化剂中的Cu在高温下发生置换反应,其中一种产物为CuS,该反应的化学方程式为 。
(3)利用如图装置对硫酸镁和木炭进行高温煅烧,并对产生的四种气体进行分步吸收或收集。
已知:常温下,硫为固体;SO2、CO2均能与NaOH溶液反应。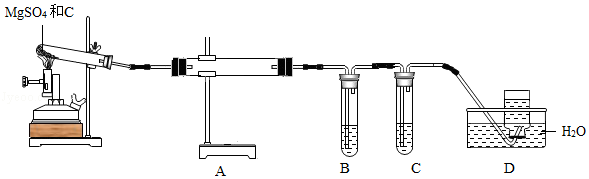
①装置B、C中的溶液分别是 、 。(填字母)
a.NaOH溶液
b.KMnO4溶液
②装置B、C的作用分别是 、 。
③装置D的作用是 。
④若将装置A中的固体隔绝空气加热至500℃,就会变成蒸气,其中有一种相对分子质量为128的气体。该气体的化学式为 。
请根据下列实验装置图回答有关问题:

(1)写出标号仪器的名称:① ;② 。
(2)实验室收集少量氢气时,可选用的装置是 (填字母)。实验室制取少量二氧化碳时,若用装置C收集二氧化碳,则检验其是否收集满的方法是 。
(3)若实验室采取加热KClO3与MnO2的混合物制少量O2,则可选用的发生装置是 (填字母),二氧化锰固体的颜色是 ,反应的化学方程式为 。
(4)已知:一氧化氮(NO)是生命体系信息分子之一,在常温下,它是难溶于水且不与水反应,易与O2反应生成二氧化氮(NO2)的气体。
①NO与O2反应生成NO2的化学方程式为 。
②实验室收集少量NO的装置可用 (填字母)。
实验室制取气体时需要的一些装置如图所示,请回答下列问题:
(1)写出标有序号的仪器名称:① 。
(2)实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是 ,其中实验室制O2的化学方程式为 。
(3)若要制取并收集到干燥的氧气,所选择装置的连接顺序为: (填字母序号)。
(4)若B装置用于实验室制取二氧化碳,则反应的化学方程式为 。
(5)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,甲烷密度比空气小,难溶于水,收集装置可以选择 (填字母序号,一种即可);请写出甲烷完全燃烧的化学方程式 。
能源的利用与社会可持续发展密切相关。
(1)煤燃烧时产生NO2、 等气体,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
(2)在一定条件下,甲烷(CH4)和水反应(未配平)的微观示意图如图所示。

①W表示的物质的化学式是 。
②该反应中两种生成物Z和W的分子个数比为 。
(3)实验室可用锌和稀硫酸反应制取氢气。写出该反应的化学方程式: 。
目前,氢气作为新能源在生活和生产中还未能广泛应用,其原因是 。
(4)在高温下,工业上以赤铁矿(主要成分是Fe2O3)和一氧化碳反应来炼铁的化学方程式为 。
请回答下列实验问题:
(1)现提供下列装置:

①如图E装置中,甲仪器的名称是 。
②实验室用KClO3和MnO2混合制O2,发生装置可选用 (填装置序号),用装置C干燥O2,气体由导管 端(填“a”或“b”)进入,用E装置收集O2的依据是 。
③英国化学家布莱克是第一个“捕捉”到CO2的人,实验室制备CO2的化学方程式为 ;1774年德国化学家贝格曼将CO2通入紫色石蕊试液中,发现试液由紫色变为红色,此反应的化学方程式为 。
(2)对一定质量的粗盐(含泥沙)进行初步提纯。
①实验的主要步骤:称量与溶解、过滤、蒸发;蒸发结束后用 (填仪器名称)将固体从蒸发皿转移到纸片上,比较食盐提纯前后的状态。
②下列有关蒸发过程说法正确的是 (填序号)。
a.蒸发时用玻璃棒不断搅拌
b.当蒸发皿中水分全部蒸干时,停止加热
c.蒸发时若有滤液溅出,则精盐质量将偏低
d.蒸发过程中,溶液中钠元素质量增大
化学与科技、生产、生活密切相关。
(1)某学校的营养早餐配料标签如图1所示,该配料中富含油脂的物质是 。当衣服上粘有油脂时,可以用洗衣粉除去,其去污原理是 。
(2)泰州是中国人民解放军海军的摇篮,138泰州舰上使用的
玻璃钢属于 材料;舰体在高盐的海水中易生锈,原因是海水中所含的 物质存在时会加速铁的锈蚀。
(3)利用植物秸秆、牲畜粪便等可制得沼气,沼气的主要成分甲烷在空气中完全燃烧的化学方程式为 ,推广使用沼气做燃料的优点是 (答1点即可)。
(4)一种创可贴中间有个凸起的小囊区,如图2.按贴伤口的同时,小囊区内的水和硝酸铵固体被挤破混合,利用硝酸铵固体溶解时温度 ,起到快速止血的作用。
