古往今来,金属材料和制品在生产生活中应用广泛。
(1)三星堆遗址发掘现场出土了华丽的鸟型金饰片,金能被加工成超薄金箔,是因为金具有良好的 ;同时出土的铜头像、青铜神树等表面有锈迹,铜生锈的主要原理是:2Cu+H2O+O2+X═Cu2(OH)2CO3,X的化学式为 。
(2)向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热充分反应后冷却、过滤得到滤渣和滤液。
①在滤液中加入一枚洁净的铁钉,发现铁钉表面无任何变化,则滤液中一定没有的阳离子是 (填离子符号)。
②向滤渣中再滴入稀硫酸产生气泡,则滤渣中一定含有 (填名称)。
氯化钠是生产、生活中的一种重要化合物,应用很广泛。
Ⅰ.图甲和图乙分别是钠原子和氯原子的原子结构示意图。

(1)图甲中的x= 。
(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有 个电子的相对稳定的氯离子,氯离子用化学符号表示为 。
Ⅱ.如表是氯化钠在不同温度下的溶解度数据。
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
(1)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于
(填“饱和”或“不饱和”)溶液。
(2)医用盐水(溶质为NaCl)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其中含NaCl的质量为 g。
(3)学生化学实验活动之一:配制50g质量分数为6%的氯化钠溶液,该实验需要的仪器有药匙、托盘天平、玻璃棒、胶头滴管、 (从下列图中选择写出名称)。

Ⅲ.工业上常用电解饱和食盐水的方法来制取氢氧化钠、氯气和氢气,其化学反应方程式可表示为:xNaCl+yH2O zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
(填数字)。
大量实验证明,化学反应符合质量守恒定律。
(1)如图是铁钉与硫酸铜溶液反应的实验。
①反应一段时间,观察到的现象是 ;
②该反应的化学方程式是 ;
③溶液中减少的铜元素质量等于反应生成的 的质量。
(2)取足量的铁、锌,各加入相同质量相同溶质质量分数的稀盐酸,完全反应后,铁、锌均有剩余,下列说法正确的是 。
| A. |
生成氢气的质量相等 |
| B. |
生成的氯化亚铁和氯化锌的质量相等 |
| C. |
参加反应的铁和锌的质量相等 |
| D. |
参加反应的稀盐酸中HCl的质量相等 |
(3)经计算3g镁和100g质量分数7.3%的盐酸充分反应可生成氢气0.2g,但经实验测定,生成氢气的质量大于0.2g,则可能的原因是过量的镁与 发生反应。

阅读下面科普短文。
碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过液态碳和晶形碳三大类,如图1。

石墨是制铅笔芯的原料之一,在16世纪被发现后,曾被误认为是含铅的物质。直到18世纪,化学家将石墨与KNO3共熔后产生CO2,才确定了它是含碳的物质。
碳纤维既有碳材料的固有本质特性,又有纺织纤维的柔软可加工性,综合性能优异。目前,我国已形成碳纤维生产、碳纤维复合材料成型,应用等产业链,碳纤维复合材料应用领域分布如图2。
科学界不断研发出新型碳材料,碳气凝胶就是其中一种。碳气凝胶具有优良的吸附性能,在环境净化中发挥重要作用。我国科研人员在不同温度下制备了三种碳气凝胶样品,比较其对CO2的选择性吸附性能。他们在不同压强下测定了上述样品对混合气体中CO2吸附的选择性值,实验结果如图3。图中选择性值越高,表明碳气凝胶对CO2的选择性吸附性能越好。
随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。
依据文章内容回答下列问题:
(1)金刚石属于 (填序号)。
A.无定形碳
B.过渡态碳
C.晶形碳
(2)石墨与KNO3共熔,能发生如下反应,配平该反应的化学方程式:5C+4KNO3
K2O+ N2↑+ CO2↑。
(3)由图2可知,我国碳纤维复合材料应用占比最高的领域是 。
(4)判断下列说法是否正确(填“对”或“错”)。
①石墨是一种含铅的物质 。
②碳材料其有广阔的应用和发展前景 。
(5)对比图3中三条曲线,得到的实验结论是 。
小明同学对金属的有关化学性质进行梳理和总结。请完成下列问题。
(1)对图1中几种金属的原子结构示意图进行分析,发现金属原子最外层电子一般都 4个,在化学反应中容易 电子变成阳离子,小明同学判断D和E的化学性质相似,他的依据是 ;

(2)如图2,将一锌片投入稀硫酸中,观察到的现象是 ,该反应过程溶液中增加的粒子是 (用符号表示),溶液的pH (填"逐渐减小""逐渐增大"或"不变"),反应的化学方程式为 。

(3)图3是将铜丝插入硝酸银溶液中反应的微观示意图,从微观粒子变化的角度分析该反应的实质是 ,反应过程中溶液的质量变化是 (填"增大""减小"或"不变")。
化学就在我们身边,化学与生活息息相关.
(1)如表为某食品包装袋的部分说明:
| 商品名称 |
××饼干 |
| 配料 |
小麦粉、白砂糖、精炼植物油、鸡蛋、食盐、食品添加剂(碳酸氢铵、碳酸氢钠、柠檬酸等) |
| 规格 |
180g |
| 保持期 |
10个月 |
请回答下列问题:
①在饼干的配料中,富含蛋白质的是
②碳酸氢钠的俗称 ;在医疗上,它是治疗 症的一种药剂.
③考虑到营养均衡,把榨好的蔬菜汁放在面粉中和面,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养素是糖类和 .
(2)饮用硬度过大的水不利于人体健康,日常生活中常用 来区分硬水和软水,可用 的方法降低水的硬度.
(3)交警通过酒精检测仪显示的颜色变化,可快速检测出司机是否酒后驾车,其反应原理为2CrO 3(红色)+3C 2H 5OH+3H 2SO 4═Cr 2(SO 4) 3(绿色)+3CH 3CHO+6X,X的化学式为 .
水在生活、生产中和化学实验中起着十分重要的作用.
Ⅰ.自来水厂净化水的过程为:取水→过滤→吸附→消毒,高铁酸钾(K 2FeO 4)能用作絮凝剂.
(1)制备K 2FeO 4的化学方程式为2Fe(OH) 3+3Cl 2+10KOH═2K 2FeO 4+6X+8H 2O,则X的化学式为 ,K 2FeO 4中铁元素的化合价为 .
(2)自来水厂净化水的过程 (填"能"、"不能")将硬水软化成软水.
Ⅱ.欲证明一瓶无色透明液体是纯净水,可靠的实验方法是 .
A.1.01×10 5Pa时沸点为100℃
B.测得其pH=7
C.电解时得到H 2与O 2的体积比为2:1
Ⅲ.请根据如图实验现象并结合溶解曲度线回答(其中甲、乙、丙均不含结晶水)

(1)生石灰与水反应的化学方程式为 ,试管内所盛饱和溶液的溶质为对应溶解曲度线中的 (填甲、乙、丙).
(2)如果要配制相同浓度的甲、乙饱和溶液,需要把温度控制在 ℃.
(3)t 3℃时,将甲、乙、丙的饱和溶液都降温到t 1℃,溶液中溶质质量分数由小到大的顺序为 .
化学与生活息息相关,我们的衣、食、住、行都离不开化学。说到"行",火车、汽车、轮船、自行车等交通工具,都离不开金属材料。
(1)钢铁在潮湿的空气中会生锈,其实质是铁与空气中的 发生了缓慢氧化;采取一定的措施可防止自行车铁制部位生锈,请你列举一例 。
(2)汽车上的电瓶大多使用的是铅蓄电池,铅蓄电池报废后应回收处理,原因是 。
(3)汽车酒驾事件,当警钟长鸣。交警通过酒精检测仪可快速测出司机是否酒后驾车。其反应原理为:2X(红色)+3C 2H 5OH+3H 2SO 4=Cr 2(SO 4) 3(绿色)+3CH 3CHO+6H 2O
X的化学式为 。
有一工业过程:

按要求回答下列问题:
(1)请将电石与水反应的化学方程式补充完整:
CaC 2+2H 2O═Ca(OH) 2+ ↑.
(2)有关物质常温下的溶解度如表:
| 物质 |
Ca(ClO 3) 2 |
CaCl 2 |
KClO 3 |
KCl |
| 溶解度/g |
209.0 |
74.5 |
7.3 |
34.2 |
上述流程中加入了KCl粉末,KCl与 (填化学式)发生了复分解反应得KClO 3晶体,该过程得到KClO 3晶体的原因是 .
(3)写出向CaCl 2溶液中通入两种气体生成CaCO 3的化学方程式: .
以黄铁矿(主要成分为FeS 2)为原料生产硫酸的工艺流程如图所示:
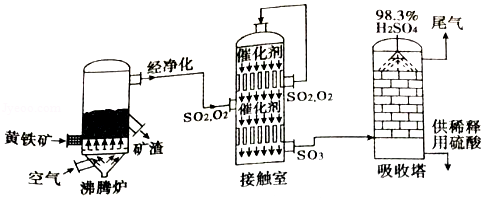
(1)沸腾炉中发生反应的化学方程式为:4FeS 2+11O 2 2X+8SO 2,其中X的化学式为 。
(2)接触室中发生反应的化学方程式为:2SO 2+O 2 2SO 3,产物SO 3中硫元素的化合价为 ;吸收塔中发生反应的化学方程式为:SO 3+H 2O═H 2SO 4,该反应的基本类型是 。若有800kg三氧化硫进入吸收塔中,且完全被吸收,则理论上制得硫酸的质量为 kg。
(3)O 2、SO 2、SO 3、H 2SO 4四种物质中属于氧化物的是 。
(4)实验室中稀释浓硫酸的操作是 。