世博同学在探究铝、铜、银三种金属活动性顺序时做了如下实验,并由此得出了正确结论。
(1)请指出上述实验操作中的错误________________________________________;
(2)乙中发生的化学反应方程式为______________________________。
化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题:
(1)“沙里淘金”说明黄金在自然界中能够以 (填“单质”或“化合物”)形式存在。
(2)刘大爷种的小麦出现倒伏现象,你会建议他使用化肥中的 肥。
(3)长期使用的热水瓶内胆常有一层水垢(主要成分为碳酸钙),可以用稀盐酸除去。请写出反应的化学方程式: 。
生铁和钢都是铁的合金,在生活中有着广泛的用途。
(1)铁合金材料属于 (填“混合物”或“化合物”);
(2)生铁含碳量比钢 ,生铁炼钢的过程属于 ,(选填物理变化或化学变化);
(3)用过量稀盐酸除去铁锈,会产生气泡的原因是(用化学方程式表示) _。
将一铁片放在硫酸铜溶液中,片刻后取出,发现铁片表面有 色物质生成,写出
反应的化学方程式: 。
(1)中国的青铜举世闻名,青铜属于 材料;
(2)中国的铁锅源远流长,受到联合国卫生组织的推崇,原因之一是由于铁锅能为人体补充铁元素。若人体缺乏铁元素,容易引起 症;
(3)被发掘出的宋代铜钱已经锈迹斑斑,这是因为铜能与空气中的 、 以及二氧化碳发生化合反应生成铜绿[Cu2(OH)2CO3],请写出该反应的化学方程式: ;若要除去铜钱表面的铜绿,可选用的试剂为 (填化学式)。
在加热的条件下浓硫酸与铜反应
Cu+ H2SO4浓 =△= CuSO4+SO2↑+2
H2SO4浓 =△= CuSO4+SO2↑+2 (请在方框内填上适当的数字和化学式使之成为完整的化学方程式)。但足量的铜和浓硫酸充分反应后溶液中仍有硫酸剩余,原因是 。
(请在方框内填上适当的数字和化学式使之成为完整的化学方程式)。但足量的铜和浓硫酸充分反应后溶液中仍有硫酸剩余,原因是 。
金属材料在生活、生产中应用非常广泛,请仔细看图并填空:

(1)图A主要是利用了金属的 性。
(2)图B是用两块金属片相互刻划,观察到在纯铜片上有明显的划痕。该实验探究的目的是 。
(3)2010年5月,400多年前的古沉船“南澳一号”成功打捞。图C是古船上部分文物图片,其中可以判断铁比铜活泼的信息是 。稀盐酸除锈的化学程式为 :Fe2O3+ 6HCl = 2FeCl3+ 3H2O,该反应的基本类型为 。生活中常用的防锈方法有 。
(4)为了比较铁和铜的活动性,小华选用了硫酸铜溶液。请你写出该反应的化学方程式 。
农业上配制波尔多液(CuSO4溶液)时,不用铁桶盛装,原因是 (用化学方程式表示),该反应说明铁的活动性比铜 (填“强”或“弱”);黄金是一种贵重金属,各种黄金首饰易于保存,具有收藏价值的主要原因是 。
(1)《淮南万毕术》:“曾青得铁,则化为铜,外化而内不变”,有人据此说,早在西汉时候(公元前),中国已经知到了下面的反应。请写出相关的化学方程式:
(2)“遥知不是雪,为有暗香来”,产生这一现象的原因是因为分子具有 的性质。
(3)“釜底抽薪”的灭火原理是 。
为探究金属A、金属B、金属银的活动性顺序,小明同学做了如下实验实验1:将金属A放入硫酸铜溶液中,金属A表面有红色金属B析出实验2:将金属B放入硝酸银溶液中,金属B表面逐渐变为银白色.由本实验可得出,这三种金属中 的活动性最强.
甲、乙、丙、丁均为常见物质,由氢、碳、氧、氯、铁、钙6种元素中的1-3种组成。在一定条件下,四种物质存在如下转化关系:甲 + 乙 → 丙 + 丁。
(1)若甲的固体俗称干冰,其化学式是 。写出符合上述转化关系的一个化学方程式 。
(2)若甲、丙均为单质,反应后溶液为浅绿色。则符合上述转化关系的反应物是 。
(3)如图所示。关闭止水夹,将装置A注射器中的液体推入瓶中,与集气瓶中收集的气体发生上述(1)的反应,待恰好反应完全后,将装置B分液漏斗中过量的液体放入瓶中(使液面没过导管下端),与瓶中适量固体接触,发生上述(2)的反应,立即关闭开关,打开止水夹,可以看到的现象有:B中的液体进入A中、 ,分析B中液体进入A中的原因是 。

某同学取一块表面完全锈蚀的生铁片进行了以下探究:
(1)实验: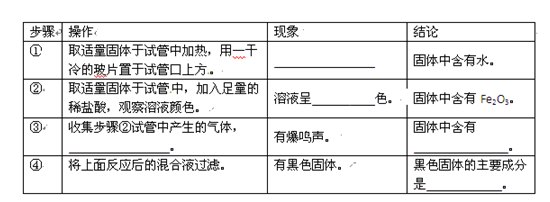
(2)表达:步骤②的化学方程式为__________________、___________________。
(3)拓展:取2枚未生锈的铁钉,一枚部分浸入蒸馏水、另一枚部分浸入盐水,生锈较快的是______________。
为了验证铁、铜、银的金属活动性顺序,设计了如下实验:
Ⅰ.将铁片浸入稀硫酸
Ⅱ.将铜片浸入稀硫酸
Ⅲ.将铁片浸入硝酸银溶液
(1)上述实验(选填"能"或"不能")验证三种金属的活动性顺序。
(2)将铁、铜、银三种金属浸入溶液(只填一种),即可验证它们的活动性顺序。
化学不仅为人类生活创造物质基础,还为人类社会可持续发展做出了巨大贡献。
(1)钢铁是人类生产和生活中非常重要的材料,但每年因锈蚀而损失的数量是巨大的,钢铁锈蚀的条件是与 和 同时接触,防止钢铁生锈措施有
(写一点即可),铁锈(主要成分为Fe2O3)可用稀盐酸将其除去,化学方程式为: 。
(2)合金在生活中应用广泛、下列有关合金的说法正确的是 (填字母)。
| A.合金的熔点一般比它的成分金属高 |
| B.合金的硬度一般比它的成分金属低 |
| C.组成合金的元素种类相同,合金的性能就一定相同 |
| D.合金与各成分金属相比,具有许多优良的物理、化学或机械性能 |
(3)自热米饭的发热包中有铁粉、镁粉、碳粉等物质,使用时,镁粉和H2O、O2反应生成Mg(OH)2,并放热,反应的化学方程式 。
检验发热包中是否含有铁粉的方法是:取少量发热包中固体,加入 ,若 ,则含有铁粉。
(4)往Zn(NO3)2和Cu(NO3) 2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生.则滤渣中一定有 ,滤液中一定有 。
金属具有广泛的应用,根据金属及其化合物的性质和用途,请回答:
(1)下列金属制品中,利用金属导电性的是 (填字母序号)。
A.黄金饰品 B.铝蒸锅 C.铜导线
(2)铁制品在沙漠地区不易锈蚀的原因是 。
(3)某化学小组用一定量的硝酸银和硝酸铜的混合溶液进行了如图所示实验,并对溶
液A和固体B的成分进行了分析和实验探究。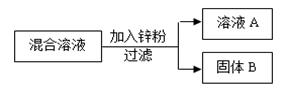
【提出问题】溶液A中的溶质可能有哪些?
【做出猜想】①只有硝酸锌 ②硝酸锌、硝酸银
③硝酸锌、硝酸铜 ④硝酸锌、硝酸铜、硝酸银
【交流讨论】不合理的猜想是 (填序号)。
【实验探究】若猜想①成立,通过以下实验可探究固体B的成分,请填写下表。
| 实验步骤 |
实验现象 |
化学方程式及结论 |
| 取少量固体B,滴加 |
有气泡产生 |
固体B的成分是 |