(8分)取只含有少量氯化钠杂质的粉末状纯碱样品11.4g于烧杯中,逐滴加入稀盐酸至不再产生气体为止,共消耗稀盐酸的质量为50g,反应后称得烧杯中溶液的质量为57g(假定反应产生的二氧化碳全部逸出,水蒸气挥发忽略不计)。请分析回答下列问题:
(1)题中涉及到的化学反应方程式为 。
(2)运用质量守恒定律,可以算出题中放出二氧化碳的质量为 g。
(3)计算反应后溶液中溶质的质量分数(写出详细的计算过程,数据精确到l%)。
为测定石灰石中碳酸钙的质量分数,化学兴趣小组的同学设计了以下方案:将
稀盐酸加入到
石灰石样品中,恰好完全反应。生成的二氧化碳气体全部用足量的
溶液吸收,
溶液增加的质量随时问变化如下表:(友情提示:石灰石中的杂质不参加反应且难溶于水)

求:
(1)最终生成
的质量;
(2)样品中
的质量分数(计算结果精确到
);
(3)将石灰石与稀盐酸反应后的剩余物质进行过滤,再向滤液中加入多少克水可以得到
的
溶液。
向
和
的混合溶液中,逐滴加入
溶液。滴加
溶液的质量与生成沉淀的质量关系如下图,结合下图回答问题:
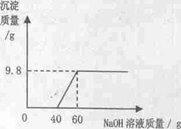
(1)写出生成沉淀的化学方程式:
(2)通过图像你能获得哪些信息(只答两点)。
①②
小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取l0g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是(温馨提示:杂质不参加反应)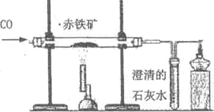
| A.玻璃管中的固体由黑色逐渐变成红色 |
| B.实验中通入CO的质量为4.2g |
| C.生成CO2的质量为2.4g |
| D.铁矿石样品中Fe2O3的质量分数为80% |
现有一瓶硫酸溶液,为测定其溶质的质量分数,取该溶液98g于烧杯中,逐渐加入足量的氯化钡溶液,反应中物质间的质最关系如右图所示。请计算:
(1)原硫酸溶液中溶质的质量分数。
(2)若取一定量该硫酸溶液配制509溶质的质量分数为7%的稀硫酸,需加人水的质量是多少?

某化工厂生产的纯碱产品中含有少量氯化钠杂质,为测定该产品中含碳酸钠的质量分数,某课外兴趣小组进行了以下实验。取一定质量的该纯碱样品于试管中,加入85. 6g稀盐酸,恰好完全反应,产生8.8g气体。经测定,所得溶液常温下为不饱和溶液,溶液中含钠元素的质量为10. 0g。请你据此分析计算:
(1)该产品中碳酸钠的质量分数是。
(2)反应后所得溶液中溶质的质量分数。
某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗
溶液80
,洗涤后溶液呈中性。(反应的化学方程式为:
)
请计算:
(1)这一定量石油产品中含
的质量。
(2)若所用的氢氧化钠溶液是用40%的氢氧化钠溶液稀释而成,则稀释过程中需要加水的质量。
计算题(共6分) 相对原子质量:Fe:56 C:12 O:16
我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为: 3CO+ Fe2O3高温2Fe + 3CO2 。用含Fe2O360%的赤铁矿石800t,理论上可炼出纯铁多少吨?
16g Fe2O3与184g稀H2SO4恰好完全反应,求所得Fe2(SO4)3溶液的溶质质量分数。
已知氯化钠溶液和硝酸银溶液反应生成氯化银(
)沉淀和硝酸钠。为测定某生理盐水的溶质质量分数,将生理盐水样品与足量的硝酸银溶液混合,有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实验数据 | 生理盐水样品的质量 | 加入硝酸银溶液的质量 | 过滤后剩余溶液物质量 |
| 130 | 40 | 167.13 |
(1)反应后生成氯化银的质量为
。
(2)计算该生理盐水的溶质质量分数。
某课外活动小组利用稀硫酸测定粗锌中纯锌的含量。现称取粗锌20
,加入到足量硫酸溶液中充分反应(杂质不参与反应),测得数据如下表:
| 时间/ | 0 | 3 | 6 | 9 |
| 粗锌及溶液总质量/ | 150.4 | 150.2 | 150.0 | 150.0 |
(1)计算反应过程中产生氢气的质量。
(2)根据表中数据计算粗锌中锌的质量分数。
纸包皮蛋是一项新技术,制作过程中需要配制料液。某配方料液中含
、
、红茶末、五香粉等,技术员先配得
、
的混合液2400g,其中含80g
,81g
。计算:
(1)混合液中
的质量分数。
(2)如果取24g混合液,加入一定质量
的稀盐酸恰好完全反应,计算所加稀盐酸的质量。
(3)24g混合液与稀盐酸反应后所得溶液中
的质量分数。
为测定某石灰石样品中碳酸钙的含量,取样品l0.0克于烧杯中再向其中加入稀盐酸50.0克,恰好完全反应(杂质不反应),反应后烧杯中物质总质量为56.7克。
(1)生成
的质量。
(2)求石灰石样品中碳酸钙的质量分数(写出计算过程)。
有 和 混合物l8.6g。为测定其中 的质量,将固体溶于水,并逐渐加入稀硫酸至100g时,开始产生气体;再加入稀硫酸至100g时,不再产生气体,生成气体共4.4g(提示: )
(1)在图28中画出产生气体的质量与所加稀硫酸质量的关系曲线。
(2)求混合物中
的质量是多少?
(3)所用稀硫酸的溶质质量分数是多少?

在用稀盐酸和氢氧化钡溶液进行中和反应实验时,反应过程中溶液酸碱度变化及相关数据如图20所示。

(1)根据此变化曲线,你认为实验操作是将滴加到另一种溶液中
(2)当加入溶液的质量是a克时,滴入无色酚酞试液,溶液呈色,此时溶液中溶质是(写化学式)
(3)求恰好完全反应时溶液中溶质的质量(需写出计算过程)