在密闭容器中盛有6克碳和18克氧气,加热使它们充分反应后,容器内的气体是
| A.CO2和O2 | B.CO | C.CO2和CO | D.CO2 |
将m1g碳与m2g氧气置于密闭容器中,在一定条件下充分反应,恢复至常温,若此时密闭容器中的气体是纯净物,则m1∶m2不可能是
| A.1∶1 | B.1∶2 | C.3∶4 | D.3∶8 |
有氮气、一氧化碳和二氧化碳的混合气体40g,其中碳元素的质量分数为30%。使该混合气体通过足量的灼热氧化铜充分反应后。再将气体通入过量的石灰水中,能得到白色沉淀的质量为
| A.30g | B.50g | C.100g | D.150g |
“热重分析法(TG)”是利用程序控制温度测量物质质量与温度关系的一种技术。用TG法研究一水合草酸钙(CaC2O4•H2O)的热分解产物时,随温度升高依次发生如下反应:CaC2O4•H2O CaC2O4+H2O↑;CaC2O4
CaC2O4+H2O↑;CaC2O4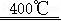 CaCO3+CO↑;CaCO3
CaCO3+CO↑;CaCO3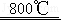 CaO+CO2↑现取29.2g CaC2O4•H2O,用TG法加热一段时间后冷却,测得剩余固体中钙的质量分数为33.7%.下列关于剩余固体成分的判断中正确的是( )
CaO+CO2↑现取29.2g CaC2O4•H2O,用TG法加热一段时间后冷却,测得剩余固体中钙的质量分数为33.7%.下列关于剩余固体成分的判断中正确的是( )
A.只有CaC2O4B.CaC2O4•H2O和CaCO3
C.CaCO3和CaOD.CaC2O4和CaCO3
烧杯中盛有一定质量的FeO和Fe 2O 3的固体混合物,向其中加入100g质量分数为7.3%的稀盐酸,恰好完全反应,得到107g该温度下的不饱和溶液。下列数据中,与原固体混合物中铁元素的质量分数最接近的是( )
| A. |
77.1% |
B. |
73.9% |
C. |
70.0% |
D. |
56.0% |
现有铜和氧化铜的混合物22.4g,加入某质量分数的稀盐酸至恰好完全反应,所用稀盐酸质量100g,将反应后的固液混合物过滤,得到滤液116g,则该混合物中铜元素的质量分数为
| A.28.6% | B.85.7% | C.87.5% | D.71.4% |
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是()

| A. | 生成 的质量: |
| B. | 参加反应的 的质量: |
| C. | 参加反应的 的质量: |
| D. | 参加反应的镁和氧气的质量比 |
称取12.5g石灰石(主要成分是CaCO3,杂质不参加反应)放人烧杯中,向其中加入50g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算石灰石中杂质的质量分数。
取一定量Fe2O3与Al2O3的混合物,加入含溶质9.8 g的稀硫酸,恰好完全反应。原混合物中氧元素的质量是
| A.0.8 g | B.1.6 g | C.3.2 g | D.6.4 g |
Fe2O3、ZnO、CuO的固体混合粉末a克,在加热条件下用足量CO还原,得到金属混合物2.41克,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00克白色沉淀,则a的数值为
| A.7.41 | B.3.59 | C.3.21 | D.2.46 |
某气体样品可能含有NO、N2O5、NO2中的一种或几种,经实验测定该样品中,氮、氧两种元素的质量比为7:16。其样品的组成不可能是
| A.NO、NO2和N2O5 | B.N2O5和NO |
| C.N2O5和NO2 | D.NO2 |
钢铁是使用最多的金属材料.
(1)利用一氧化碳与氧化铁反应,要制得5.6
铁,最少需要多少克一氧化碳?
(2)现有一种铁碳合金,其中的碳元素全部以
的形式存在,且合金中
的质量分数为36%,计算合金中碳的质量分数,并判断该合金属于生铁还是钢.
取7.8g锌与铜的混合物与49.0g稀硫酸恰好完全反应,产生氢气的物质的量与时间关系如图所示。
①计算样品中所含锌的质量 (20) (根据化学方程式列式计算);
②反应后溶液中溶质的质量分数为 (21) (计算结果精确到0.1%)。
向盛有碳酸钙粉末的试管中加入足量的稀盐酸,完全反应后共收集到 二氧化碳气体,试计算反应消耗的碳酸钙的质量.