工业上常用废铜屑跟热的稀硫酸和氧气反应制取硫酸铜:2Cu + O2 +2H2SO4=2CuSO4 + 2H2O
现将25.6t废铜屑和368t热的稀硫酸混合,通入足量的氧气,恰好完全反应。试计算:
(1)参加反应的氧气有多少吨?
(2)可制得无水硫酸铜多少吨?
(3)反应后溶液中CuSO4的质量分数。
取镁、碳酸镁组成的固体混合物20.4g,放入325g稀硫酸中,恰好完全反应,得到5.4g气体和溶质质量分数为20%的溶液,则原固体混合物中镁元素的质量为
| A.4.8g | B.9.6g | C.13.6g | D.16.8g |
某化工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢
氧化钠溶液40g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4质量是多少?
(5分)某化学实验小组要测定一种纯碱样品中碳酸钠的含量,并用一定溶质质量分数的稀硫酸进行实验,记录实验数据如下(样品中杂质不含钠元素、不溶于水也不与硫酸反应)
| |
第一次 |
第二次 |
第三次 |
| 加入的稀硫酸的质量(g) |
100 |
100 |
100 |
| 加入的样品的质量(g) |
20 |
40 |
42 |
| 生成气体的质量(g) |
2.2 |
4.4 |
4.4 |
(1)写出实验中发生反应的化学方程式 ;
(2)根据已知条件列出求解第三次参加反应的纯碱的质量(x)的比例式 ;
(3)将第二次实验所得的溶液蒸发掉6.2g水,所得不饱和溶液中溶质的质量分数为 ;
(4)若配制实验中所用稀硫酸200g,需要用溶质质量分数为98%的浓硫酸的质量为 ;
(5)这种纯碱样品中碳酸钠的质量分数为 。
将1.5 g混有铜粉的镁粉投入100g11.76%的稀硫酸中,至不再产生气泡为止,共收集0.1 g气体。过滤后,向所得溶液滴入质量分数为10%的氢氧化钠溶液。开始滴入时无沉淀生成,滴加一定质量的氢氧化钠溶液后开始出现白色沉淀。当滴加氢氧化钠溶液的质量为80g时,恰好得到最多的沉淀量2.9 g。试求:
(1)原混合物中镁的质量分数;
(2)最终所得溶液中溶质的质量分数。(计算结果保留至0.01%)
(3)请画出平面直角坐标图:要求以氢氧化钠溶液的质量为横坐标,产生沉淀的质量为纵坐标,并且标示出起点、折点的坐标
现有一定质量的甲烷不完全燃烧,生成一氧化碳、二氧化碳和水蒸气的混合气体75g,经测定混合气体中碳元素的质量分数为16%,则参加反应的氧气的质量是
| A.48g | B.56g | C.59g | D.64g |
将m1g碳与m2g氧气置于密闭容器中,在一定条件下充分反应,恢复至常温,若此时密闭容器中的气体是纯净物,则m1∶m2不可能是
| A.1∶1 | B.1∶2 | C.3∶4 | D.3∶8 |
现有铜和氧化铜的混合物22.4g,加入某质量分数的稀盐酸至恰好完全反应,所用稀盐酸质量100g,将反应后的固液混合物过滤,得到滤液116g,则该混合物中铜元素的质量分数为
| A.28.6% | B.85.7% | C.87.5% | D.71.4% |
化学实验课上,老师为每组同学分别提供了一瓶氢氧化钠溶液,让他们用1%的稀盐酸(密度为1.1g/mL)来测定其溶质的质量分数。甲组同学的实验如图1所示:在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,溶液pH的变化如图2所示.请回答
(1)a点溶液中大量存在的离子有__________
(2)b点溶液中的溶质有__________________
(3)计算氢氧化钠溶液中溶质的质量分数。(保留一位小数)
化学小组同学欲测定某NaCl和Na2SO4固体混合物中NaCl的质量分数,其实验操作及所得数据如下:将一定质量的该固体混合物完全溶于100g水中,加入一定溶质质量分数的BaCl2溶液117g恰好完全反应,过滤,得到23.3g沉淀和溶质质量分数为10%的滤液。请计算: 原固体混合物中NaCl的质量分数。
向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20﹪的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示。请回答:
(1)OA段无沉淀产生,请写出反应的化学方程式 ;
(2)加入镁粉的质量为 g;
(3)求产生氢气的质量是多少g?(写出计算过程,保留小数点后一位)。
取一定量Fe2O3与Al2O3的混合物,加入含溶质9.8 g的稀硫酸,恰好完全反应。原混合物中氧元素的质量是
| A.0.8 g | B.1.6 g | C.3.2 g | D.6.4 g |
为测定某盐酸的质量分数:往20g40%的氢氧化钠溶液的烧杯中逐滴加入该盐酸,加入盐酸的质量与烧杯中溶液pH的变化关系如图所示。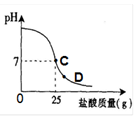
①所用氢氧化钠溶液中溶质的质量为 (8) g;
②当滴加盐酸到图像中D点时,烧杯中溶液的溶质是 (9) (填化学式);
③计算该盐酸的质量分数是多少?(根据化学方程式列式计算)(10)
为测定实验室中某过氧化氢溶液的溶质质量分数,取100.0g过氧化氢溶液放入小烧杯中,然后进行如图所示的实验.请计算:
①反应后产生气体的物质的量 ⑴ 。
②该过氧化氢溶液的溶质质量分数 ⑵ 。(请根据化学方程式列式计算)
将6.8 g含杂质的锌粒,加入到盛有50.0g过量的稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为56.6 g。试计算
(1)生成的气体的化学式是______________;其质量为______________ g。
(2)锌粒中所含锌的质量分数(精确到0.1%)。