天津市河北区初三总复习质量检测(一)化学试卷
用“王水”(浓盐酸与浓硝酸的混合物)溶解黄金后得到一种物质:HAuCl4(四氯合金酸)其中金元素(Au)的化合价为
| A.+1 | B.+2 | C.+3 | D.+4 |
厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生。这种气体是
| A.二氧化碳 | B.二氧化硫 | C.氢气 | D.氧气 |
下列说法正确的是
| A.原子是不可再分的粒子 |
| B.分子是保持物质性质的最小粒子 |
| C.分子、原子都能构成物质 |
| D.相对原子质量就是原子的实际质量 |
下表为人体内几种体液或代谢产物的正常pH范围,其中碱性最强的是
| 体液 |
A.胃液 |
B.尿液 |
C.血液 |
D.小肠液 |
| pH |
0.8~1.5 |
5.0~7.0 |
7.4~7.5 |
7.8~8.0 |
下列物质的性质与用途对应关系正确的是
| A.氧气能支持燃烧,可用于医疗急救 |
| B.氢氧化钙显碱性,可用于中和胃酸过多 |
| C.氢氧化钠固体易吸水潮解,可用于干燥二氧化碳 |
| D.二氧化碳固体(干冰)升华吸热,可用于人工降雨 |
下列实验方案的设计中,不正确的是
| A.用适量氢氧化钙除去氯化钠溶液中少量的碳酸钠 |
| B.用适量稀硫酸清除铁制品表面的铁锈 |
| C.用灼烧法鉴别羊毛纤维和棉纤维 |
| D.用足量稀盐酸检验久置的氢氧化钠固体是否变质 |
从金银花中提取的绿原酸(其化学式为C16H18O9)有很高的药用价值。下列有关绿原酸的说法正确的是
| A.绿原酸属于混合物 |
| B.绿原酸相对分子质量为354 |
| C.绿原酸中氧元素的质量分数最高 |
| D.绿原酸中碳、氢元素的质量比为16︰18 |
下图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子。下列说法中不正确的是
A.图中能表示氢分子的是 |
| B.该反应中共涉及四种分子和三种原子 |
| C.化学反应前后各元素化合价都不变 |
| D.化学反应前后原子种类和个数均不变 |
正确观察和描述实验现象是学好化学的因素之一,下列说法中不正确的是
| A.镁条在空气中燃烧,发出耀眼的白烟 |
| B.硫在氧气中燃烧,产生明亮的蓝紫色火焰 |
| C.一氧化碳在空气中燃烧发出淡蓝色火焰 |
| D.细铁丝在氧气中剧烈燃烧,火星四射,有黑色固体生成 |
下表列出了除去物质中所含少量杂质的方法,其中错误的是
| |
物质 |
杂质 |
除去杂质的方法 |
| A |
CaO |
CaCO3 |
加入足量的水溶解、过滤 |
| B |
NaOH溶液 |
Na2CO3 |
加入过量的Ca(OH)2溶液,过滤 |
| C |
Cu(NO3)2溶液 |
AgNO3 |
加入过量的铜粉,过滤 |
| D |
CO |
CO2 |
通过NaOH浓溶液,干燥 |
为了探究实验室中久置的生石灰样品变质情况,同学们进行如下图所示的实验。下列分析和结论不正确的是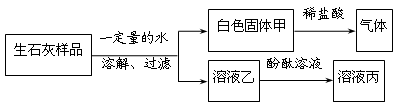
| A.溶液丙呈红色 |
| B.该样品中一定含有碳酸钙 |
| C.固体甲可能为Ca(OH)2和CaCO3的混合物 |
| D.该样品已完全变质 |
化学与生活息息相关,现有以下常见的物质:
| A.小苏打 |
| B.葡萄糖 |
| C.熟石灰 |
| D.纤维素 |
E.硝酸钾
F.甲烷
选择相应物质的字母进行填空。
(1)可用于改良酸性土壤的是 ;
(2)棉、麻等天然植物纤维的主要成分是 ;
(3)焙制糕点所用的发酵粉的主要成分之一是 ;
(4)属于复合肥料的是 ;
(5)淀粉等糖类物质在人体内水解变成 后,才能被人体吸收;
(6)天然气的主要成分是 。
下面是钠元素和氯元素在元素周期表中的信息和三种粒子的结构示意图。请回答下列问题:
(1)氯原子的电子总数是______;钠原子与氯原子的最本质区别是 。
(2)在钠和氯气生成氯化钠的反应中,得到电子的是 原子(填字母,下同);Na+的结构示意图是 。
化学是研究物质的组成、结构、性质及其变化规律的基础自然科学,请回答下列问题:
(1)①从组成角度看:水是由 组成的。
②从微粒角度看:水是由 构成的。
③从资源角度看:水是生命之源,下图是用来净化河水的简易装置,下列说法错误的是 。
A.利用上图装置能把硬水变为软水
B.通过过滤可以除去水中所有的杂质
C.利用上图装置能对水杀菌消毒
④从变化角度看:水通电分解能生成最理想的能源 气,电解一定量的水,当其中一个电极产生5 mL气体时,另一电极产生的气体体积可能是 mL。
(2)水是很好的溶剂。下图是KNO3和KCl在不同温度时的溶解度,回答下列问题:
①t1℃时,两物质中溶解度较大的是 。
②t2℃时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较多的是 的溶液。
③t2℃时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的 (填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数 (填“变大”或“不变”或“变小”)。
④欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是 。
A、D均为黑色固体(D为常见金属),B为稀硫酸,D、E、F均为单质。下图为这些物质的转化关系,其中部分反应物、生成物、反应条件已省略。
(1)请写出下列物质的化学式: E ;F 。
(2)反应④除了生成E,另一生成物的化学式为 ,该反应的基本类型是 。
(3)写出反应①和反应③的化学方程式 , 。
金属在日常生活中随处可见,研究金属的性质可以更好地利用金属。
(1)下列生活用品中,主要利用金属导热性的是 (填序号)。
(2)“淬火”是金属热处理常用的方法。宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,该反应的化学方程式为 。
(3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有 。
(4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等。下列做法与此结果相符的是 (填序号)。
| A.相同质量的三种金属与足量的稀盐酸反应 |
| B.2.4 g镁、6.5 g锌、5.6 g铁与足量的稀盐酸反应 |
| C.向足量的镁、锌、铁中加入稀盐酸的质量比为2︰3︰2 |
| D.足量的三种金属与等量的稀盐酸反应 |
下图为实验室常见的一些实验装置,请根据图回答下列问题:
(1)写出实验仪器①、②的名称① ② 。
(2)用氯酸钾和二氧化锰混合物制取氧气,该反应的化学方程式是 ,若制取较干燥的氧气应选用的实验装置是 (填序号)。
(3)用锌和稀硫酸制取氢气,所选用的实验装置是 (填序号),该反应的化学方程式是 。
在实验室配制溶液时,常涉及以下过程:①溶解 ②称量 ③计算 ④装瓶存
放。请回答问题:
(1)现欲配制50g 5%氯化钠溶液,配制过程的先后顺序是 (填序号)。
(2)用已调节平衡的托盘天平称取氯化钠固体时,发现指针偏右,接下来的操作是 。
(3)要配制245g质量分数为10 %的稀硫酸,需要溶质质量分数为98%的浓硫酸 g,在浓硫酸稀释过程中,一定要把 沿器壁慢慢注入 里,并不断搅拌。
硬水受热后会产生水垢,水垢的主要成分是CaCO3和Mg(OH)2。 实验室由水垢制取纯净CaCl2固体的流程如下:
请按要求填空:
(1)酸A是人体胃酸的主要成分,酸A的化学式是 ;
(2)步骤①中生成气体的化学反应方程式是 ;步骤②中生成沉淀的化学反应方程式是 ;
(3)步骤④加适量酸A的作用是 ;
(4)步骤⑤是利用 的方法得到氯化钙固体。
人体摄入锌不足会引起多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌口服液来补锌。已知葡萄糖酸锌的化学式为Cl2H22O14Zn。填空:
(1)葡萄糖酸锌相对分子质量为 ;
(2)葡萄糖酸锌中锌元素的质量分数为 ;
(3)现有一支20mL的葡萄糖酸锌口服液,其中含葡萄糖酸锌45 mg,那么这支口服液中锌的质量是 mg。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号