绘制知识网络是化学学习的一种有效方法,元素单质及其化合物的“价态—类别”二维图就是其中的网络图之一。如图是铁及其化合物的“价态—类别”二维图,下列有关说法或方程式正确的是( )
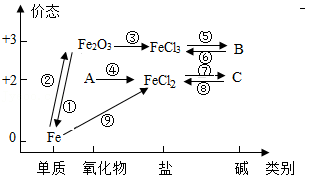
A.物质A的名称是氧化铁
B.①反应可能是Fe2O3+3Al 3AlO+2Fe
3AlO+2Fe
C.⑤反应可能是FeCl3+3NaOH═Fe(OH)3↓+3NaCl
D.⑤~⑨全部是复分解反应
A~E五种初中常见物质的部分转化关系如图。其中A与C的组成元素相同,B能使带火星的木条复燃,D是一种极易与血红蛋白结合的有毒气体,加热时D、E均能与黑色固体丙反应。回答下列问题:
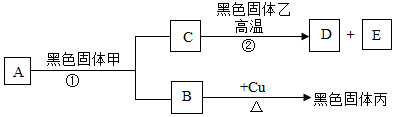
(1)黑色固体甲的化学式为 。反应①属于基本类型中的 反应。
(2)在D与丙的反应中,D表现出 性。
(3)反应②的化学方程式为 。
古诗《石灰吟》:“千锤万凿出深山,烈火焚烧若等闲。粉身碎骨浑不怕,要留清白在人间。”中蕴含了如图所示三种物质间的相互转化关系,下列说法不正确的是( )
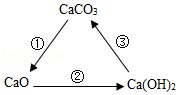
A.CaO俗名叫生石灰,是一种氧化物
B.“烈火焚烧若等闲”描述的是反应①的变化
C.反应②发生时,会放出热量
D.反应③是改良酸性土壤的原理
某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图所示(部分产物略去)
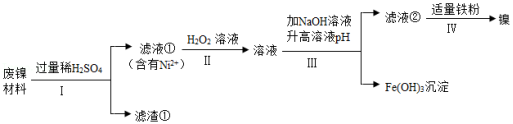
查阅资料:a.H 2O 2溶液可将Fe 2+转化为Fe 3+。
b.Fe 3+、Ni 2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)步骤Ⅰ的操作为 。
(2)滤渣①的成分为 。
(3)单质Fe参与反应的化学方程式为 (任写一个)。
(4)滤液②中有Ni 2+、无Fe 3+,则滤液②pH可能为 (填序号)。
A.pH=1
B.pH=2
C.pH=6
D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为 。
“垃圾是放错的资源”。碘循环工艺不仅能吸收SO2,减少环境污染,而且还可以得到仅含一种元素的化工原料X,流程如图所示:

(1)流程中可循环利用的物质是 。
(2)膜反应器中发生的是分解反应,X的化学式是 。
(3)反应器中发生反应的化学方程式为 。
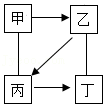
如图所示甲、乙、丙、丁四种物质间相互关系中的反应,均为初中化学常见反应("一"表示相连的两种物质能反应,"→"表示通过一步反应能实现转化),下列选项符合图示关系的是( )
| 选项 |
甲 |
乙 |
丙 |
丁 |
| A |
H 2O |
O 2 |
CaO |
Ca(OH) 2 |
| B |
H 2SO 4 |
HCl |
MgCl 2 |
Mg(OH) 2 |
| C |
HCl |
CO 2 |
CaCO 3 |
H 2O |
| D |
FeSO 4 |
FeCl 2 |
Cu |
CuO |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
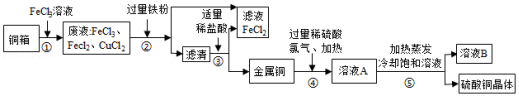
电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),如图是某兴趣小组设计的处理该生产过程中产生废液的流程图,据如图回答下列问题:
查阅资料:2Cu+2H2SO4+O2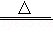 2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是 (写化学式)。
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是 ,步骤②还需要进行的实验操作是 。
(3)步骤③加入适量稀盐酸充分反应。当观察到 现象时,说明滤液中只剩下铜。
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用,根据质量守恒定律可推测该单质是 。
(5)溶液B中含有的溶质是 。
2021年6月8日是第13个“世界海洋日”。烟台有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图。据如图回答:
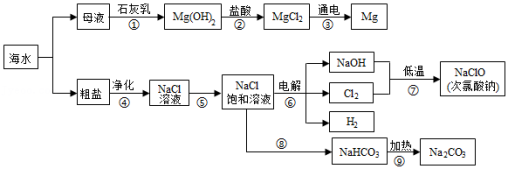
(1)海水制镁,步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。
(2)海水晒盐。通常采用 (填“降温”或“蒸发”)结晶的方法使海水中的氯化钠析出。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是 。
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质是 (写化学式)。步骤⑨中发生反应的化学方程式是 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式是 。
某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如图所示:
请回答下列问题:
(1)工厂废液中加入过量A反应的化学方程式为 。
(2)用化学式表示固体甲的成分 。
(3)溶液甲中的金属离子是 (用离子符号表示)。
(4)完成步骤④的化学方程式:4Fe(OH)2+O2+2 ═4Fe(OH)3。
海水是一种重要资源,利用海水可制取镁等物质,某化学兴趣小组的同学设计了如下实验流程进行实验:
分析该流程图,下列说法错误的是( )
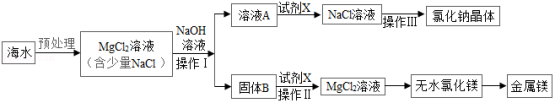
A.操作Ⅰ,操作Ⅲ都需用到的玻璃仪器是玻璃棒
B.固体B是Mg(OH. 2,试剂X是盐酸
C.加入NaOH溶液应过量,其目的是使MgCl 2完全反应
D.处理等量海水,若将NaOH溶液换成石灰乳,既能节约成本又能提高镁的产量
如果将物质按单质、氧化物、酸、碱、盐、有机物分类,如图中甲、乙、丙、丁是四种不同类别的物质,且相连物质之间均能发生化学反应。下列说法符合图示要求的是( )
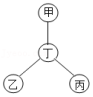
| A. |
当甲、乙、丙分别为酸、碱、盐时,丁可以为碳酸钠 |
| B. |
当甲为氯化铜时,丁可以为氢氧化钠 |
| C. |
当丁为氧气时,甲、乙、丙可以为红磷、甲烷、一氧化碳 |
| D. |
当丁为盐酸时,甲、乙、丙可以为铜、硝酸银、氢氧化钙 |
氢基熔融冶金技术是利用氢作为还原剂代替碳还原剂,从而实现减少CO2排放的目的,实现低碳冶金。氢基熔融还原生产高纯铸造生铁的主要流程如图所示(部分略去)。
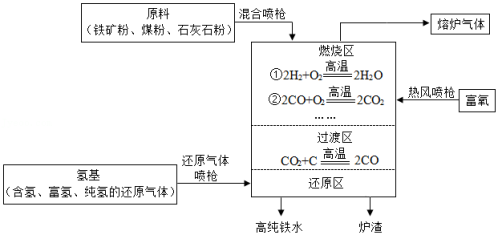
(1)燃烧区的作用是 ,燃烧区发生燃烧反应的物质还有 (填化学式)。
(2)还原区的反应除3CO+Fe2O3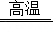 2Fe+3CO2,另一主要反应的化学方程式是 。
2Fe+3CO2,另一主要反应的化学方程式是 。
(3)从环境保护角度,与高炉炼铁技术相比,氢基熔融冶金技术的优点是 。
下列物质间的转化关系,不能实现的是( )
A.C→CO2→COB.Mg→MgO→MgSO4
C.KCl→KNO3→K2SO4D.NaOH→Na2CO3→NaCl
海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图(如图)回答问题:
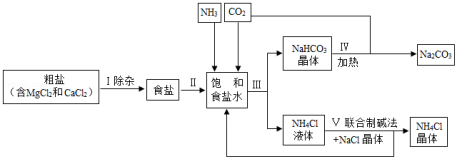
(1)步骤Ⅰ除杂中,常见的方法有两种:一是物理方法,即用NaCl溶液浸洗粗盐,溶解除去其中的可溶性杂质,则浸洗溶液应选用NaCl的 (填“饱和”或“不饱和”)溶液;二是化学方法,操作步骤依次为:加水溶解→加过量试剂①→加过量试剂②→过滤→加适量盐酸,以下试剂①②组合选用合理的是 。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步骤Ⅲ先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,写出步骤Ⅲ反应的化学方程式 。
(3)步骤Ⅳ发生的反应属于 反应(填基本反应类型)。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥