我国早在西汉时期,在《淮南万毕术》一书中就写到“曾青得铁则化为铜”,意思是可溶性的铜的化合物与铁发生反应得到单质铜。
(1)上述湿法冶金所发生的化学反应,其基本类型是 反应,发生这类反应的基本条件之有两个,条件一是参加反应的金属单质其活泼性必须比化合态的金属的活泼性 (选填“强”或“弱”),从物质的溶解性角度看条件二是 。
(2)此法冶金与高炉炼铁比其优点有许多,试写出一条 。
(3)根据上述题意你能写出一个用湿法冶金的化学反应方程式吗? 。
随着炼铁技术的进步,对物质资源的综合利用是大势所趋。竖炉冶铁工艺流程如下图所示,根据下列流程图回答问题。

(1)该工艺的主要原料为氧气、 和 。
(2)赤铁矿与CO反应的化学方程式为 。
(3)在催化反应室中,化合价发生改变的元素是 。
(6分)请结合下列实验回答问题:
(1)甲图实验现象是 ,结论是 。
(2)乙图的实验目的是为了探究铁生锈的条件时需要 ,为达到此实验目右侧试管中的水要经过煮沸并迅速冷却后再倒入,依据的原理是 。
(3)丙图实验中为防止爆炸常采取的一条安全措施是 。
(4)实验前后分别用磁铁吸引玻璃管中的粉末,这样做的目的是 。
兰州市中山桥南侧的"将军柱"(铸造材质主要是铁),距今已有630年的历史,它与中山桥一起组成了"兰州铁桥"一景,近日"将军柱"商标获得国家批准。

(1)"将军柱"已出现较多锈迹,其主要原因是铁与等物质共同作用的结果。生活中常用稀硫酸除去铁制品表面的铁锈,其反应的化学方程式为。
(2)废旧金属的回收利用是保护金属资源的重要途径,请你再写一条保护和节约金属资源的有效方法或途径:。
(6分)“孔雀石”的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它是一种重要的铜矿石原料。小明欲从孔雀石中提炼出单质铜。
【查阅资料】(1)碱式碳酸铜加热易分解,其方程式为:Cu2(OH)2CO3加热2CuO+CO2↑+H20。
(2)向Cu2(OH)2CO3中加入足量的盐酸,固体完全溶解,有无色气体生成,写出此反应的化学方程式:(2分) 。
【设计方案】在实验室中以碱式碳酸铜、铁粉、稀盐酸为原料来制取单质铜。请你仿照下图画出方案二制取铜的流程图,要求:步骤最少。
方案一:
方案二:你设计的方案为 (2分)
【进行实验】方案一中最后一步:在溶液中加入过量的Fe的实验现象为
【反思】铜锈的主要成分也是碱式碳酸铜,从碱式碳酸铜的化学式[Cu2(OH)2CO3]推知,铜生锈可能与空气中的氧气、水、________________________有关。
金属在生活中随处可见。请回答下列问题。
(1)"一角"硬币的材料是铝合金。合金属于 (填"纯净物"或"混合物"),制造合金硬币不需要考虑的性质是 (填字母序号)。
| A. |
光泽好 |
| B. |
耐腐蚀 |
| C. |
能导电 |
(2)生活中铁制品比铜制品更容易锈蚀,这说明铁的金属活动性比铜 (填"强"或"弱")。将表面光洁的铁钉放入稀硫酸中会有气泡产生,该反应的化学方程式是 。
(3)下列做法不利于有效保护金属资源的是 (填字母序号)。
| A. |
回收废旧金属制品 |
| B. |
寻找金属的替代品 |
| C. |
加速开采矿物资源 |
金属材料在国防建设中起着量要的作用,图1为歼﹣15飞机在辽宁舰上起飞
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 。
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果,工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 。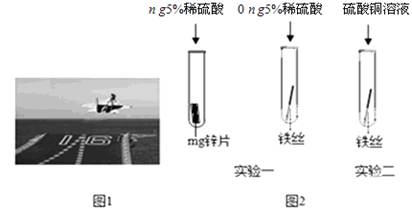
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是 。
②实验二中,若出现 现象,可证明铁的活动性强于铜,该反应的化学方程式为 。
某研究性学习小组利用下图装置探究温度对
还原
的影响(固定装置略)。
查阅资料:
;
溶液遇
溶液变红。
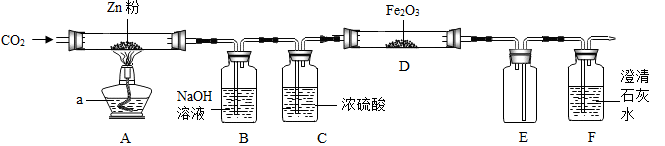
请回答下列问题:
(1)仪器
的名称是,装置
的作用是,尾气处理的方法是。
(2)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(纯净物)。两组分别用产物进行以下实验:
| 步骤 |
操作 |
甲组现象 |
乙组现象 |
| 1 |
取黑色粉末加入盐酸 |
溶解,无气泡,溶液呈浅黄绿色(含两种金属离子) |
溶解,有气泡,溶液呈浅绿色 |
| 2 |
取步骤1所得溶液,滴加
溶液 |
变红 |
无现象 |
则甲组步骤1中反应的化学方程式是,乙组得到的黑色粉末是。
(3)从安全考虑,本实验应在装置和之间添加装置
防止倒吸。(填字母编号)
(4)该对比实验结果表明
的还原能力随温度的升高而(填"增强"或"减弱")。
根据下图所示实验回答问题.
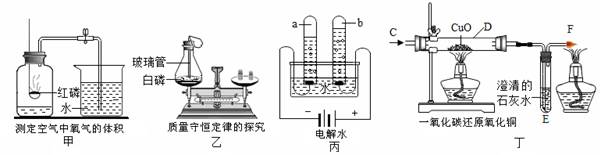
①甲实验:实验结束后,打开弹簧夹,烧杯里的水进入瓶中的原因是 ,若发现瓶内进入的水量明显小于1/5,其原因可能有
②乙实验:实验成功的关键因素你认为应该是 ,质量守恒的实质 ;
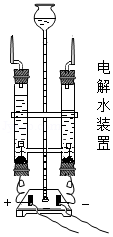
③丙实验:收集到氢气的试管是 (填“A”或“B”),电解时在水中加入少量硫酸钠的原因是:
④丁实验:加热前先通入CO的目的是 ;为确保实验得到亮红色的铜,当玻璃管D停止加热时,不需要断开D、E装置间的连接,原因是 ;
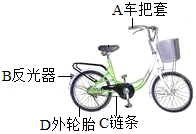
如图是人们经常使用的便捷交通工具﹣﹣自行车。请回答下列问题:
(1)所标各部件中由金属材料制成的是 (填字母),属于有机合成材料的有 (任选一种部件填字母)。
(2)生铁和钢都是铁的合金,其性能不同的原因是 。
(3)金属矿物储量有限,不可再生。保护金属资源的有效途径,除了防止金属锈蚀外,还有 (写一条即可)。
(4)将一定量的铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。则滤渣中一定含有 (填化学式),滤液中溶质的组成可能是 (填化学式)。
阅读下面的科普材料。
地球上的金属资源广泛存在于地壳和海洋中,除少数很不活泼的金属如金、银等有单质形式存在外,其余都以化合物的形式存在。陆地上存在各种各样的金属矿藏。
部分常见的金属矿石
矿石名称 |
赤铁矿 |
孔雀石 |
辉铜矿 |
铝土矿 |
白钨矿 |
图样 |
|
|
|
|
|
主要成分 |
Fe2O3 |
Cu2(OH)2CO3 |
Cu2S |
Al2O3 |
CaWO4 |
从矿石中制取金属单质的过程叫冶金,金属作为金属材料,其价值不仅取决于它在地壳中的含量和独特的性能,在很大程度上还取决于其冶炼的难易程度。例如铝是人们熟悉的金属,其蕴藏量居金属之首,应用广泛,但在1886年以前,它的价格比黄金还高,其原因是冶炼成本太高。目前工业冶炼铝的原理是:将铝土矿提纯后,在熔融状态下电解,生成铝和氧气。
早在春秋战国时期,我国就开始生产和使用铁器。从1世纪起,铁成了一种最主要的金属材料,工业上可利用一氧化碳还原赤铁矿制得金属铁。
金属除了有光泽、导电性、导热性、延展性等共同的物理性质外,还有各自的特性。例如,铁、铝等大多数金属都呈银白色,但铜呈紫红色;常温下大多数金属是固体,但汞是液体。
金属材料应用广泛。形状记忆合金是具有形状记忆效应的合金,人造卫星和宇宙飞船上的天线是由钛镍形状记忆合金制造的,它具有形状记忆功能,可揉成一团放入卫星或宇宙飞船舱内,需要时可在一定条件下恢复原来的抛物面形状。钛合金与人体具有很好的“相容性”,因此可以用来制造人造骨等。
人类每年要从自然界提取数以亿吨计的金属,但矿物的储量有限,因此,对金属资源的保护变得迫在眉睫。
回答下列问题:
(1)根据材料可知,工业上可以用 (填矿石名称)来冶炼金属钨。
(2)铝是地壳中含量最多的金属元素,1886年以前铝的价格比黄金还高的原因是 。
(3)根据材料,写出工业冶炼铝的化学方程式 。
(4)金属可以压成片,抽成丝,利用了金属的 性。
(5)根据材料可知, 合金可用来制造卫星或宇宙飞船的天线。
(6)保护金属资源的途径有:①防止金属腐蚀;② ;③合理开采矿物;④寻找金属代用品。
铬(Cr)是银白色有光泽的金属,含铬、镍的钢称为不锈钢,具有极强的抗腐蚀性。
(1)纯铁与不锈钢相比较,硬度较大的是 ;铁生锈的实质是铁与 共同作用的结果。
(2)已知铬能与稀盐酸反应生成+2价铬的化合物,请写出该反应的化学方程式 。
(3)请写出一条保护金属资源的有效措施 。
(1)初中化学关于研究物质组成的方法有多种,例如:
①化合法:适用于由两种单质发生的化合反应。如通过氢气与氧气反应生成水来研究水的组成,其化学方程式为 ;
②分解法:如通过电解水研究水的组成。如图装置中与直流电源正、负两极相连的玻璃管中生成的气体的质量比是 。运用上述两种方法研究水的组成,可知水是由氢、氧两种元素组成的。两种研究方法的理论依据是 。
③燃烧法:很多化合物燃烧有多种生成物,需通过定量研究来确定物质的组成。如: ____ (写出一种有机物燃烧的化学方程式)
(2)资源是人类最大的财富,请完善下列保护金属资源的途径。
①防止金属的腐蚀,如防止铁制品锈蚀的方法有 (填一条);除铁锈的化学方程式是 _____
②
③有计划合理的开采矿物,严禁不顾国家利益乱采矿,如对稀土的开采。
金属在生产、生活中起着重要重要.
(1)金属生锈是世界面临的难题,铁生锈实际上是铁与水、 共同作用的结果;
(2)家庭中自行车车架经常采用的防锈方法是 ;
(3)工业上采用赤铁矿石(主要成分是氧化铁)炼铁的反应原理是 (用化学方程式表示);
(4)金属的回收利用和防止金属的腐蚀,是保护金属资源的有效途径,请你再写出一条 。
某种氧化铜样品中混有少量木炭粉,为测定该样品中氧化铜的质量分数,某同学设计了如下装置进行实验(N2不参加反应,不考虑外界空气对实验的影响)。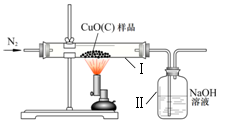
①该实验需要测定的量:反应前后装置Ⅱ的质量和 (9) 的质量
②充分反应后,装置Ⅱ的质量增加了0.44 g,则生成的二氧化碳的物质的量是 (10) mol。求参加反应的氢氧化钠的物质的量。(请根据化学方程式列式计算) (11)
③为达到实验目的,对反应前氢氧化钠溶液中溶质质量的要求是 (12) g。
④关于该实验的下列说法正确的是(13) 。
| A.当黑色粉末全部变为光亮红色时方可停止加热 |
| B.实验结束时先熄灭酒精喷灯会导致Ⅱ中液体倒流入Ⅰ中 |
| C.只称量反应前后装置Ⅰ中固体质量也可达到实验目的 |
| D.用氧气代替氮气完成实验也可达到实验目的 |