化学概念之间在逻辑上存在并列、交叉和包含等关系。下列各图中概念之间关系正确的是( )
A.
B.
C.
D.
下列关于溶液的说法正确的是( )
A.溶液一定是混合物
B.饱和溶液的浓度比不饱和溶液的浓度一定大
C.医用碘酒是碘的水溶液
D.添加溶质是不饱和溶液变成饱和溶液的唯一方法
物质世界的变化都遵循一定的规律。下列叙述中,不正确的是( )
A.水的天然循环是通过其三态变化实现的
B.一切化学变化都遵循质量守恒定律
C.物质发生化学变化时伴随着能量变化
D.某温度下的饱和溶液不能再溶解任何物质
硝酸钾的溶解度曲线如图所示。下列说法正确的是( )

A.氢氧化钙的溶解度曲线与硝酸钾相似
B.A、B、C三点对应的溶液均为饱和溶液
C.溶质的质量分数:A>B>C
D.从硝酸钾溶液中获得晶体的方法:蒸发浓缩、冷却结晶
如图是X、Y两种固体物质的溶解度曲线。下列叙述正确的是( )

A.温度低于t2℃时,物质Y的溶解度小于X
B.X、Y的溶解度都随温度升高而增大
C.a点表示t1℃时X、Y的溶液都不饱和
D.Y的饱和溶液降低温度后,溶质质量分数不变
t℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。回答下列问题:
(1)蒸发溶剂前, (填“甲”或“乙”)是饱和溶液;
(2)b点对应的乙溶液是 (填“饱和溶液”或“不饱和溶液”);
(3)t℃时, (填“甲”或“乙”)的溶解度更大;
(4)甲的饱和溶液的质量分数是 (用含m、n的代数式表示)。

在20℃时,某固体物质(不含结晶水)的水溶液,经历如图变化( )
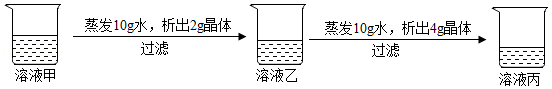
下列说法你认为正确的( )
A.溶液甲是饱和溶液
B.20℃时,该固体物质的溶解度是40g
C.溶液丙若蒸发10g水,析出的晶体一定大于4g
D.溶液乙溶质的质量分数小于溶液丙溶质的质量分数
甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是( )

| A. |
10℃时,甲的溶解度最大 |
| B. |
图中P点表示10℃时丙的饱和溶液 |
| C. |
20℃时,向130g乙的饱和溶液中加入20g水,乙的质量分数变为20% |
| D. |
50℃时,同质量的甲、乙、丙饱和溶液降温至10℃,丙溶液中析出固体最多 |
如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)P点表示的意义: 。
(2))t2℃时,A、B、C三种固体物质的溶解度大小顺序是: 。
(3)t2℃时,将60gA物质放入100g水中,充分溶解后,所得溶液是 (填“饱和溶液”或“不饱和溶液”),所得溶液的质量是 g。

如图是A、B、C三种物质的溶解度曲线,请认真分析并回答:
(1)t3℃时,A、B、C三种物质的溶解度由小到大的顺序为 。
(2)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃时变为不饱和溶液的是 。
(3)当A中含有少量的B,可采用 (填“降温”或“蒸发”)结晶的方法提纯A物质。
(4)t3℃时,若用A、B两物质各50g配成饱和溶液,则所需加水的质量A B(填“>”,“<”,“=”号)

甲、乙两种固体物质在水中的溶解度曲线如图所示。据图作答:
(1)甲、乙两物质的溶解度受温度影响较大的是 ;在0℃~t1℃之间时,相同温度下甲物质的溶解度 (填“>”“<”或“=”)乙物质的溶解度。
(2)t2℃时,把20g甲物质加入50g水中充分溶解,所得溶液为 (填“饱和”或“不饱和”)溶液,把该溶液降温到t1℃时,会析出甲物质 g。

如图,室温下,盛水的烧杯内放置两支分别盛有等质量KNO 3溶液和饱和石灰水的试管甲和乙,向烧杯内的水中加入NH 4NO 3固体后,甲中未观察到明显现象。下列说法正确的是( )

| A. |
乙中溶液一定变浑浊 |
| B. |
甲中溶液一定变成饱和溶液 |
| C. |
乙中溶液溶质的质量分数一定变小 |
| D. |
甲、乙中溶液质量一定相等 |
氯化钠是生产、生活中的一种重要化合物,应用很广泛。
Ⅰ.图甲和图乙分别是钠原子和氯原子的原子结构示意图。

(1)图甲中的x= 。
(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有 个电子的相对稳定的氯离子,氯离子用化学符号表示为 。
Ⅱ.如表是氯化钠在不同温度下的溶解度数据。
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
(1)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于
(填“饱和”或“不饱和”)溶液。
(2)医用盐水(溶质为NaCl)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其中含NaCl的质量为 g。
(3)学生化学实验活动之一:配制50g质量分数为6%的氯化钠溶液,该实验需要的仪器有药匙、托盘天平、玻璃棒、胶头滴管、 (从下列图中选择写出名称)。

Ⅲ.工业上常用电解饱和食盐水的方法来制取氢氧化钠、氯气和氢气,其化学反应方程式可表示为:xNaCl+yH2O zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
(填数字)。
NaHCO3在生产和生活中有许多重要用途,某学习小组对其性质进行了如下探究。物质的溶解度见下表。回答下列问题:
温度 |
10℃ |
20℃ |
NaHCO3的溶解度(g/100g水) |
8.1 |
9.6 |
Ca(HCO3)2的溶解度(g/100g水) |
16.6 |
(1)在20℃时称取4g NaHCO3加入46mL蒸馏水(密度取值为1g/mL),充分搅拌制得澄清溶液。该实验可以达到探究NaHCO3 性的目的;实验中不需要的仪器是 (选填字母编号)。

(2)用pH计测得溶液的pH为8.2,说明溶液呈 性。
(3)所配NaHCO3溶液的质量分数等于 ,降温到10℃时溶液 (填“是”或“不是”)饱和溶液。
(4)取2mL所配NaHCO3溶液于试管中,滴加5%的CaCl2溶液,观察到气泡和白色沉淀,实验证明该气体是CO2.据此小组同学讨论认为:白色沉淀不可能是Ca(OH)2,其理由是 ,于是得出结论:白色沉淀是 。
甲、乙、丙三种物质的溶解度曲线如图1所示。回答下列问题:

(1)当温度为 ℃时,甲、丙两种物质的溶解度相等。
(2)t3℃时,甲物质的饱和溶液中,溶质和溶液的质量比为 。
(3)若采用升温、恒温蒸发溶剂、增加溶质的方法都能使接近饱和的溶液变成饱和溶液,则该物质是 。
(4)R是甲,乙、丙三种物质中的一种,现用R作图2实验,①②中没有固体析出,③中有固体析出。根据图示信息,以下几种说法正确的是 (填标号)。

A.R是甲物质
B.①和②的溶液中,溶质质量相等
C.①②③中,只有③的上层清液是饱和溶液
D.①的溶液中溶质的质量分数比③的上层清液中溶质的质量分数小