某校同学以“探究常见金属与稀硫酸的化学性质”为课题进行实验探究。
【所用药品】溶质质量分数相同的稀硫酸,大小形状都相同的Al、X、Cu三种金属。
【实验记录】
| |
|
Al |
X |
Cu |
| 现象 |
开始时 |
几乎无气泡产生 |
产生气泡速度慢 |
无气泡产生 |
| 一段时间后 |
产生气泡速度快 |
产生气泡速度慢 |
无气泡产生 |
【分析与结论】
(1)实验开始时,铝表面几乎无气泡产生的原因是_____________________ ;
一段时间后,铝表面产生气泡且速度快,写出反应的化学方程式
据此,你认为该同学在操作实验时缺少的一个操作步骤是
⑵三种金属的化学性质由强到弱的顺序是____________ ______。
某兴趣小组为探究“氧化铁和铜粉”混合物中铜的质量分数,称取一定质量的混合物,按照右图实验装置进行实验: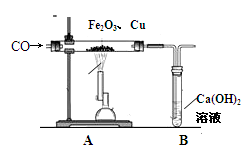
(1)实验时要“先通一氧化碳气体,后加热”的目的是 。
(2)装置A中发生反应的方程式为 。
(3)实验装置B中的现象是 ,发生反应的化学方程式为 。
(4)该装置的设计有一明显不当之处,你的改进方案是 。
[定量分析]
该兴趣小组按照科学的方案完成实验后,对充分反应后的管内固体X进行如下后续实验探究: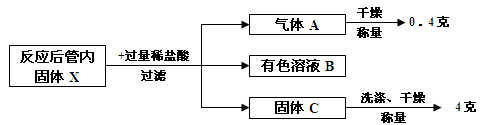
回答下列问题:
(1)写出固体X与稀盐酸反应的方程式: 。
(2)如何证明固体C已经洗涤干净? 。
(3)有色溶液B中含有的溶质: (填化学式)。
(4)根据以上实验流程,计算原混合物“氧化铁和铜粉”中铜的质量分数为 。
碱石灰是实验室常用的干燥剂。
[提出问题]
实验室中久置的碱石灰样品的成分是什么?
[进行猜想]
久置的碱石灰样品中可能含有CaO、NaOH、
Ca(OH)2、Na2CO3、CaCO3等成分。样品中可能含有Ca(OH)2、Na2CO3的原因是(用化学方程式表示) 、 。
[实验过程] 
试回答下列问题:
(1)操作①的名称是 。溶液C中加入酚酞的现象I为 。
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有 ,反应的方程式为 。
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是 。
[实验结论] 该久置的碱石灰样品中能确定一定含有的物质是 。(填序号)
| A.CaO | B.NaOH | C.Ca(OH)2 | D.Na2CO3E、CaCO3 |
对下列实验过程的评价,正确的是 ( )
| A.向某固体中滴加稀盐酸,有气泡产生,该固体一定是碳酸盐 |
| B.在无色溶液中滴入酚酞试液,溶液变红色,该溶液一定是碱溶液 |
| C.用小木棍蘸少量浓硫酸,小木棍变黑说明浓硫酸有吸水性 |
| D.燃着的蜡烛用烧杯罩住,火焰熄灭,说明燃烧一般需要氧气 |
下列“家庭小实验”可以达到实验目的的是( )
| A.用铅笔芯试验石墨的导电性 | B.用食盐水除去热水瓶中的水垢 |
| C.用淬火后的钢针做钓鱼钩 | D.用铜导线和食醋制氢气 |
课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3、还含有少量NaCl,其它杂质不计)和石灰乳(氢氧化钙的悬浊液)为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 ▲ 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
【粗产品成分分析】
(1)取适量粗产品溶于水,加入Ba(NO3)2溶液出现白色浑浊,发生反应的化学方程式为 ▲ ,该粗产品中一定不含有 ▲ ,理由是 ▲ 。
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
【粗产品含量测定】
Na2CO3含量的测定:
(1)该兴趣小组的同学设计了下图所示的实验装置。取20.0g粗产品,进行实验。
【说明】①碱石灰是CaO与NaOH的固体混合物。
②E装置中的饱和NaHCO3溶液是为了除去二氧化碳气体中的氯化氢,发生
的反应为:NaHCO3 + HCl = NaCl + CO2 ↑ + H2O。
(2)操作步骤
①连接好装置,检查气密性;
②打开弹簧夹C,在A处缓缓通入一段时间空气;
③称量G的质量;
④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;
⑤打开弹簧夹C,再次缓缓通入一段时间空气;
⑥再次称量G的质量,得前后两次质量差为4.8g。
(3)问题探究
①F中的试剂应为 ▲ 。
②B装置的作用是 ▲ ,H装置的作用是 ▲ 。
③若没有H装置,则测定的Na2CO3的质量分数会 ▲ (填“偏大”、“偏小”、“不变”)。
事实上20.0 g粗产品只能产生4.4 g CO2。请你仔细分析上述实验,解释实验值4.8g比正确值4.4 g偏大的原因(假设操作均正确) ▲ 。
(4)数据计算
根据正确值4.4 g可求得粗产品中Na2CO3的质量分数为 ▲ %。
NaOH含量的测定:
该小组同学又另取20.0g粗产品,逐滴加入20%的盐酸至恰好完全反应时,消耗盐酸的质量为73 g,放出CO2 4.4 g(不考虑二氧化碳气体的溶解)。求原粗产品中NaOH的质量分数。(写出计算过程)
2010年4月28日某媒体题为“排污工程施工,毒气放倒三人”的报道,引起
某兴趣小组同学的思考。
【提出问题】排污管道中的毒气有什么成分?
【查阅资料】
I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S, CH4等。
Ⅱ.H2S气体能与CuSO4溶液反应生成黑色沉淀,且能与碱溶液发生中和反应。
【提出猜想】小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、 H2S; 猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4; 猜想4:有CO2、H2S、 ▲ ;
猜想5:有CO、CO2、 H2S、CH4。
【实验方案】小组同学共同设计了下图所示的装置并进行探究(夹持仪器已省略)。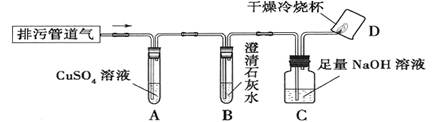
【问题讨论】
(1)如果A装置没有明显变化,则猜想 ▲ 成立;
(2)在验证猜想1的实验中,装置C中NaOH溶液的作用是 ▲ ;若要进一步验证气体燃烧后的产物,操作是:迅速把烧杯倒过来,向烧杯内注入▲ ,振荡。
(3)要确证猜想5中是否有CH4,某同学认为图示装置有不足之处,需要在装置C与D之间加一个 ▲ 装置。改进后,若气体燃烧,且D装置内壁出现 ▲ ,证
明气体中一定含有CH4。
下列描述正确的是
| A.化学反应前后元素的种类不变,原子的个数可能改变 |
| B.水受热变成水蒸气,说明了分子可以再分 |
| C.有单质生成的反应一定是置换反应 |
| D.能使酚酞试液变红的溶液不一定是碱溶液 |
某校研究小组的同学进行了下列实验:
【步骤1】用5个规格相同的塑料矿泉水瓶分别收集1瓶空气、1瓶CO2以及3瓶空气和CO2的混合气体(CO2含量分别为10%、20%、30%),并用带温度计的胶塞塞紧瓶口;
【步骤2】把上述装有气体的矿泉水瓶放到白炽灯下照射,每隔1分钟记录一次温度,实验数据记录如右表所示。请分析右表,回答下列问题:
(1)本次实验的目的是: ;
(2)根据本次活动的研究目的,该实验可以得出的结论有:_________________________。
(3)根据本次活动的上述数据推测,在相同条件下,当CO2含量为25%时,温度达到25.4℃需要的时间范围为 min。
下图是某同学设计的趣味实验装置,其气密性良好。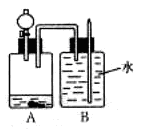
(1)若B中尖嘴导管出有“喷泉”产生,则A中的分液漏斗和集气瓶中分别盛放的物质可能是 、 ;
(2)若要使B中的水倒流入A中,A中的分液漏斗和集气瓶中可分别盛放的物质是 、 ;
某同学做了以下两个实验: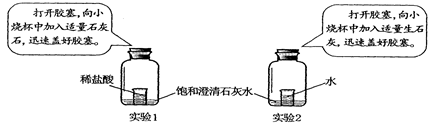
(1)实验1中澄清石灰水的现象是___________________,
产生此现象的原因是__ _______ _____________ ___________;
(2)实验2中澄清石灰水的现象是_______________________,
产生此现象的原因是___ ________ ___________。
物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙两位同学按下面的步骤进行探究: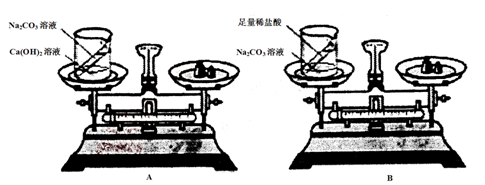
(1)提出假设:物质发生化学变化前后总质量不变。
(2)进行实验:甲同学设计的实验装置和选用药品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。
写出A、B两个实验发生反应的化学方程式:A、
B、 。
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
你认为导致乙同学实验结论错误的原因什么?
对实验现象的观察和分析,有助于获得化学知识并学会科学探究的方法。下列对实验现象的分析合理的是
| A.向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱溶液 |
| B.某白色固体与熟石灰研磨,产生的气体可使酚酞溶液变成红色,证明该固体是铵盐 |
| C.向某无色溶液中滴入氯化钡溶液,产生白色沉淀,证明该溶液是硫酸溶液 |
| D.把燃着的木条伸入某无色气体的集气瓶中,火焰熄灭,该气体不一定是二氧化碳气体 |
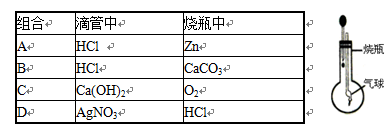
探究小组利用下图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )