主族元素W、X、Y、Z的原子序数依次增大,W原子最外层电子数是次外层的3倍,X,Y和Z分属于不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有二组分化合物中,由元素W、Y形成的化合物M的熔点最高。请回答下列问题:
(1)W原子L层电子排布式为 W3空间构形是
(2)X单质与水反应的主要化学方程式
(3)化合物M的化学式 其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是 。将一定是的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂酸醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有 ,O-C-O的键角约
(4) X、Y、Z可形成立方晶体的化合物,其晶胞中X占有棱的中心,Y位于顶角,Z位于体心位置,则该晶体的组成为X:Y:Z= 。
(5)含有元素Z的盐的焰色反应为 色,许多金属盐都可以发生焰色反应,其原因是
(6) ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm,密度为 g·cm-3(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为____________pm。

[化学选修5—有机化学基础]
药物菲那西洒汀的一种合成路线如下:

(1)菲那西汀的分子式 _____________________;
(2)①~⑥反应过程中在苯环上发生取代反应的是_____________________;
(3)反应②中生成的无机物的化学式为 _____________________;
(4)写出⑤反应的化学方程_____________________;
(5)菲那西汀水解的化学方程式是_____________________;
(6)菲那西汀的同分异构体中,符合下列条件的共有_______种;
①含苯环且只有对位两个取代基②苯环上含有氨基③能水解,水解产物能发生银镜反应
(7)菲那西汀的同分异构体中,含苯环且只有对位两个取代基,两个取代基含有相同碳原子数,且含 有α-氨基酸结构,写出这种同分异构体缩聚后高分子产物的结构简式_____________________。
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________、B___________、C____________、
F___________、H___________、乙____________。
(2)写出下列反应离子方程式:
反应①______________________
反应⑥_____________________
A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体、B为黄绿色气体、C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体。它们之间的转化如图所示(某些反应条件和部分反应产物已略去)。

(1)写出下列物质的化学式:D X 。
(2)在反应①~⑦中,不属于氧化还原反应的是 (填编号)。
(3)反应⑥的离子方程式为: 。
(4)往G溶液中加入NaOH溶液观察到的现象是 。
(5)反应⑦的化学方程式为 ;该反应中每消耗0.3mol的A,可转移电子 mol。
(6)除去D溶液中混有的少量G的方法是: 。
(1)X是最简单的烯烃。现有如下的反应关系:(已知F是一种常见的塑料)

①X的结构简式为 ;C的官能团名称是 。
②由E制取F的化学方程式为 。
(2)某实验小组用下列装置进行A转化为B的实验。

①请写出A制取B的化学反应方程式:___________________________。
②甲和乙两个水浴作用不相同。甲的作用是_____________;乙的作用是_____________。
③试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,要除去该物质,可在混合液中加入___(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
(3)阿斯匹林的结构简式为: ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为 。
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为 。
(4)某烃的分子式为C8H10,其不能使溴水褪色,但可使酸性KMnO4溶液褪色,且此烃与液溴在催化剂条件下只得到一种取代产物,其结构可能有 种。
| A.1种 | B.3种 | C.4种 | D.5种 |
已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个石油化工发展水平的标志。下列是有机物A~G之间的转化关系:
请回答下列问题:
(1)A的官能团的名称是________________;C的结构简式是________________;
(2)G是一种高分子化合物,其链节是______________;
(3)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27OC)进行应急处理。写出由A制F的化学反应方程式:____________________,决定F能用于冷冻麻醉应急处理的性质是___________________。
已知有如右图所示转化关系(反应条件略)。
已知;①X、Y、Z、W均为氧化物。常温下,X是红棕色气体;Y能使澄清石灰水变浑浊但不能使品红溶液褪色。②相对分子质量:甲<乙。③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。请完成下列空白:
(1)Z是(写化学式):______________。
(2)将乙的浓溶液露置在空气中一段时间,质量增加浓度降低,表明乙的浓溶液具有__________性。利用这种性质可以进行__________项(填字母)实验操作。
| A.钝化铁片 | B.检验Ba2+ | C.干燥氨气 | D.干燥氯气 |
(3)在X与Z的反应中,被氧化的X与被还原的X的物质的量之比是________________。
(4)W可用于工业制溴过程中吸收潮湿空气中的Br2,写出该反应的离子方程式:______________。该反应很好地解决了环保问题,但给工业生产带来了_______________的问题。
(5)写出M与甲的浓溶液在加热条件下反应的化学方程式:______________。
在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。回答下列问题:

(1) 写出反应②的化学反应方程式 ,在该反应中,每生成2.24LG(标准状况),该反应转移电子的物质的量是 。
(2)若反应①在溶液中进行,A、C、D均含氯元素,且A中氯元素的化合价介于C和D之间。则反应①的化学方程式是 。
(3)若反应①在溶液中进行,A是一种强酸,B是一种含两种金属元素的盐,当A过量时,C及D均易溶于水。则A过量时反应①的离子反应方程式是 。
【化学——选修5:有机化学基础】已知:苯和卤代烃在催化剂作用下可以生成烷基苯和卤化氢。根据以下转化关系(生成物中所有无机物均已略去),回答下列问题:

(1)H中所含官能团的名称是 ,E中所含官能团的结构式是 ,D的结构简式为 。
(2)①②③④⑤⑥反应中属于消去反应的是 。
(3)写出反应⑥的化学方程式 。写出H→I的化学方程式______________________________。
(4)写出符合下列要求的F的同分异构体的结构简式:
① F的同分异构体中属于酯类,能发生银镜反应,苯环上有两个取代基且苯环上的一氯代物只有两种: 。
② F的同分异构体中属于醇类,能发生银镜反应,苯环上有两个取代基且苯环上的一氯代物只有两种: 。(写出一种即可)
化合物A为一种常见金属元素与一种常见非金属元素组成的化合物,阳离子与阴离子的个数比为2:3。K为常见固态非金属单质,J为常见气态单质。其余为化合物,其中I、F在常温下为液态,C、D为刺激性气体,H无色无味气体,B为白色胶状沉淀,L为氯碱工业中的常见产品。F的浓溶液与K加热可生成D和H。(部分生成物未标出)

(1)写出下列物质的化学式:E J
(2)写出D通入足量稀Ba(NO3)2溶液反应的化学方程式:_______________________
(3)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在Al制容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,写出该反应的离子方程式_____________
(4)A电池性能优越,A-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2A+3AgO+2NaOH=2NaAO2+3Ag+H2O,下列说法正确的是

A.该隔膜是阳离子交换膜
B.当电极上析出1.08 g Ag时,电路中转移的电子为0.01 mol
C.A电极的反应式为:A-3e-+4OH-=AO2-+2H2O
D.正极的电极反应式为:O2+2H2O+4e-=4OH-
下图是100 mg CaC 2 O 4 H 2 O受热分解时,所得固体产物的质量随温度变化的曲线。试利用图中信息结合所学的知识,回答下列各问题: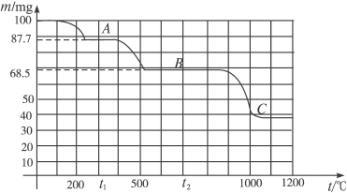
(1)温度分别为t 1 和t 2 时,固体产物的化学式A是______________,B是______________。
(2)由CaC 2 O 4 H 2 O得到A的化学方程式为______________________。
(3)由A得到B的化学方程式为____________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族。 E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 。
(2)E2+离子的价层电子排布图是 ,F原子的电子排布式是 。
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ,B元素的气态氢化物的VSEPR模型为 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为 。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程为 。
(6)某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为 ,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度d= g/cm3。(保留两位小数)

【选修—有机化学基础】
A是一种五元环状化合物,其核磁共振氢谱只有一个峰;X是一种良好的溶剂;F的核磁共振氢谱有3个峰,峰面积之比为2:2:3;G是一种合成橡胶和树脂的重要原料。A→G转化关系如下:

已知 :

请填写下列空白。
(1)写出A的结构简式: ,1molA和足量的H2反应最多消耗掉H2的物质的量为 。
(2)B中含有非氧官能团的名称是______________;⑤的反应类型是___________。
(3)G按系统命名法应命名为_________________。
(4)若E在一定条件下能脱水生成六元环状化合物,写出该六元环化合物的结构简式:_______________________。
(5)反应⑥的化学方程式为 ________。
(6)有机物H与E互为同分异构体,且官能团的种类和数目相同,写出所有符合条件的H的结构简式: __ ______。
【化学——选修3:物质结构与性质】
有A、B、C、D四种元素。已知A原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大。B 的基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同,B位于元素周期表的s区。C元素原子的外围电子层排布式为nsn-1npn-1。 D原子M能层为全充满状态,且核外的未成对电子只有一个。请回答下列问题:
(1)ACl3分子中A的杂化类型为 。ACl3分子的空间构型为 。
(2)某同学根据上述信息,推断B的核外电子排布如右图所示,
该同学所画的电子排布图违背了 。

(3)A、B、C三元素原子第一电离能由大到小的顺序为 (用元素符号表示)。C60分子中每个原子只跟相邻的3个原子形成共价键,且每个原子最外层都满足8电子稳定结构,则C60分子中π键的数目为 。
(4)D的基态原子有 种能量不同的电子;D2+ 的价电子排布式为 ;下图 (填甲、乙或丙)表示的是D晶体中微粒的堆积方式。若该晶体中一个晶胞的边长为a cm,则D晶体的密度为 (写出含a的表达式,用NA表示阿伏加德罗常数的值)。若D的原子半径为r ,则D晶胞这种堆积模型的空间利用率为 。(用含r的式子表示,不需化简)

甲 乙 丙
X、Y、Z三种短周期元素,其中X元素的原子序数大于Y,且X、Y的氧化物都是形成酸雨的主要物质。Z是地壳中含量最高的金属元素;而地壳中含量最高的非金属元素与X同主族、与Y同周期。
(1)实验室用H2XO4制取XO2气体的化学反应方程式为 。(请用具体元素符号表示化学式,下同)
(2)t℃时,0.1 mol·L-1的NaHXO3溶液pH=6,该溶液中各离子浓度由大到小顺序排列为 。
(3)请写出Z的氧化物与烧碱溶液反应的离子方程式 。
(4)一定条件下,YO与YO2存在下列反应:YO(g)+ YO2(g)  Y2O3(g),其平衡常数表达式为K= 。
Y2O3(g),其平衡常数表达式为K= 。
(5)工业上用氧化YH3法制取YO,该反应的热化学方程式为:
4YH3(g)+5O2(g)=4YO(g)+6H2O(g) △H="-905.8" kJ·mol-1;
已知Y2(g)+O2(g)=2YO(g) △H="+180" kJ·mol-1,则YH3与氧气反应产生两种无污染物质的热化学式为 。
(6)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。

①导线中电子移动方向为________。(用A、D表示)
②生成目标产物的电极反应式为__________________。
③该储氢装置的电流效率η=____________________。
(η= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)