现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。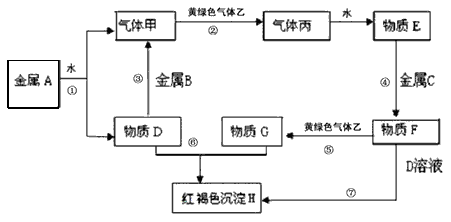
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________、B___________、C____________、
F___________、H___________、乙____________。
(2)写出下列反应离子方程式:
反应①______________________
反应⑥_____________________
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________、B___________、C____________、
F___________、H___________、乙____________。
(2)写出下列反应离子方程式:
反应①______________________
反应⑥_____________________