(15 分)二甲醚是一种重要的化工原料,利用水煤气(CO、H2)合成二甲醚是工业上的常用方法,该方法由以下几步组成:
2H2(g) +CO(g)  CH3OH(g) ΔH=" —90.0" kJ· mol-1 ①
CH3OH(g) ΔH=" —90.0" kJ· mol-1 ①
2CH3OH(g)  CH3OCH3(g) + H2O(g) ΔH="—24.5" kJ· mol-1 ②
CH3OCH3(g) + H2O(g) ΔH="—24.5" kJ· mol-1 ②
CO(g) + H2O(g) CO2(g) + H2(g) ΔH="—41.1" kJ· mol -1③
CO2(g) + H2(g) ΔH="—41.1" kJ· mol -1③
(1)反应①的 ΔS 0(填“>”、“<”或“=”)。在(填“较高”或“较低”)温度下该反应自发进行。
(2)在 250℃的恒容密闭容器中,下列事实可以作为反应③已达平衡的是_______(填选项字母)
| A.容器内气体密度保持不变 |
| B.CO 与 CO2的物质的量之比保持不变 |
| C.H2O 与 CO2的生成速率之比为 1∶1 |
| D.该反应的平衡常数保持不变 |
(3)已知一些共价键的键能如下:
运用反应①计算一氧化碳中碳氧共价键的键能kJ· mol-1。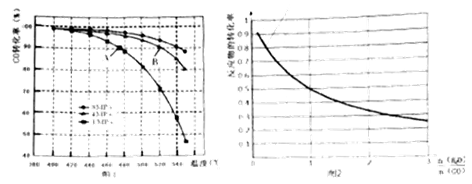
(4)当合成气中 CO 与 H2的物质的量之比恒定时,温度、压强对 CO 转化率的影响如图 1 所示。图 1 中 A 点的 v(逆)B 点的 v(正)(填“>”、“<”或“=”),说明理由。实际工业生产中该合成反应的条件为 500℃、4MPa 请回答采用 500℃的可能原因。
(5)一定温度下,密闭容器中发生反应③,水蒸气的转化率与 n(H2O)∕n(CO)的关系如图2所示。计算该温度下反应③的平衡常数 K=。
在图 2 中作出一氧化碳的转化率与 n(H2O)∕n(CO)的曲线。
物质A ~ G有下图所示转化关系部分反应物、生成物未列出)。其中A为某金属矿的主要成分,经过一系列反应可得到气体B和固体C。单质C可与E的浓溶液发生反应,G为砖红色沉淀。
请回答下列问题:
(1)写出下列物质的化学式:B___________、G___________。
(2)反应②的化学方程式是__________________________________________________。
(3)利用电解可提纯C物质,现以碱性锌锰电池为外电源,在该电解反应中电解质溶液是_______________,阳极物质是______________。MnO2是碱性锌锰电池的正极材料,电池放电时,正极的电极反应式为_____________________________________________。
(4)将0.20 mol B和0.10 mol O2充入一个固定容积为5 L的密闭容器中,在一定温度并有催化剂存在下,进行反应①,经半分钟后达到平衡,测得容器中含D 0.18 mol,则vO(2)== ______________mol/L·min);若温度不变,继续通入0.20 mol B和0.10 mol O2,则平衡________________移动填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol < nD) < ________mol。
(5)写出F G转化过程中,甲醛参与反应的化学方程式:_______________________________。
G转化过程中,甲醛参与反应的化学方程式:_______________________________。
【化学—选修5:有机化学基础】β-拉帕醌(β-lapachone)是一种抗癌新药,合成路线如下:
(1)已知X的分子式为C5H9Cl,则X的结构简式为:__________________
(2)有机物B的官能团为:__________________(填名称)
(3)上述反应中,原子利用率达100%的是( ) (选填:“A→B”、“B→C”、“D→E”、“E→F”).
(4)D→E发生的是取代反应,还有一种副产物与E互为同分异构体,且属于醚类,该物质的结构简式为:______________________________.
(5)化合物B的同分异构体很多,满足下列条件的同分异构体数目有_________种(不包括立体异构).
①苯环上有两个取代基;
②分子中有一个醛基和一个羧基;
③分子中只含有一个手性碳原子
(6)已知:双烯合成反应:
由2-甲基-1,3-丁二烯和乙烯为原料(无机试剂及催化剂任用)合成高分子 。
。
请写出下面两个反应方程式:
2-甲基-1,3-丁二烯与乙烯:_____________________________________________________。
生成高分子 :______________________________________________。
:______________________________________________。
乳酸分子式为C3H6O3,在一定的条件下可发生许多化学反应,下图是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。(已知—OH,—COOH等为亲水基团,F常做内燃机的抗冻剂)请回答相关问题: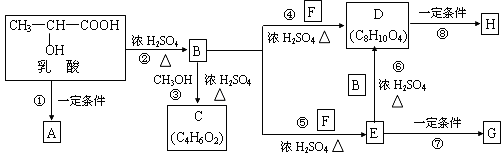
(1)推断C、F的结构简式。C:;F:。
(2)B中所含的官能团名称为;反应③的反应类型是。
(3)反应①的化学方程式为。
酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据下图所示:
溶解度/(g/100g水)
 温度/℃ 温度/℃化合物 |
0 |
20 |
40 |
60 |
80 |
100 |
| NH4Cl |
29.3 |
37.2 |
45.8 |
55.3 |
65.6 |
77.3 |
| ZnCl2 |
343 |
395 |
452 |
488 |
541 |
614 |
| 化合物 |
Zn(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
| Ksp近似值 |
10-17 |
10-17 |
10-39 |
回答下列问题:
(1)该电池的正极反应式为 ,电池反应的离子方程式为:
(2)维持电流强度为0.5A,电池工作五分钟,理论消耗Zng。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以通过____分离回收,滤渣的主要成分是二氧化锰、______和,欲从中得到较纯的二氧化锰,最简便的方法是,其原理是。
(4)用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入新硫酸和双氧水,溶解,铁变为加碱调节PH为,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。继续加碱调节PH为 ,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。若上述过程不加双氧水的后果是,原因是。
(12分)[化学---化学与技术]
工业上利用氨氧化获得的高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,工艺流程如下:
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)中和液所含溶质除NaNO2及少量Na2CO3外,还有__________(填化学式)。
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。蒸发Ⅰ产生的蒸气中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的_______(填操作名称)最合理。
(3)母液Ⅰ进行转化时加入稀HNO3的目的是_______。母液Ⅱ需回收利用,下列处理方法合理的是________。
a.转入中和液 b.转入结晶Ⅰ操作 c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO2、NaNO3两种产品的物质的量之比设为2:1,则生产1.38吨NaNO2时,Na2CO3的理论用量为______吨(假定Na2CO3恰好完全反应)。
非金属元素H、C、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛。
(1)O2-的离子结构示意图为,CS2的晶体类型为晶体;
(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例________(写化学式,任写两种);
(3)CH3OH在常温下为液态,沸点高于乙烷的主要原因是;
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
| 危险性 |
 |
| 储运要求 |
远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 |
NaOH、NaHSO3溶液吸收 |
| 包装 |
钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl-):c(ClO-)=11:1时,则c(ClO-):c(ClO3-)比值等于。
(5)镁是一种较活泼的金属,Mg与Ca类似,也能与C形成某种易水解的离子化合物。已知该化合物0.1mol与水完全反应后,产生0.1mol的某种气体。该气体被溴水全部吸收后,溴水增重2.6g。请写出该水解反应方程式。
【化学——选修5:有机化学基础】6-羰基庚酸是一种重要的化工中间体,其合成路线如下: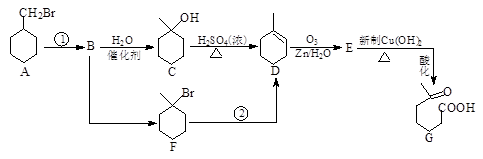
已知: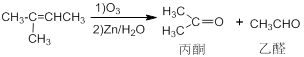
(1)反应①的条件是,C→D的反应类型是,C中官能团的名称是。
(2)下列说法中正确的是()
a.C能被催化氧化成酮
b.D不能使酸性高锰酸钾溶液褪色
c.Ni催化下1mol E最多可与2molH2加成
d.G既能发生取代反应,又能发生加成反应
(3)E与新制Cu(OH)2反应的化学方程式为。
(4)G的同分异构体有多种,满足以下条件的同分异构体有种。
A.分子中含有环己烷的结构
B.能与NaHCO3溶液反应,放出气体
C.1mol该物质能与2molNa完全反应
(5)已知“Diels-Alder反应”为: 。物质D与呋喃(
。物质D与呋喃(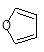 )也可以发生“Diels-Alder反应”,该化学反应方程为:。
)也可以发生“Diels-Alder反应”,该化学反应方程为:。
[化学——选修2]化学与技术:(15分)硫酸是重要的工业原料.工业上生产硫酸主要分为造气、催化氧化、吸收三个阶段,其生产流程图如下:
(1)操作I的内容是,此操作目的是.物质B是.a=。
(2)工业上既可用硫黄也可用硫铁矿(FeS2)造气,若使用硫铁矿造气.另一产物是一种常见的红棕色固体.写出用硫铁矿造气时反应的化学方程式。
(3)催化反应室中的反应是一个气体体积缩小的反应.增大压强有利于反应向右进行.但实际生产却是在常压下进行的.原因是。
(4)工业生产中常用氨一硫酸法进行尾气脱硫,以达到消除污染、废物利用的目的.用两个化学方程式表示其反应原理。
(5)若用等质量的硫黄、FeS2生产硫酸.假设原料的总利用率均为90%.则二者得到硫酸的质量比为。
高铁酸盐是一种强氧化剂,在能源、环保等方面均有广泛的用途。湿法、干法制备高铁酸钾的原理如下表所示:
| 湿法 |
强碱介质中,Fe(NO3)3与NaClO反应得到紫红色高铁酸盐溶液 |
| 干法 |
Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸钾(K2FeO4)和KNO2等产物 |
(1)某工厂用湿法制备高铁酸钾的流程如图所示:
①反应I的化学方程式为。
②反应Ⅱ的离子方程式为。
③已知25℃时Fe(OH)3的Ksp=4.0×10—38,反应Ⅱ后的溶液中c(Fe3+)=4.0×10—5mol·L—1.则需调整pH=时,开始生成Fe(OH)3沉淀(不考虑溶液体积的变化)。
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠溶液中加入饱和KOH溶液,即可析出高铁酸钾。
①已知高铁酸钠和水反应,有Fe(OH)3和O2生成,则高铁酸钠的氧化性比O2(填“强”或“弱”)。
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠(填“大”或“小”)。
(3)高铁酸钾是一种理想的水处理剂,其处理水的原理为。
(4)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为。
液晶高分子材料应用广泛。新型液晶基元——化合物Ⅳ的合成线路如下: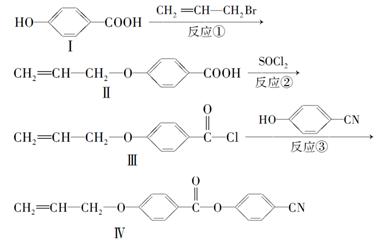
(1)化合物Ⅰ的分子式为________,1 mol化合物Ⅰ最多可与________mol NaOH反应。
(2)CH2=CH—CH2Br与NaOH水溶液反应的化学方程式为(注明条件)______________。
(3)化合物Ⅰ的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异体的结构简式____________________。
(4)下列关于化合物Ⅱ的说法正确的是_______(填字母)。
| A.属于烯烃 | B.能与FeCl3溶液反应显紫色 |
| C.一定条件下能发生加聚反应 | D.能使溴的四氯化碳溶液褪色 |
(5)反应③的反应类型是________。在一定条件下,化合物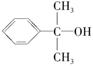 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。Ⅴ的结构简式是__________。
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。Ⅴ的结构简式是__________。
(本题共12分)碘及其化合物可广泛用于医药和工业生产等。回答下列问题:实验室用海带提取I2时操作步骤依次为:灼烧、溶解、过滤、_______、_______及蒸馏。
灼烧海带时除需要三脚架、酒精灯、玻璃棒外,还需要的实验仪器是______________。
“过滤”后溶液中含一定量硫酸盐和碳酸盐。现要检验溶液中的I-,需选择的试剂组合及其先后顺序是_____________。(选填编号)
a.AgNO3溶液 b.Ba(NO3)2溶液 c.BaCl2溶液 d.CaCl2溶液在海带灰滤液中加入适量氯水后一定存在I2,可能存在IO3—。
请补充完整检验含I2溶液中是否含有IO3—的实验方案(可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液):
①取适量含I2溶液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②_____________________________________________________________________。分解水可用SO2/I2循环法。该法共涉及三步化学反应。
___________________;2H2SO4  2SO2↑+ O2↑+ 2H2O;____________________。
2SO2↑+ O2↑+ 2H2O;____________________。
与传统的分解水的方法相比,本法的优点是____________;缺点是_____________。
[化学—选修3:物质结构与性质]
(1)锌是一种重要的金属,锌及其化合物有着广泛的应用。
①指出锌元素在周期表中的位置:周期,族,区。
②NH3分子中氮原子的杂化轨道类型为,基态氮原子的核外电子排布式是;
③下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为;该化合物的晶体熔点比干冰高得多,原因是。
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为140-145pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 ,并阐述理由。
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为。
③继C60后,科学家又合成了Si60、N60。C、Si、N原子电负性由大到小的顺序是。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则 Si60分子中的数目为。
【化学—选修2化学与技术】氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下:
金属离子含量与混合液pH、CuCl产率与混合液pH的关系图如图。
【已知:金属离子浓度为1 mol·L-1时,Fe(OH)3开始沉淀和沉淀完全的pH分别为1.4和3.0,Cu(OH)2开始沉淀和沉淀完全的pH分别为4.2和6.7】
请回答下列问题:
(1)酸浸时发生反应的离子方程式是______;析出CuCl晶体时的最佳pH在_______左右。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为________________。
(3)析出的CuCl晶体要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2 h、冷却密封包装。70℃真空干燥、密封包装的目的是_____________________________________。
(4)产品滤出时所得滤液的主要分成是________,若想从滤液中获取FeSO4·7H2O晶体,还需要知道的是__________________。
(5)若将铁粉换成亚硫酸钠也可得到氯化亚铜,试写出该反应的化学方程式:_________________。为提高CuCl的产率,常在该反应体系中加入稀碱溶液,调节pH至3.5。这样做的目的是_____________。
(NH4)2Fe(SO4)2俗称莫尔盐,其常见的制备工艺流程如下: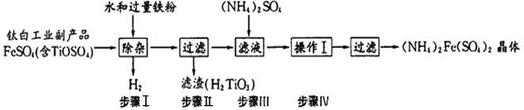
(1)已知流程中铁粉制备反应如下:
4 H2O(g) +3Fe(s) Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s) =" 3" Fe(s)+ 2O2(g) △H ="b" kJ/mol
则光解气态水制备H2的热化学方程式为。
(2)步骤I中加水发生如下反应,请完善该反应:+2H2O  2H++ H2TiO3 ↓;
2H++ H2TiO3 ↓;
该步骤加入铁粉的作用是①;②。
(3)步骤Ⅳ生成(NH4)2Fe(SO4)2,其化学反应方程式为;
写出(NH4)2Fe(SO4)2溶液中各离子溶度由大到小的顺序:
(4)已知在潮湿空气中Fe(OH)2比FeCl2更易被氧化。据此分析(NH4)2Fe(SO4)2比FeSO4稳定的原因是。
(5)室温时Fe(OH)3的悬浊液中存在Fe(OH)3(s) Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)="0.08" mol·L-1则溶液的pH等于。
Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)="0.08" mol·L-1则溶液的pH等于。