按以下步骤可从 合成
合成 (部分试剂和反应条件已去).
(部分试剂和反应条件已去).
请回答下列问题:
(1)B、F的结构简式为:B F 。
(2)反应①~⑦中属于消去反应的是 (填代号)。
(3)根据反应 ,写出在同样条件下
,写出在同样条件下
CH2=CH—CH=CH2与等物质的量Br2发生加成反应的化学方程式: 。
(4)写出第④步 的化学方程式(有机物写结构简式,注明反应条件). 。
的化学方程式(有机物写结构简式,注明反应条件). 。
(5)A—G这七种有机物分子中含有手性碳原子的是(填序号) 。
(6)核磁共振谱是测定有机物分子结构最有用的工具之一。在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。例如:乙醛的PMR谱中有2个信号峰,其强度之比为3∶1。则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是 。
A. B.
B.
C. D.
D.
某芳香族化合物A式量小于150,氢氧质量比为1∶8,完全燃烧后只生成CO2和H2O。取等质量的A分别与足量NaHCO3和Na反应,生成的气体在同温同压下的体积比为1∶1。工业常用A来合成药物B及医药中间体G,流程如下:
已知:

(1)写出A含有的官能团的名称 ,D的结构简式 。
(2)D生成E的反应类型是 。
(3)A合成B的同时,A自身之间也能发生缩聚反应,写出该缩聚反应的化学方程式 。
(4)写出F与过量NaOH共热时反应的化学方程式 。
(5)B有多种同分异构体,写出符合下列条件的一种物质的结构简式 。
①只有一种官能团
②能发生银镜反应
③苯环上的一氯取代物只有二种
④核磁共振谱共有四组峰,个数比为3∶2∶2∶1。
(6)下列有关说法正确的是 。
| A.可由A经一步反应获得D |
B. 与G互为同分异构体 与G互为同分异构体 |
| C.G易水解,可用FeCl3溶液检验是否发生水解 |
| D.1molG一定能和5mol氢气反应 |
A、B、C、D是四种常见单质,其对应元素的核电荷数依次增大,其中B、D属于常见金属,E、F、G化合物。所有物质之间有如下的转化关系:



(1)写出D→A+F的化学方程式: ;
(2)写出B→A+E的离子方程式: 。
(3)将G的饱和溶液滴入沸水中可形成红褐色的透明液体,再将此液体装入U型管,并在U型管的两端插入电极,接通直流电,在阳极端可观察到的现象是___________________;
(4)向含0.1 mol E的溶液中滴加5 mol/L 的盐酸溶液,得到沉淀3.9 g,则加入盐酸体积为 mL。
I.如图1为向25mL 0.1mol·L—1NaOH溶液中逐滴滴加0.2mol·L-1CH3COOH溶液过程中溶液pH的变化曲线。请回答:
⑴ B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?________(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?________区间(若正确,此问不答)。
⑵关于该滴定实验,从下列选项中选出最恰当的一项________(选填字母)。
| |
锥形瓶中溶液 |
滴定管中溶液 |
选用指示剂 |
选用滴定管 |
| A |
碱 |
酸 |
酚酞 |
(乙) |
| B |
酸 |
碱 |
甲基橙 |
(甲) |
| C |
碱 |
酸 |
石蕊 |
(甲) |
| D |
酸 |
碱 |
酚酞 |
(乙) |
⑶ AB区间,c(OH—)>c(H+),则c(OH—)与c(CH3COO—)大小关系是________。
A.c(OH—)大于c(CH3COO—) B.c(OH—)小于c(CH3COO—)
C.c(OH—)等于c(CH3COO—) D.上述三种情况都可以
⑷在D点时,溶液中c(CH3COO—)+c(CH3COOH)________2c(Na+)(填“>”“<”或“=”)。
Ⅱ.t℃时,某稀硫酸溶液中c(H+) = 10—a mol·L—1,c(OH-) = 10—b mol·L—1,已知a+b=13:
⑸该温度下水的离子积常数Kw的数值为________。
⑹该温度下(t℃),将100mL 0.1mol·L—1的稀H2SO4与100mL 0.4mol·L—1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=________。
已知2X2(g)+Y2(g) = 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2,在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴此反应平衡常数表达式为_________________;若将温度降低到300℃,则反应平衡常数将___________(填增大、减少或不变)。
⑵若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系___________(用代数式表示)。
⑶能说明反应已达平衡状态的是___________________。
| A.浓度c(Z)=2c(Y2) | B.容器内压强保持不变 |
| C.v逆(X2)=2v正(Y2) | D.容器内的密度保持不变 |
⑷若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2mol X2和1mol Y2达到平衡后,Y2的转化率将_____(填“变大”、“变小”或“不变”)。
汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g) + O2(g)  2NO(g) △H > 0
2NO(g) △H > 0
已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)该反应的平衡常数表达式为
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率是 %(保留整数)。
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L 和3.0×10-3mol/L,此时反应 (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是 .
(4)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是 (填字母序号)。
(5)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数 (填“变大、“变小”或“不变)
CuSO4溶液是中学化学及工农业生产中常见的一种试剂。
(1)某同学配制CuSO4溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了,随后,他向烧杯中加入了一定量的 溶液,得到了澄清的CuSO4溶液。
(2)该同学利用制得的CuSO4溶液,进行以下实验探究。
①图一是根据反应Zn + CuSO4== Cu + ZnSO4设计成的锌铜原电池。Cu极的电极反应式是 ,盐桥中是含有琼胶的KCl饱和溶液,电池工作时K+向 移动(填“甲”或“乙”)。
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是 (填“CH4”或“O2”),a处电极上发生的电极反应式是 ;当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为 L。
(3)反应一段时间后,燃料电池的电解质溶液完全转化为K2CO3溶液,以下关系正确的是 。
| A.c(K+)+c(H+)=c(HCO3-)+ c(CO32-)+c(OH-) |
| B.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C.c(K+)>c(CO32-)>c(H+)>c(OH-) |
| D.c(K+)>c(CO32-)>c(OH-)>c(HCO3-) |
E.c(K+)= 2c(CO32-)+ c(HCO3-)+c(H2CO3)
制取硝酸铵的流程图如下:
请回答下列问题:
(1)合成氨的原料通常各来自何处?
(2)已知N2(g)+3H2(g) 2NH3(g),Q>0。请解释:
2NH3(g),Q>0。请解释:
①什么是可逆反应?
②为有效提高氨的产率,实际生产中宜采取哪些措施?
(3)写出氨催化氧化的化学方程式。铂—铑合金网有何作用?为什么铂铑合金网未预热也会发热?
(4)举出硝酸铵的两种主要用途。解释为什么该用途对现代社会非常重要?
(5)在一定温度和压强的密闭容器中,将平均式量为8.5的H2和N2混合,当该反应达到平衡时,测出平衡混合气的平均式量为10,此时N2的转化率为______________,平衡混合气体中NH3的体积分数为____________________________________。
(6)请你为硝酸厂的选址提出合理化建议。
将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应:
I2(g) + H2(g)  2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示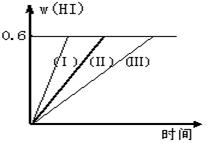
(1)达平衡时,I2(g)的物质的量浓度为 写出该反应的平衡常数表达式 _____________________________________。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是 ,则乙条件可能是 。
(填入下列条件的序号)
①恒容条件下,升高温度; ②恒容条件下,降低温度;③恒温条件下,缩小反应容器体积; ④恒温条件下,扩大反应容器体积; ⑤恒温恒容条件下,加入适当催化剂。
高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂。
(1)FeO42-与水反应的方程式为:4FeO42- + 10H2O  4Fe(OH)3 + 8OH-+ 3O2,
4Fe(OH)3 + 8OH-+ 3O2,
K2FeO4在处理水的过程中所起的作用是 和 。
(2)将适量K2FeO4配制成c(FeO42-) =1.0×10-3 mol·L-1(1.0mmol·L-1)的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ。题(1)中的反应为FeO42-变化的主反应,该反应的△H 0。
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是 (填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.改变溶液的pH,当溶液由pH=10降至pH=4的过程中,HFeO4-的分布分数先增大后减小
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:H2FeO4+OH-=HFeO4-+H2O
D.pH约为2.5 时,溶液中H3FeO4+和HFeO4-比例相当
(4)HFeO4- H++FeO42-的电离平衡常数表达式为K=___________________,其数值接近 (填字母)。
H++FeO42-的电离平衡常数表达式为K=___________________,其数值接近 (填字母)。
A.10-2.5 B.10-6 C.10-7 D.10-10
(5)25℃时,CaFeO4的Ksp = 4.536×10-9,若要使100mL,1.0×10-3 mol·L-1的K2FeO4溶液中的c(FeO42- )完全沉淀,理论上至少要加入的Ca(OH)2的物质的量为 mol,
完全沉淀后溶液中残留的c(FeO42- )为______________。
在2.00L的密闭容器中,反应2A(g) B(g)+ C(g)分别在三种不同实验条件下进行,但起始浓度相同,均为c(A)=0.100mol/L、c(B)=0.020mol/L及c(C)=0.020mol/L。反应物A的浓度随时间的变化如下图所示:
B(g)+ C(g)分别在三种不同实验条件下进行,但起始浓度相同,均为c(A)=0.100mol/L、c(B)=0.020mol/L及c(C)=0.020mol/L。反应物A的浓度随时间的变化如下图所示:
请回答下列问题:
(1)以下说法能说明该反应已达到平衡状态的是: (填序号)
①c(A):c(B):c(C)=2:1:1
②v(A)=" 2" v(B)
③体系的压强不再改变
④A的质量分数不再改变
⑤混合气体的密度不再改变
(2)根据实验③回答:反应开始到4.0min时反应物A的转化率为 ,
B平均反应速率为 。
(3)与①比较,②和③分别仅改变一种反应条件。所改变的条件是:
② ;③ 。
(4)实验①条件下该反应的化学平衡常数值是 。若实验①到达平衡后,维持体系温度不变,往容器中再投入0.028mol B和0.028mol C,求新平衡时体系中A的物质的量浓度。(写出计算过程)
四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
| 元素 |
A |
B |
C |
D |
| 性质 结构 信息 |
原子核外有两个电子层,最外层有3个未成对的电子 |
原子的M层有1对成对的p电子 |
原子核外电子排布为[Ar]3d104s1, 有+1、+2两种常见化合价 |
有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
⑴写出B原子的电子排布式 。
⑵A元素的氢化物的沸点比同主族相邻元素氢化物沸点 (填“高”或“低”),其是__________________________。
⑶D的最高价氧化物的电子式: 。高温下D的氧化物还原赤铁矿的方程式为可逆反应,写出该反应的化学方程式___________________,该反应的平衡常数表达式K=___________。
⑷往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为________________,简要描述该配合物中化学键的成键情况__________________。
⑸下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键。
”表示没有形成共价键的最外层电子,短线表示共价键。
则在以上分子中,中心原子采用sp3杂化形成化学键的且空间构型是角形的是 (填写序号);在②的分子中有 个σ键和 个π键。
⑹已知NH4+、N4H44+的空间构型均为四面体,NH4+的结构式为 \s\up10(∣←N-,\s\up10(∣H(→表示共用电子对由N原子单方面提供)。 请画出N4H44+的结构式_____________________。
在20L恒容的密闭容器中,加入3mo1SO3(g)和lmo1氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.09 mol·L-1,当反应到8min时,反应到达平衡,此时三氧化硫浓度c(SO3)=" a" mol·L-1。

(1)0min~4min内生成O2平均速率v(O2)= mol·L-1·min-1
(2)达到平衡时c(O2)=c(SO2),则a= mol·L-1,在下列坐标系中作出0min~8min及之后SO2、O2、SO3浓度随时间变化曲线.
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于a mol·L-1的是
| |
A |
B |
C |
D |
| SO3 |
1mol |
3mol |
3mol |
0mol |
| SO2 |
2mol |
1.5mol |
0mol |
6mol |
| O2 |
2mol |
1mol |
0mol |
5mol |
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表: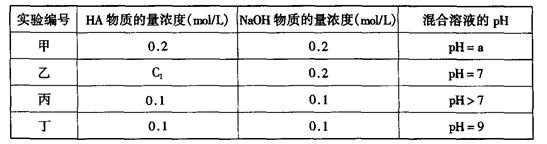 请回答:
请回答:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱 酸 。
(2)不考虑其它组的实验结果,单从乙组情况分析,C1是否一定等于0.2mol/L (选填“是”或“否”)。混合溶液中离子浓度c(A-)与c(Na+)的大小关系是
| A.前者大 | B.后者大 | C.二者相等 | D.无法判断 |
(3)从丙组实验结果分析,HA是 酸(选填“强”或“弱”)。
该混合溶液中离子浓度由大到小的顺序是
(4)丁组实验所得混合溶液中由水电离出的c(OH—)= mol/L
写出该混合溶液中下列算式的精确结果(不能做近似计算,回答准确值,结果不一定要化简)。 c(Na+)-c(A—)= mol/L
云南省曲靖的铬渣污染经媒体报道后,铬污染再次引起人们的关注。利用化学原理可以对工厂排放的含铬废水、铬渣等进行有效处理。
I.含铬废水的处理:某企业排放的含铬废水中含有较多毒性较大的Cr2O72-,某研究性学习小组为了变废为宝,将废水处理得到金属铬,设计了如下的工艺流程。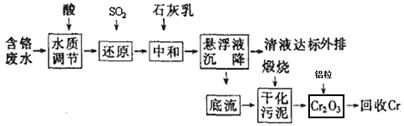
(1)加酸调节到pH=6,则用pH试纸测定溶液pH的操作是: 。
。
(2)在含Cr2O72-废水中存在着平衡:Cr2O72-+H2O 2CrO42-+2H+,请写出该平衡的平衡常数表达式k= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
2CrO42-+2H+,请写出该平衡的平衡常数表达式k= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
(3)请写出通入SO2时发生的离子反应: 。
(4)写出加入铝粒时发生反应的化学方程式 ,该反应是焓 (填“增加”或“减少”)反应。
II.铬渣的处理
铬渣烧结炼铁法:铬渣中约含有55%的氧化钙和氧化镁,此外还含有15%左右的氧化铁,这些都是炼铁所需的成份。少量的铬渣代替消石灰同铁矿粉、煤粉混合,经烧结后送入高炉冶炼,六价铬还原为三价铬或金属铬,金属铬熔入铁水,而其它成分熔入熔渣。炼铁可使铬渣彻底解毒并充分利用,是铬渣治理的良好方法之一。
碱性溶液还原法:直接在碱性铬渣中加入硫化钠等进行六价铬的还原反应,形成Cr(OH)3沉淀后,过滤回收铬污泥。
(5)铬渣烧结炼铁法中煤粉的作用是 。(写两点)
(6)请配平碱性溶液还原法中发生的离子反应:□Cr2O72-+□S2—+□H2O=□Cr(OH)3+□S2O32—+□OH—