晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体的晶胞如右图所示。随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度越来越高。现有一简单可行的测定方法,具体步骤如下:
①将固体食盐研细,干燥后,准确称取mgNaCl固体并转移到定容容器A中;
②用滴定管向定容容器A中加入苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为VmL。回答下列问题:
(1)步骤①中A仪器最好用_______________(填仪器名称);;
(2)你认为步骤②中用_________(填“酸式”或“碱式”滴)滴定管,_____________,原因是________________;
(3)能否用胶头滴管代替步骤②中的滴定管___________,其原因是_________。
(4)经X射线衍射仪测得NaCl晶体中最邻近Na+和Cl-平均距离为acm.则利用上述方法测得的阿伏加德罗常数的数学表达式为NA=_________________。
氮元素可以形成多种分子和离子,如NH3、N2H4、N2-、NH4+、N2H62+等。回答以下问题:
(1)N的基态原子中,有_________个运动状态不同的未成对电子;
(2)某元素原子与N3-含有相同的电子数,其基态原子的价电子排布图是____________;
(3)NH3、N2H4、NH4+、N2H62+四种微粒中,同种微粒间能形成氢键的有_________;不能作为配位体的有_______;
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8K,主要原因是_______;
(5)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物.
①N2H4分子中氮原子的杂化类型是_________;
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)
若该反应中有4mol N-H键断裂,则形成的π键有_________mol;
(6)肼能与硫酸反应生成N2H6SO4.N2H6SO4化合物类型与硫酸铵相同,则N2H6SO4内微粒间作用力不存在_________(填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
金属及其化合物在人类生产、生产中发挥着重要的作用。
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是________(填化学式,下同);适宜做耐火材料的是_______________。
(2)若Na2CO3粉末中混有少量NaHCO3杂质,最适宜的除杂方法是________,反应的化学方程式___________。
(3)取少量FeCl2溶液,按如图所示操作,使其跟NaOH溶液反应.可观察到的实验现象是_____________。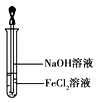
(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是____________(填序号)。
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
榴石矿石可以看作由CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下: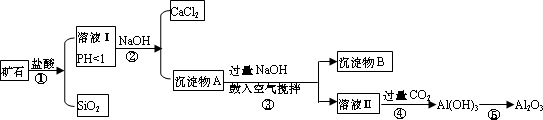
(1)溶液Ⅰ中除了Ca2+外,还可能含有的金属阳离子有__________________;
(2)步骤③中NaOH参加反应的离子方程式____________________________,鼓入空气并充分搅拌的目的是(用化学方程式表示)____________________;
(3)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是_____________________。
将一定质量的镁铝合金投入100 mL 一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L 的NaOH 溶液,生成的沉淀跟加入的NaOH 溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)
求:
(1)加入NaOH 溶液0--20mL 过程中反应的化学方程式为_______________________。
160--180mL 过程中反应的离子方程式为__________________________。
(2)合金中Mg 的质量为____________g,所用HCl 的物质的量浓度为____________mol/L。
实验室可用KMnO4固体和浓盐酸反应制氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)  2KCl+2MnCl2+5Cl2↑+8H2O。
2KCl+2MnCl2+5Cl2↑+8H2O。
(1)该反应中氧化剂是_____________,还原剂是__________________。
(2)若反应中有0.20 mol 电子发生转移,生成氯气的体积为____________(标准状况),被氧化的HCl的物质的量是___________________。
[化学——物质结构与性质
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。回答下列问题:
(1)基态砷原子的电子排布式为 ;
(2)K3[Fe(CN)6]晶体中Fe3+与CN之间化学键类型为_________键,与CN互为等电子体的化合物分子式为 ;
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有0
NOx、O3、CH2=CHCHO、HCOOH、CH3—C—0—0—N02 (PAN)等二次污染物。
①N2O结构式可表示为N=N=O,N2O中中心氮原子的杂化轨道类型为 ;
1 mol PAN含σ键数目为 ;
②测定大气中PM2.5的浓度方法之一是 -射线吸收法,
-射线吸收法, -射线放射源可用85Kr。K晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则
-射线放射源可用85Kr。K晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则 = (填数字)。已知Kr晶体的密度为pg/cm3,摩尔质量为Mg/mol,阿伏伽德罗常数用Na表示,列式表示Kr晶胞参数a= nm。
= (填数字)。已知Kr晶体的密度为pg/cm3,摩尔质量为Mg/mol,阿伏伽德罗常数用Na表示,列式表示Kr晶胞参数a= nm。
[化学—化学与技术]
海洋是一个丰富的资宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河人海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和 池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用: (写一点即可)。
(2)电渗析法是近年发展起的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:
①海水不能直接通人到阴极室中,理由是 。
②A口排出的是 (填“淡水”或“浓水”).

(3)用苦卤(含Na+、K+、Mg2+CL-、Br-等离子)可提取溴,其生产流程如下:

①若吸收塔中的溶液含BrOf,则吸收塔中反应的离子方程式为: .
②通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化重新获得含Br2的溶液? 。
③向蒸馏塔中通人水蒸气加热,控制温度在90°C左右进行蒸馏的原因是 。
钼(Mo)是一种过渡金属元素,通常用作合金及不镑钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备 金属钼的主要流程图,已知钼酸难溶于水。
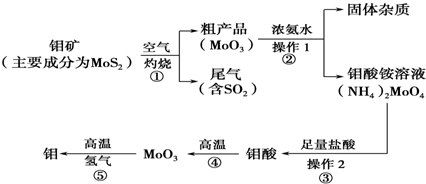
(1)写出反应①的化学方程式: 。
(2)写出反应②的化学方程式: 。
(3)反应①的尾气可以用碳酸钠溶液吸收。已知:根据表中提供的数据可知,在溶液中不能大量共存的微粒是______________;
| A.HCO3-、HSO3- | B.HCO3-、SO32- | C.HCO3-、H2S03 | D.HSO3- CO32- |
向过量碳酸钠溶液中通人少量二氧化硫,写出反应的离子方程式: 。
(4)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有 。
(5)工业上制备还原性气体CO和H2的反应原理为C02+CH4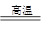 2CO + 2H2,CH4 + H2
2CO + 2H2,CH4 + H2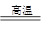 CO + 3H2,含甲烷体积分数为80%的10L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原Mo03制钼,理论上能生产钼的质量为g(小数点后保留1位,钼的相对原子质量为96)。
CO + 3H2,含甲烷体积分数为80%的10L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原Mo03制钼,理论上能生产钼的质量为g(小数点后保留1位,钼的相对原子质量为96)。
雾霾天气肆虐给人类健康带来了严重影响。燃煤和汽车尾气 是造成空气污染的原因之一。
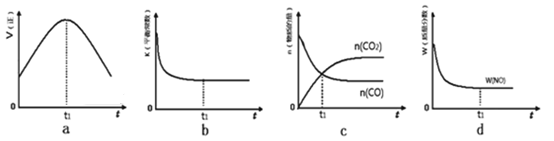
(1)汽车尾气净化的主要原理为: 2NO(g)+2CO(g)= 2C02 (g)+N2 (g) △H<0 。
①该反应的速率时间图像如右图中左图所示。若其他条件不变,仅在反应前加人合适的催化剂,则其速率时间图像如右图中右图所示。

以下说法正确的是 (填对应字母)。
| A.a1>a2 | B.b1<b2 |
| C.t1>t2 | D.右图中阴影部分面积更大 |
E.左图中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) △H="-867" kJ/mol
2NO2(g)= N2O4(g) △H="-56.9" kJ/mol
H2O(g) = H2O(l) △H ="-44.0" kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(1)的热化学方程式: 。
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O CO+3H2 ,该反应在不同温度下的化学平衡常数如下表:
CO+3H2 ,该反应在不同温度下的化学平衡常数如下表:
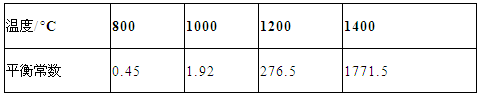
①该反应是 反应(填“吸热”或“放热”)。
②T℃时,向1L密闭容器中投入1mol CH4 和1mol H2Og),平衡时C(CH4)=0.5 mol·L- ,该温度下反应CH4 + H2O= CO+3H2的平衡常数K= 。
(4)甲烷燃料电池可以提升能量利用率。如图是利用甲烷燃料电池电解l00mLlmol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变)。

①甲烷燃料电池的负极反应式: 。
②电解后溶液的pH= ,(忽略氯气与氢氧化钠溶液反应)。
③阳极产生气体的体积在标准状况下是 L。
无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为 ;
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
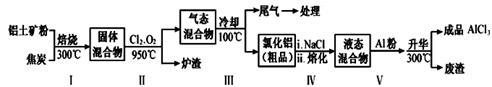
已知:
| 物质 |
SiCl4 |
AlCl3 |
FeCl3 |
FeCl2 |
| 沸点/℃ |
57.6 |
180(升华) |
300(升华) |
1023 |
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是 (只要求写出一种);
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是 ;
③已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1="+1344.1kJ" ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2="+1169.2kJ" ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为 ;
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为 ;
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是 。
麦秸杆、木屑等废料经干馏制燃料气过程中产生大量的废液,俗称木醋液(主要成分乙酸,还含少量的甲醇、苯酚、焦油等)。以木醋液与白云石(主要成分2MgCO3·3CaCO3,还含有SiO2等杂质)等为原料,可制备出绿色环保型融雪剂CMA(醋酸钙、醋酸镁固体的混合物)。
CMA生产流程如下:
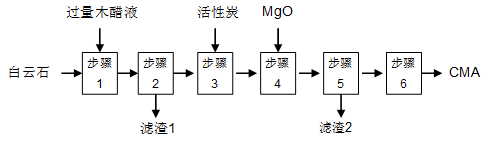
(1)步骤①发生反应的离子方程式为 ________________。
(2)滤渣1的主要成分为 (写化学式);步骤②所得滤液常呈褐色,颜色除与木醋液中含有少量的有色焦油外,产生颜色的另一主要原因是 。
(3)步骤③是往滤液中加活性炭粉,可使滤液脱色,这是利用了活性炭具有 。
实验测知CMA中钙、镁离子的物质的量之比与出水率(与融雪效果成正比)的关系如图。
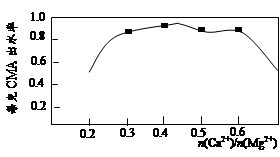
(4)由图知,当CMA中n(Ca2+)∶n(Mg2+)约为 时融雪的效果最好。(选填字母)
a.1∶2 b.3∶7 c.2∶3
步骤④的目的主要是 , 。
(5)步骤⑥包含的操作有 、过滤、洗涤及干燥。
海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素。
(1)氯原子结构示意图是 ,碘在元素周期表中的位置是 ,HI的稳定性比HBr (填写“强”或“弱”)。
(2)向浓缩的海水中通入Cl2,可将Br-转化为Br2。再用“空气吹出法” 将Br2从浓海水中吹出,并用纯碱浓溶液吸收,生成NaBr、NaBrO3等。当有1 mol Br2被纯碱吸收时,转移的电子数为 。
下图是NaClO的发生装置。该装置主要利用了电解饱和食盐水的原理,可实现对海水的消毒和灭藻。
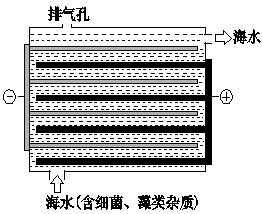
(3)写出装置中产生NaClO的化学方程式 。海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH) 2和CaCO3。 生成CaCO3的离子方程式是 。若每隔5-10 min倒换一次电极电性,可有效地解决阴极的结垢问题。试用电极反应式并结合必要的文字进行解释 。
NaOH溶液吸收SO2得Na2SO3,可用Na2SO3吸收SO2。在SO2被吸收的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下:
| n(SO32-):n(HSO3-) |
91:9 |
1:1 |
1:91 |
| pH |
8.2 |
7.2 |
6.2 |
(4)从上表可判断,NaHSO3溶液呈 (填“酸性”、“碱性”、“中性”),请用平衡原理解释: 。
(5)当吸收液呈中性时,溶液中离子浓度关系正确的是 (选填字母)。
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
d.c(Na+)>c(SO32-)>c(HSO3-)>c(H+)=c(OH-)
农业对化肥的需求是合成氨工业发展的持久推动力。
(1)氮原子最外电子层上有 种能量不同的电子,其原子核外存在 对自旋相反的电子。
(2)一定温度、压强下,氮气和氢气反应生成1mol氨气的过程中能量变化示意图如右,请写出该反应的热化学反应方程式: 。(Q的数值用含字母a、b的代数式表示)
下图表示500℃、60.0MPa条件下,原料气H2和N2的投料比与平衡时NH3体积分数的关系。


(3)工业上合成氨的温度一般控制在500℃,原因是 。
根据图中a点数据计算N2的平衡体积分数为 。
(4)硫化铵晶体与晶体硅相比较,____________的熔点较高,原因是___________。
(5)写出等物质的量浓度等体积的硫酸氢钠与硫化铵溶液反应的离子方程________________。