(1)25℃时,将0.1 mol/L NaOH溶液与0.06mol/L的H2SO4溶液等体积混合(忽略混合后体积的变化),求所得溶液的pH= 。
(2)纯水中c(H+ )=5.0×10-7 mol/L,则此时纯水中的c(OH-) =_______________;若温度不变, 滴入稀硫酸使c(H+)=5.0×10-3mol/L,则c(OH-) =_______________;在该温度时,往水中滴入NaOH溶液,溶液中的c(OH-)=5.0×10-2 mol/L,则溶液中c(H+ )= 。
为检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。

请回答下列问题:
(1)装置A、D中发生反应的化学方程式为 ; 。
(2)实验前欲检查装置A的气密性,可以采取的操作是 ;
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是 (用操作编号填写)
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为 ;
(5)当D中产生 现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;
(6)装置D的作用为 。
某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。

(1)装置A中发生反应的离子方程式为_____________________________。
(2)该实验装置明显存在不足之处,改进的措施为____________________
(3)已知在装置C中通入一定量的氯气后,观察到测得D中有黄红色的气体(提示:是一种氯的氧化物)。已知C中所得固体含有NaHCO3。现对C中的成分进行猜想和探究。
①提出合理假设.
假设一:存在两种成分,为NaHCO3、NaCl
假设二:存在三种成分,为NaHCO3、Na2CO3、NaCl
②设计方案并实验.请在表格中写出实验步骤以及预期现象和结论.
限选试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。

结论:由步骤3的结论结合步骤2中的a,则假设一成立;由步骤3的结论结合步骤2中的b,则假设二成立.
若C中有0.1molCl2恰好与10.6gNa2CO3反应,且假设一成立,由此可推知C中反应生成的氯的氧化物为
(写化学式),写出C中发生反应的化学方程式 。
下图是测定植物某一生命活动过程的装置,A瓶中的氢氧化钠的作用是______________,B瓶中的石灰水的作用是___________,D瓶中出现的现象是_____________。此实验说明植物具有_________性质。
已知醋酸和盐酸是日常生活中极为常见的酸。
(1)常温常压,在 pH=5的稀醋酸溶液中,c(CH3COO‾)=_____________;下列方法中,可以使0.10 mol/LCH3COOH的电离程度增大的是___________。
a.加入少量0.10 mol/L的稀盐酸
b.加热CH3COOH溶液
c.加入少量冰醋酸
d.加水稀释至0.010 mol/L
e.加入少量氯化钠固体
f.加入少量0.10 mol/L的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)__________V(醋酸),反应的最初速率为:
υ(盐酸)_________υ(醋酸)。
(3)常温下,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:Va________Vb;溶液中各离子的浓度按照由大到小排序为_________。
(4)已知:90℃时,水的离子积常数为Kw=38×10‾14,在此温度下,将pH=3的盐酸和pH=11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=____________(保留三位有效数字)。
早期发现的一种天然二十面体准晶颗粒由三种Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)可通过 方法区分晶体、和非晶体。
(2)基态Fe原子有 个未成对电子,Fe3+的电子排布式为 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为 。
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为 ,1mol乙醛分子中含有的σ键的数目为 。乙酸的沸点明显高于乙醛,其主要原因是 。
(4)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g·cm-3(不必计算出结果)。
按要求填空:
(1)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式: 。
(2)金属钠在氧气中充分燃烧,将所得产物投入水中,产物和迅速发生反应,写出该反应的化学方程式: 。向所得溶液中加入FeSO4溶液,看到的现象是: ,此过程中发生的氧化还原反应的化学方程式: 。
(3)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式 。
I. H2A在水中存在以下平衡:H2A  H++HA-,HA-
H++HA-,HA- H++A2-
H++A2-
(1)NaHA溶液显酸性,则溶液中离子浓度的大小顺序为 。
(2)常温时,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性。此时该混合溶液的下列关系中,一定正确的是______________。
| A.c(Na+ )>c(K+ ) | B.c(H +)•c(OH )=1×10-14 |
| C.c(Na+ )=c(K+ ) | D.c(Na+ )+c(K+ )=c(HA- )+c(A2-) |
Ⅱ.含有Cr2O72- 的废水毒性较大,某工厂废水中含4.00×10-3 mol/L Cr2O72-。为使废水能达标排放,作如下处理:

(3)该废水中加入FeSO4•7H2O和稀硫酸,发生反应的离子方程式为: 。
(4)欲使25 L该废水中Cr2O72- 转化为Cr3+,理论上需要加入_________g FeSO4•7H2O。
(5)若处理后的废水中残留的 c(Fe3+)=1×10-13mol/L ,则残留的 Cr3+的浓度为_________。(已知:Ksp[Fe(OH)3]≈1.0×10-38mol,/L ,Ksp[Cr(OH)3]≈1.0×10-31 mol/L )
III.已知:I2+2S2O32-==2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
(6)步骤c中判断恰好反应完全的现象为
(7)根据以上实验和包装袋说明,所测精制盐的碘含量是 mg/kg。(以含w的代数式表示)
在标准状况下充满HCl的烧瓶做完喷泉实验后得到稀盐酸,用标准碳酸钠溶液滴定这种盐酸测定它的准确浓度,请你回答下列问题:
(1)用标准Na2CO3溶液滴定这种盐酸时,Na2CO3溶液应装在__________式滴定管内,若用甲基橙作指示剂,达到滴定终点时,溶液从_________色变为____________色;
(2)现配制三种浓度的标准Na2CO3溶液,你认为最合适的是下列第_____________种(填序号);
①2.500 mol/L ②0.25 mol/L ③0.025mol/L
(3)若采用上述合适浓度的标准Na2CO3溶液滴定,用c(Na2CO 3)表示,滴定时实验数据列表如下:
| 实验编号 |
待测盐酸体积(mL) |
滴入Na2CO3溶液体积(mL) |
| 1 |
20.00 |
18.80 |
| 2 |
20.00 |
16. 95 |
| 3 |
20.00 |
17. 05 |
根据以上数据计算时应带入的Na2CO3溶液体积_______________求这种待测盐酸的物质的量浓度(用数据和符号列式即可):c(HCl)=_________________。
海水的综合利用可以制备金属镁,其流程如下图所示:
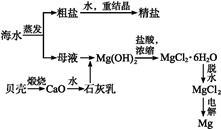
(1)完成下列方程式:
煅烧贝壳(化学方程式): ;
Mg(OH)2加盐酸(离子方程式):
(2)电解熔融MgCl2的反应化学方程式是 。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,分别说明在这3种情况下使用玻璃棒的目的。
溶解时: 。
过滤时: 。
蒸发时: 。
(4)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl和HCl,写出相应反应的化学方程式: 。
把一定质量的镁、铝混合物投入到2 mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入2 mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。
(1)金属铝的质量为____________。
(2)a的取值范围是________________。
(3)盐酸的体积是________mL。
(4) 的最大值是____________。
的最大值是____________。
(5)80~90 mL对应反应的离子方程式________________。
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:

(1)写出工业上制取Cl2的化学方程式_________________________。
(2)在“反应液I”中加入KOH固体的目的是①_________________,②提供碱性环境。
(3)写出Fe(NO3)3溶液与碱性KClO溶液反应的化学方程式: 。
(4)K2FeO4可作为新型多功能水处理剂的原因是:
① ,② 。
(5)从“反应液II”中分离出K2FeO4后,副产品是_________________(写化学式)。
(6)该工艺每得到1.98 kg K2FeO4,理论上消耗Cl2的物质的量为 mol。
常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害.某化学兴趣小组拟采用如图1处理方法回收废电池中的各种资源.
(1)填充物用60℃温水溶解,目的是 .
(2)操作A的名称为 .
(3)铜帽溶解时加入H2O2的目的是 (用化学方程式表示).铜帽溶解完全后,可采用 方法除去溶液中过量的H2O2.
(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为 .
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O.
①当1mol MnO2参加反应时,共有 mol电子发生转移.
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出该应的化学方程式: .
(6)锌锰干电池所含的汞可用KMnO4溶液吸收.在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图2所示:
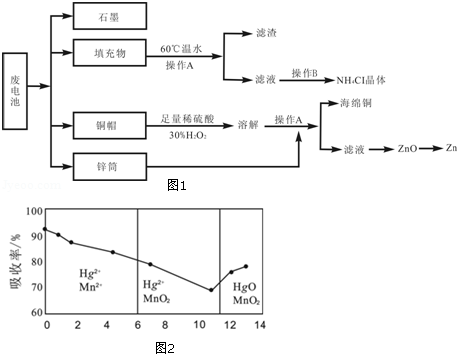
根据图可知:
①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率 .
②在强酸性环境下Hg的吸收率高的原因可能是KMnO4在酸性条件下 强.
维拉左酮是临床上使用广泛的抗抑郁药,其关键中间体合成路线如如:

已知:①
②
(1)反应类型:反应④ 反应⑤
(2)结构简式:A C
(3)写出反应②的化学方程式: 。
实验中反应②必须在碳酸钾弱碱性条件下进行的原因是 。
(4)合成过程中反应③与反应④不能颠倒的理由为 。
(5)反应⑥中,(Boc)2是有由两分子C5H10O3脱水形成的酸酐,写出分子式为C5H10O3,且分子中只含有2种不同化学环境氢原子,能发生水解反应的结构简式(书写2种): 、 。
(6)实验室还可以用 和
和 直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式 。
直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式 。