常温下,在20.0mL 0.20mol/LCH3COONa溶液中滴加0.20mol/L的稀盐酸。溶液的PH值的变化关系如右图所示。

(1) a >7.0的理由是(用离子方程式表示)
(2)如图,当加入稀盐酸的体积为V1mL时,溶液的pH值
刚好为7.0。此时溶液中c(Cl-) c(CH3COOH)
(填<、>或=)。简要写出判断依据
。
(3)当加入的盐酸的体积为20.0mL时,测定溶液中的c(H+)为1.3×10-3 mol/L,求CH3COOH的电离平衡常数Ka(设混合后的体积为二者的体积之和,计算结果保留两位有效数字)。
我们可以通过以下实验步骤来验证醋酸银(CH3COOAg)的溶度积KSP=2.0×10-3:将已知质量的铜片加入到CH3COOAg饱和溶液中(此饱和溶液中没有CH3COOAg固体),待充分反应之后,将铜片冲洗 干净、干燥、称重.
干净、干燥、称重.
(1)写出表示CH3COOAg沉淀溶解平衡的方程式.
(2)刚开始铜片的质量为23.4 g,将铜片放在100 mL的CH3COOAg饱和溶液中,通过 计算说明当充分反应
计算说明当充分反应 后铜片的质量为何值时,CH3COOAg的KSP=2.0×10-3可以得到证实.(
后铜片的质量为何值时,CH3COOAg的KSP=2.0×10-3可以得到证实.(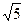 =2.24,
=2.24,  =1.41)
=1.41)
有Fe和Fe2O3的混合物溶于500 mL的稀硝酸中,放出NO气体22.4 L(标准状况)并余5.44 g Fe,过滤,向滤液中通入20.16 L的Cl2(标准状况),恰好能使溶液中的Fe2+全部氧化。求:(1)稀硝酸的物质的量浓度 ;
(2)原混合物中Fe的质量 ,氧化铁的物质的量 。
我国规定饮用水的硬度不能超过25度。硬度的表示方法是:将水中的Ca2+和Mg2+都看作Ca2+,并将其折算成CaO的质量。通常把1升水中含有10mg CaO称为1度。某化学实验小组对本地区地下水的硬度进行检测,实验过程如下:
实验中涉及的部分反应:M2+(金属离子)+EBT(铬黑T) =M EBT
蓝色 酒红色
M2+(金属离子)+Y4-(EDTA) = MY2-
MEBT+Y4-(EDTA) = MY2-+EBT(铬黑T)
⑴取地下水样品25.0毫升进行预处理。已知水中由Ca2+、Mg2+和HCO3-所引起的硬度称为暂时硬度,可通过加热减小硬度,写出加热时所发生的化学反应(任写一个) ▲ 。预处理的方法是向水样中加入浓盐酸,煮沸几分钟,煮沸的目的是 ▲ 。
⑵将处理后的水样转移到250 mL的锥形瓶中,加入氨水-氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.0100 mol·L-1的EDTA标准溶液进行滴定,滴定时眼睛应 ▲ ,滴定终点时的实验现象是 ▲ 。
⑶滴定终点时共消耗EDTA溶液15.0 mL,则该地下水的硬度= ▲ 。
⑷若实验时装有EDTA标准液的滴定管只用蒸馏水润洗而未用标准液润洗,则测定结果将 ▲ (填“偏大”、“偏小”或“无影响”)。
我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。高炉内可能发生如下反应:
C(s)+O2 (g) = CO2(g) △H1=-393.5 kJ·mol—1 ①
(g) = CO2(g) △H1=-393.5 kJ·mol—1 ①
C(s)+CO2(g) = 2CO(g) △H2=+172.5 kJ·mol—1 ②
4CO(g)+Fe3O4(s) = 4CO2(g)+3Fe(s) △H3=-13.7 kJ·mol—1 ③
请回答下列问题:
⑴计算3Fe(s)+2O2(g) = Fe3O4(s)的△H= ▲ 。
⑵800℃时,C(s)+CO2(g) 2CO(g)的平衡常数K=1.64,相同条件下测得高炉内c(CO)=0.20mol·L-1、c(CO2)=0.05mol·L-1,此时反应向 ▲ (填“正”或“逆”)方向进行。
2CO(g)的平衡常数K=1.64,相同条件下测得高炉内c(CO)=0.20mol·L-1、c(CO2)=0.05mol·L-1,此时反应向 ▲ (填“正”或“逆”)方向进行。
⑶某种矿石中铁元素以氧化物FemOn形式存在,现进行如下实验:将少量铁矿石样品粉碎,称取25.0 g样品于烧杯中,加入稀硫酸充分溶解,并不断加热、搅拌,滤去不溶物。向所得滤液中加入10.0 g铜
粉充分反应后过滤、洗涤、干燥得剩余固体3.6 g。剩下滤液用浓度为2mol·L-1的酸性KMnO4滴定,至终点时消耗KMnO4溶液体积25.0 mL。
提示:2Fe3++Cu=2Fe2++Cu2+ 8H++MnO4-+5Fe2+=Mn2++5Fe3++4H2O
①计算该铁矿石中铁元素的质量分数。
②计算氧化物FemOn的化学式(m、n为正整数)
现有一种碱金属的碳酸盐(M2CO3)和碳酸氢钠组成的混合物,取其1.896g加热至质量不再变化,把放出的气体通入足量的澄清石灰水中,得到白色沉淀0.800g。将加热后残留的固体与足量稀硫酸充分反应,生成的气体经充分干燥后通过足量的过氧化钠粉末,结果过氧化钠粉末增重0.336 g。
(1)试通过计算确定M2CO3的M为何种元素。
(2)有同学提出,通过简单的定性实验,也可以确定该样品中的M为何种碱金属元素。你认为该实验方案是什么?
取一定量的CuO粉末与0.5 L稀硫酸充分反应后,将一根50 g铁棒插入上述溶液中,至铁棒质量不再变化时,铁棒增重0.24 g, 并收集到224 mL气体(标准状况)。求此CuO粉末的质量。
工业上用饱和电解食盐水来制取氯气。现取500mL 含NaCl为11.7g的饱和食盐水进行电解。
⑴在标准状况下制得Cl2多少升?
⑵所得NaOH的物质的量浓度为多少?(电解前后溶液体积保持不变)
随着石油资源的日趋紧张,天然气资源的转化利用越来越受到人们的关注。下图是最近研发出的天然气利用新途径:首先甲烷在催化剂作用下发生“氧氯化反应”生成一氯甲烷;然后一氯甲烷在400°C的条件下通过分子筛催化转化为低碳烯烃。
请根据以上信息回答下列问题:
(1)第一轮次反应投料时甲烷和氯化氢的最佳体积比(相同条件)为 。
(2)由一氯甲烷生成丙烯的化学方程式为 。
(3)按最佳反应投料比,若该途径中的第一步“甲烷氧氯化反应”的转化率为80%,经除水、分离出混合物中的一氯甲烷后,剩余CH4、O2和HCl全部留用并投入第二轮次生产;第二步一氯甲烷反应生成含有乙烯、丙烯、丁烯和氯化氢的混合气体,碳原子的利用率为90%,分离出其中的烯烃气体后,剩余HCl也全部留用并投入第二轮次生产,则:
①标准状况下,1m3甲烷经过一轮反应可得到 kg乙烯、丙烯、丁烯的混
合气体。
②为了与第一轮次得到的等量的低碳烯烃,第二轮次反应投料时,需补充的CH4、
O2和HCl的体积比为(相同条件) 。(请写出①和②的计算过程)
[化学选修—物质结构与性质]
已知A、B、C、D和E 5种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子。又知B、C和D是由两种元素的原子组成。请回答:
(1)组成A分子的原子的核外电子排布式是___________________________;
(2)B和C的分子式分别是__________和__________;C分子的立体结构呈_______形,该分子属于__________分子(填“极性”或“非极性”);
(3)若向D的稀溶液中加入少量二氧化锰,有无色气体生成。则D的分子式是 ,该反应的化学方程式是______________________________________________。
(4)若将1 mol E在氧气中完全燃烧,只生成1 mol CO2和2 mol H2O,则E的分子式是_____________。
化学世界里有许多“另类”的物质。如亚铁盐在空气中通常不稳定,易被氧化,如FeSO4·7H2O。而(NH4) 2Fe(SO4)2·6H2O晶体比FeSO4·7H2O晶体等其它亚铁盐稳定许多,可在分析化学中做基准试剂。常温下FeSO4·7H2O在空气中容易失去结晶水成为FeSO4,而(NH4) 2Fe(SO4)2.·6H2O失去结晶水困难许多。
FeSO4·7H2O的晶胞参数为a=1.407nm,b=0.6503nm,c=1.104nm,α=γ=90.00°,β=105.57°密度为1.898g/cm3,无水FeSO4晶体中最近的Fe—O距离为0.212nm,S—O距离为0.151nm,Fe—S距离为0.475nm,Fe—Fe距离为0.769nm,(NH4) 2Fe(SO4)2·6H2O的晶胞参数为a=0.932nm,b=1.265nm,c=0.624nm,α=γ=90.00°,β=106.80°,密度为1.864g/cm3,最近的Fe—O距离0.209nm,S—O距离为0.149nm,Fe—Fe距离为0.486nm,NH4+—Fe距离为0.483nm,N—S距离为0.361nm
⑴ 计算一个FeSO4·7H2O晶胞和一个(NH4) 2Fe(SO4)2·6H2O晶胞分别所含原子个数
⑵ 晶体自身的结构如空隙大小直接影响化学反应进行的趋势,试通过计算说明
FeSO4·7H2O比(NH4) 2Fe(SO4)2.·6H2O更易被氧化
已知:O的共价半径为0.66nm,在晶体中+2价的Fe半径为0.061nm,—2价的O半径为0.121nm,+6价的S半径为0.029nm,—3价的N半径为0.148nm
⑶ FeSO4·7H2O在潮湿的空气中被氧化的产物为Fe(OH)SO4·3H2O,写出反应的化学方程式
_____________________________________________________________
⑷ 在水溶液中(NH4) 2Fe(SO4)2·6H2O与FeSO4·7H2O稳定性相当,请分析其原因
维生素C又称抗坏血酸,广泛存在于水果、蔬菜中,属于外源性维生素,人体不能自身合成,必须从食物中摄取。其化学式为C6H8O6,相对分子量为176.1,由于分子中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,半反应为:
C6H8O6=C6H6O6+2H++2e jy=0.18V
因此,可以采用碘量法测定维生素C药片中抗坏血酸的含量。具体实验步骤及结果如下:
(1)准确移取0.01667mol/L的K2Cr2O7标准溶液10.00mL于碘量瓶中,加3mol/L H2SO4溶液10mL,10% KI溶液10mL,塞上瓶塞,暗处放置反应5min,加入100mL水稀释,用Na2S2O3标准溶液滴定至淡黄色时,加入2mL淀粉溶液,继续滴定至溶液由蓝色变为亮绿色。平行三次实验,消耗Na2S2O3标准溶液平均体积为19.76mL。
(2)准确移取上述Na2S2O3标准溶液10.00mL于锥瓶中,加水50mL,淀粉溶液2mL,用I2标准溶液滴定至蓝色且30s不褪。平行三次实验,消耗I2标准溶液平均体积为10.15mL。
(3)准确称取0.2205g的维生素C粉末(维生素C药片研细所得)于锥瓶中,加新煮沸过并冷却的蒸馏水100mL,2 mol/L HAc溶液10mL,淀粉溶液2mL,立即用I2标准溶液滴定至蓝色且30s不褪,消耗12.50mL。
(4)重复操作步骤(3),称取维生素C粉末0.2176g,消耗I2标准溶液为12.36mL;称取维生素C粉末0.2332g,消耗I2标准溶液为13.21mL。
根据以上实验结果计算出该维生素C药片中所含抗坏血酸的质量分数。
NO2-是一种常见配体,在八面体配离子[MR2(NO2)4]-中,中心离子M含量为21.27%,氮元素的含量为30.33%,只检测到一种N-O键长,请回答下列问题
⑴ 给出自由状态下的NO2-的结构,NO2-在该配合物中配位方式
⑵ 通过计算,给出配离子的化学式和名称
⑶ 画出该配离子的结构
在900℃的空气中合成出一种含镧、钙和锰 (摩尔比2 : 2 : 1) 的复合氧化物,其中锰可能以 +2、+3、+4 或者混合价态存在。为确定该复合氧化物的化学式,进行如下分析:
⑴ 准确移取25.00 mL 0.05301 mol·L-1的草酸钠水溶液,放入锥形瓶中,加入25 mL蒸馏水和5 mL 6 mol·L-1的HNO3溶液,微热至60~70oC,用KMnO4溶液滴定,消耗27.75 mL。写出滴定过程发生的反应的方程式;计算KMnO4溶液的浓度。
⑵ 准确称取0.4460 g复合氧化物样品,放入锥形瓶中,加25.00 mL上述草酸钠溶液和30 mL 6 mol·L-1的HNO3溶液,在60~70oC下充分摇动,约半小时后得到无色透明溶液。用上述KMnO4溶液滴定,消耗10.02 mL。根据实验结果推算复合氧化物中锰的价态,给出该复合氧化物的化学式,写出样品溶解过程的反应方程式。已知La的原子量为138.9。