甲醛是一种重要的化工产品,可利用甲醇脱氢制备,反应式如下:
CH3OH(g) 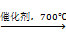 CH2O(g) + H2(g)
CH2O(g) + H2(g) 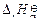 =" 84.2" kJ·mol-1 ⑴
=" 84.2" kJ·mol-1 ⑴
向体系中通入空气,通过以下反应提供反应(1) 所需热量:
H2(g) + 1/2O2(g)=H2O(g) 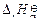 =" –241.8" kJ·mol-1 (2)
=" –241.8" kJ·mol-1 (2)
要使反应温度维持在700℃,计算进料中甲醇与空气的摩尔数之比。已知空气中氧气的体积分数为0.20。
甲醛是一种重要的化工产品,可利用甲醇脱氢制备,反应式如下:
CH3OH(g) 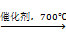 CH2O(g) + H2(g)
CH2O(g) + H2(g) 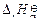 =" 84.2" kJ·mol-1 ⑴
=" 84.2" kJ·mol-1 ⑴
向体系中通入空气,通过以下反应提供反应(1) 所需热量:
H2(g) + 1/2O2(g)=H2O(g) 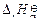 =" –241.8" kJ·mol-1 (2)
=" –241.8" kJ·mol-1 (2)
要使反应温度维持在700℃,计算进料中甲醇与空气的摩尔数之比。已知空气中氧气的体积分数为0.20。