现用Zn与实验室中的盐酸反应制取4.48L H2(标准状况)。
(1)求消耗得锌的质量为多少克?
(2)如果选用所贴标签为2.0mol·L-1的盐酸,至少需该盐酸多少毫升?
(3)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升?(Zn+2HCl = ZnCl2+H2)
将0.1mol某烃的衍生物与标准状况下4.48L氧气混合密闭于一容器中,点火后发生不完全燃烧,得到CO2、CO和H2O的气态混合物。将混合气体通过浓硫酸时,浓硫酸质量增加了3.6g,通过澄清石灰水时,可得到沉淀10g (干燥后称量)。剩余气体与灼热的氧化铁充分反应后再通入澄清的石灰水中,又得到20g固体物质(干燥后)。
求:(1)该有机物的分子式。
(2)该有机物可与醇发生酯化反应,且可使溴水褪色,写出有机物的结构式。
实验室常用加热高锰酸钾的方法制取少量氧气。
(1)请写出反应的化学方程式
(2)现欲制取2.24L(标准状况)的氧气,需要消耗高锰酸钾多少克?
(3)生成的二氧化锰的物质的量是多少?
试回答下列问题:
(1) 9g 水的物质的量是________mol,含有_______mol 氢原子,含有__________个电子。
(2)等物质的量的SO2和SO3所含的原子个数之比是__________,质量比是__________。
(3)0.4mol NH3中所含氢原子数与__________克水中所含氢原子数相等。
(4)质量分数为49%的硫酸溶液,其密度为1.4 g/cm3,则其物质的量浓度为__________。
(5) 在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-完全沉淀;若加入足量NaOH 并加热可得到c mol NH3,则原溶液中Al3+的物质的量浓度为_________。
(8分)用KMnO4氧化密度为1.19g·cm-3溶质质量分数为36.5%的HCl溶液。反应方程式如下:
2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O(写出计算过程)
(1)所用HCl溶液的物质的量浓度是多少?
(2)15.8gKMnO4能使多少克HCl发生上述反应?有多少克HCl被氧化?
(3)若Cl2在标准状况下的密度为3.17g·L-1,则产生的Cl2在标准状况下的体积为多少?
把铝、铁混合物 1.1 g 溶于200 mL 5 molL -1 盐酸中,反应后盐酸的浓度变为4.6 molL -1 (溶液体积变化忽略不计)。
求:(1)反应中消耗HCl的物质的量。
(2)该混合物中铝、铁的物质的量。
分取100mLNa2CO3和NaSO4的混合溶液,加入过量BaCl2溶液后得到14.51克白色沉淀,用过量稀盐酸处理后沉淀量减少到4.66克,并有气体放出,试计算:
(1)原混合液中Na+的物质的量浓度.
(2)用离子方程式表示产生气体的化学反应,计算标准状况下气体的体积。
将一定质量的Mg、Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得下图关系。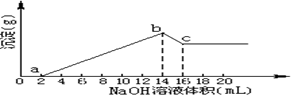
(1)求Mg,Al质量各是多少?考查镁铝化合物性质、混合物的计算,
(2)求盐酸的物质的量浓度为多少mol/L?
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等.回答下列问题:
(1)写出基态As原子的核外电子排布式________.
(2)根据元素周期律,原子半径Ga________As,第一电离能Ga________As.(填"大于"或"小于")
(3) 分子的立体构型为________,其中As的杂化轨道类型为________.
(4) 的熔点高于1000℃, 的熔点为77.9℃,其原因是________.
(5)GaAs的熔点为1238℃,密度为 , 其晶胞结构如图所示.
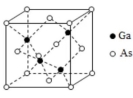
该晶体的类型为________,Ga与As以________键键合.Ga和As的摩尔质量分别为 和 , 原子半径分别为 和 ,阿伏伽德罗常数值为 ,则GaAs晶胞中原子的体积占晶胞体积的百分率为________.
0.1mol某烃的衍生物与0.35mol氧气混合密闭于一容器中,点火后发生不完全燃烧,得到CO2、CO和H2O的气态混合物。将混合气体通过浓硫酸时,浓硫酸质量增加了5.4g,通过足量澄清石灰水时,可得到沉淀20g(干燥后称量)。剩余气体与灼热的氧化铁充分反应后再通入足量澄清的石灰水中,又得到20g固体物质(干燥后)。
求:(1)该有机物的分子式。
(2)该有机物可与醇发生酯化反应,且可使溴水褪色,写出该有机物可能的结构简式和名称。
将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
(1)按顺序写出OA 段所发生反应的离子方程式_______________________。
(2)加人35mL盐酸时,产生二氧化碳的体积为___________mL
(3)计算原混合物中Na2CO3的质量(要求写出计算过程)
计算题:将0.2molMg、Al的混合物用盐酸完全溶解,放出标准状况下5.6L气体,然后再滴入2mol/LNaOH溶液,请回答:
(1)求该混合物中Mg、Al的物质的量?(写计算过程)
(2)若该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V= ml。
(3)若该Mg、Al混合物溶于200ml 3mol/L盐酸后,滴入NaOH溶液,使所得沉淀中无Al(OH)3,则滴入NaOH溶液的体积最少为 ml。
将一定质量的镁、铝合金,投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加5 mol/L NaOH溶液,生成的沉淀质量与加入NaOH溶液体积如图所示,由图中数据分析计算:

(1)原合金中镁的质量为 ;
(2)盐酸的物质的量浓度为 。
(1)在标准状况下4.48L CH4和CO2混合气体的质量为6.0g,则混合气体平均摩尔质量为 g/mol,相对于氢气的密度为 ;CH4和CO2的质量比为 .
(2)相同体积、相同物质的量浓度的AgNO3溶液,分别与相同体积的KCl、CuCl2、AlCl3溶液反应恰好完全反应,则KCl、CuCl2、AlCl3三种溶液的物质的量浓度之比为 。
(3)标准状况下,V L的某气体(摩尔质量为M g•mol﹣1)溶解在1L水(水的密度近似为1g•cm﹣3)中,假设气体完全溶解且不与水发生反应,溶液的密度为ρg•cm﹣3,则所得溶液的物质的量浓度c= mol/L.(选择以上字母表达计算式,要求化简).