空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是
A.转移0.1mol电子时,a电极产生标准状况下O2 1.12L
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
下述实验不能达到预期实验目的的是
| 序号 |
实验内容 |
实验目的 |
| A |
室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1 mol·L-1CH3COONa溶液的pH |
比较HClO和CH3COOH的酸性强弱 |
| B |
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 |
说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C |
向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生 |
验证两者都发生了水解反应,且相互促进 |
| D |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究浓度对反应速率的影响 |
亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图所示。下列有关叙述正确的是
| A.亮菌甲素分子式为C12H11O5 |
| B.亮菌甲素能与三氯化铁溶液发生显色反应 |
| C.1mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗2mol NaOH |
| D.每个亮菌甲素分子在一定条件下与足量H2反应后的产物有3个手性碳原子 |
下列图示与对应的叙述相符的是
| A.图Ⅰ表示盐酸滴加到0.1 mol/L某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 |
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| D.图Ⅳ表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
用NA表示阿伏加德罗数的值。下列叙述正确的是
| A.电解饱和食盐水,当阴极产生2.24L H2时,转移的电子数一定为0.2NA |
| B.0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氧原子数为0.3 NA |
下列离子方程式书写正确的是
A.用铜片作阴、阳极电解硝酸银溶液:4Ag +2H2O +2H2O 4Ag+O2↑+4H 4Ag+O2↑+4H |
| B.向Na2SO3、NaI的混合溶液中滴加少量氯水:2I—+C12="=2" Cl—+I2 |
C.向水杨酸中加入适量Na2CO3溶液: +CO32- → +CO32- → +CO2↑+H2O +CO2↑+H2O |
| D.AgCl沉淀在氨水中溶解:AgCl+2NH3·H2O ==Ag(NH3)2++Cl-+2H2O |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.饱和氯水中:Cl-、NO3-、Na+、CO32- |
| B.c(H+)=1.0×10-13 mol·L-1的溶液中:C6H5O-、K+、SO42-、Br- |
| C.酚酞呈红色的溶液中:SO42-、 K+、Cl-、HSO3- |
| D.pH=2的溶液中:NO3-、I-、Na+、Al3+ |
已知反应:2 E (l)  U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。则下列说法正确的是( )
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。则下列说法正确的是( )
| A.该反应的∆H > 0 |
| B.b代表50℃下E的Y-t曲线 |
| C.m点(66,0.113)时有: ∆n (E, 20℃) = ∆n (E,50℃) |
| D.升高温度可以缩短达到平衡的时间,提高E的转化率 |
铅的冶炼大致过程如下:
①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2 2PbO+2SO2;
2PbO+2SO2;
③制粗铅:PbO+C Pb+CO;PbO+CO
Pb+CO;PbO+CO Pb+CO2。
Pb+CO2。
下列说法正确的是( )
| A.浮选法富集方铅矿的过程属于化学变化 |
| B.方铅矿焙烧反应中,PbS是还原剂,发生还原反应 |
| C.过程②中,制取1molPbO共转移2mol电子 |
| D.将1molPbS冶炼成Pb理论上至少需要6g碳 |
右图是模拟电化学反应装置图。下列说法正确的是( )
| A.若X为碳棒,开关K置于N处,会加快铁的腐蚀 |
| B.若X为锌,开关K置于N处,则X极上有黄绿色气体生成 |
| C.若X为碳棒,开关K置于M处,则铁电极的电极反应式为:Fe-3e-=Fe3+ |
| D.若X为锌,开关K置于M处,则总反应方程式为:2Zn+O2+2H2O=2Zn(OH)2 |
下列溶液中,微粒的物质的量浓度关系一定正确的是( )
A.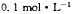 的硫化钾溶液中: 的硫化钾溶液中: |
B.常温下,pH=7的CH3COOH与CH3COONa的混合液中: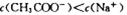 |
C.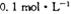 的NH4Cl溶液中: 的NH4Cl溶液中: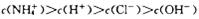 |
D.pH=3的一元酸和pH=11的一元强碱等体积混合: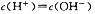 |
化学中常用图像直观地描述化学反应的进程或结果。下列对图像描述正确的是
A.根据图①可判断可逆反应 “ A2(g)+3B2(g) 2AB3(g)” 的ΔH>0 2AB3(g)” 的ΔH>0 |
B.图②表示压强对可逆反应2A(g)+ 2B(g) 3C(g)+ D(s)的影响,乙的压强大 3C(g)+ D(s)的影响,乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.图④是N2与H2合成氨的能量变化曲线,可确定该反应1 mol N2和3 mol H2充分反应时放热一定小于92 kJ |
能正确表示下列反应的离子方程式的是( )
| A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合: Ba2+ +2OH− + NH4+ + HCO3−=BaCO3↓+NH3∙H2O + H2O |
| B.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| C.向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O |
| D.碳酸氢铵溶液中加入少量NaOH:NH4+ + OH- = NH3·H2O |
常温下,下列溶液中可能大量共存的离子组是( )
| A.水电离产生的c(H+)=1×10-12mol/L的溶液中:AlO2-、S2-、PO43-、Na+ |
| B.加入金属镁能产生H2的溶液中:Na+、HCO3-、SO42-、Al3+ |
| C.能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、CO32- |
| D.含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42- |