有A、B、C、D四种无色溶液,它们分别是Na2CO3、Na2SO4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为::①A+D→溶液+气体,②B+C→溶液+沉淀,
③B+A→溶液+沉淀X,④D+B→溶液Y+沉淀,⑤溶液Y+沉淀X→溶液+气体.
(1)根据以上记录确定:A__________ B___________ C___________ D___________
(2)写出①、③各反应的离子方程式:
①_______________③______________
有甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、CO32-、SO42-中的不同阴、阳离子各一种组成,已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)它们的化学式分别为甲_________、乙_________、丁_________。
(2)写出甲溶液和丁溶液反应的离子方程式:_________________________。
(3)检验乙中阴离子所用试剂的名称是____________________。
已知某溶液中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:
①取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;②将沉淀过滤、洗涤、灼烧,得到1.6 g固体;
③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。
请回答下列问题:
(1)结合①和②,判断原溶液中肯定含有的离子是 ,可以排除的离子是 。
(2)由③推知原溶液中一定有 离子,其物质的量为 mol。
(3)综合(1)、(2)及题干信息,结合溶液中电荷守恒知识,还可以排除的离子是 。该学习小组最终得出结论:该溶液由 种阳离子(填数字,下同)和 种阴离子组成。
有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,现做以下实验:
(1)将部分粉末加水中,振荡,有白色沉淀生成;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
(3)取少量(2)的溶液滴入AgNO3溶液,有白色沉淀生成。
根据上述实验现象,判断原白色粉末中肯定含有什么物质,可能含有什么物质,写出各步反应的离子方程式。肯定有____________;可能含有____________
离子方程式:
(1)____________________________
(2)____________________________
(3)____________________________
某溶液含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下(请写出最佳答案):
(1)所加试剂的化学式:A_________、B__________、C__________
(2)写出生成沉淀1的离子方程式_________________________;生成沉淀3的离子方程式_____________________________;
(3)试猜想上述溶液中一定存在的另一种离子是________(写化学式),请写出该离子所对应的一种盐的电离方程式__________________。
有一包白色固体粉末,可能含有K2SO4、Na2CO3、NH4Cl、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
①取少量固体粉末加到足量水中,得到无色溶液;
②取①中溶液少量继续往其中加入足量稀硫酸,有气泡产生;
③继续向②中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成;
④取①中溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝。
根据以上事实判断:
(1)肯定存在的是 ;
(2)肯定不存在的是_____________________;
(3)不能确定是否存在的是 。请简述证明该物质是否存在的实验方案(实验方法、现象、结论) 。
(4)写出上述实验④中产生刺激性气味气体反应的化学方程式:____________________。
现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液.相应过程用如图表示:
(1)写出下列物质的化学式X__________;
(2)写出步骤③涉及到的离子反应__________,__________;
(3)按此实验方案得到的溶液3中肯定含有杂质,为了解决这个问题,可以向溶液3中加入适量的__________(填化学式),之后若要获得固体NaNO3需进行的实验操作是__________(填操作名称).
人类的生产生活离不开金属材料,金属及金属材料在生产、生活中应用广泛。
(1)生活中常用的铁锅炒菜,主要是利用了铁的 ;铁在潮湿的空气中容易锈蚀,喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝 ,喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,写出其中涉及到的一个化学方程式: 。
(2)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:

①A、B、C三种金属的活动性顺序为 。
②金属C是 ,已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式: 。
现有失去标签的四瓶无色溶液分别为Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示。
| 实验顺序 |
实验内容 |
实验现象 |
| ① |
A + B |
生成白色沉淀 |
| ② |
A + C |
放出无色气体 |
| ③ |
A + D |
放出无色气体 |
| ④ |
B + C |
无明显变化 |
| ⑤ |
B + D |
生成白色沉淀 |
| ⑥ |
C + D |
无明显变化 |
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4 = Na+ + H+ + SO42- 。
根据实验现象,回答下列问题:
(1)A为 ,C为 。
(2)写出下列反应的离子方程式
A + B ,A + D ,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为 ,反应后得到的溶液中含有的阴离子有 。
(4)上述没有明显变化的实验④、⑥,其中 发生了离子反应,离子方程式为 。请设计实验证明其发生了反应 。(试剂任选)
实验室有四瓶失去试剂标签的无色溶液,已知它们是K2CO3溶液、稀硫酸、Ba(OH)2溶液和MgCl2溶液。为了确定每种试剂的成分,现将它们编号为A、B、C、D,两两混合后出现如下现象:A+B→气体,A+C→沉淀,A+D→沉淀,C+B→沉淀(提示:MgCO3微溶物,量大时视作沉淀)
(1)请判断各试剂的成分(写化学式)
A_________ B_________ C_________ D_________
(2)请写出相应的化学方程式
A+C:_____________________________________________
C+B:_____________________________________________
现有四瓶贴有A、B、C、D标签的溶液,它们可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液。现进行如下实验,并记录部分现象(如下图):
据此完成下列回答:
(1)写出各物质的化学式
A、 B、
C、 D、
(2)写出下列反应的离子方程式:
A + B反应:
沉淀a+溶液b:
(3)检验物质D中阴离子的方法为 (说明实验操作、现象与结论等)。
(7分)某待测溶液中可能含有SO42-、SO32-、CO32-、HCO3-、NO3-、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出)。
请回答下列问题:(1)根据上述框图信息填写下表(不能确定的不填):
| |
肯定存在的离子 |
肯定没有的离子 |
| 化学式或离子符号 |
|
|
(2)写出沉淀A三种可能的情况:______________________________,若气体D遇空气变红棕色,则生成沉淀D时肯定发生的反应的离子方程式为 。
(3)若Mn+位于第三周期,则要确定它具体是何种离子的方法是_____________________。
下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D、E为无色气体,C能使湿润的红色石蕊试纸变蓝,B常温下为无色液体,X是一种酸式盐。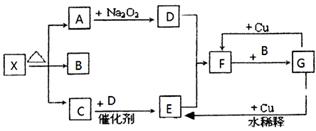
(1)写出下列各物质的化学式:X: ;F: ;G: 。
(2)利用Na2O2与A反应常作供氧剂,写出其反应方程式: 。写出G→E的化学反应方程式: 。
(3)E→F的实验现象是 ,G的稀溶液与少量Fe粉反应的离子方程式为 ,检验反应后溶液中金属阳离子的试剂为 ,实验现象为 。
(4)F→G的反应 (填是或不是)氧化还原反应,若是,则氧化产物是 ,若不是,则此空不填。
A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去)。
(1)若A为强碱溶液,其焰色反应显黄色,C常用作食品添加剂,请回答下列问题:
①D的化学式是 。
②反应Ⅲ的离子方程式是 。
③现有B和C的固体混合物 g,加热至质量不再改变时剩余固体为
g,加热至质量不再改变时剩余固体为 g,则B的质量分数为 。
g,则B的质量分数为 。
(2)若A、D均为单质,且A为黄绿色气体,D的一种红棕色氧化物常用作颜料,则:
①反应Ⅱ的离子方程式是 。
②取少许C溶液于试管中,滴入NaOH溶液并振荡,发生反应的化学方程式为:
, 。
③检验B溶液中金属阳离子的方法是 。
已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。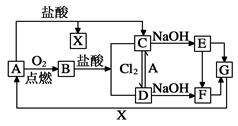
(1)写出A、C、F、G的化学式:A ,C ,F ,G 。
(2)检验D中阳离子的方法 。
(3)保存C溶液时为什么要加固体A 。
(4)写出下列转化的离子方程式C→D: 。