Ⅰ.下列实验操作中正确的是
| A.分液时,分液漏斗下层液体从下端放出,上层液体从上口倒出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.蒸发结晶时应将溶液直接蒸干 |
| D.称量非腐蚀性药品应放在托盘天平左盘的称量纸上,砝码放在托盘天平右盘的称量纸上 |
Ⅱ.影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究。他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素。甲同学的实验报告如下表:
| 实验步骤 |
现象 |
结论 |
| ①分别取等体积2mol/L的硫酸于试管中 ② |
Mg产生气泡速率快于Fe,Cu无明显变化 |
金属性质越活泼,反应速率越快 |
(1)甲同学表中实验步骤②为 。
(2)甲同学的实验目的是探究 。
乙同学为了更精确地研究浓度对反应速率的影响,利用下图所示装置进行定量实验。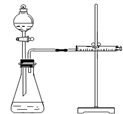
(3)乙同学在实验中应该测定的数据是 。
(4)乙同学完成实验应选用的实验药品是 。
下图中的实验装置可以用于实验室制取乙炔。请填空:
(1) 图中A管的作用是 ,
制取乙炔的化学反应方程式为 。
(2)乙炔通入酸性KMnO4溶液中,发生 反应,可以观察到
现象,若通入溴水中,发生 反应。
(3)乙炔燃烧的化学方程式为 ,燃烧时的现象为 ,
为了安全,点燃乙炔前应该先 。
现有A、B、C、D、E五种易溶于水的强电解质,它们由如下离子组成(各种离子不重复)。
| 阳离子 |
H+、NH4+、Mg2+、Ba2+、Al3+ |
| 阴离子 |
OH-、Cl-、HCO3-、NO3-、SO42- |
已知:①0.1 mol/L A溶液的pH <1;②将B溶液分别与其它四种溶液混合,均有白色沉淀生成;
③C溶液 白色沉淀。请回答下列问题:
白色沉淀。请回答下列问题:
(1)写出下列物质的化学式:A______________、B______________。
(2)写出“C溶液 白色沉淀”有关反应的离子方程式____________________________。
白色沉淀”有关反应的离子方程式____________________________。
(3)D、E两种物质中必有一种是_______________,写出将少量该物质的溶液滴加到B溶液中反应的离子方程式___________________________________________________________________。
(4)请你设计实验确定C及另一种未知物各是什么物质。(只许在A~E中选择检验试剂)
| 实验步骤 |
预期现象和结论 |
| 取适量C的溶液于试管中, ① 。 |
预期现象和结论1: ② ; 预期现象和结论2: ③ ; |
某化学课外小组用如图所示装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式________________。
(2)观察到A中的现象是____________________________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________________,写出有关的化学方程式___________________。
(4)C中盛放CCl4的作用是____________________。
(5)若证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入__ _,现象是_______________________ 。
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
(1)为完成上述实验,正确的连接顺序为_______ 接A, B接_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为 。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液及对应的现象是 。
(4)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
请你分析并回答:你认为不合理的方案及其不足之处是 。
②按测得结果更准确的方案进行计算,Cu的相对原子质量 。
下列各项实验操作正确的是( )
| A.使C2H5Br和NaOH溶液混合后水解,取上层清液,滴加AgNO3溶液检验溴元素 |
| B.为增强高锰酸钾溶液的氧化性,可用盐酸将高锰酸钾溶液酸化 |
| C.将苯与溴水混合后,再加铁粉,即可制得溴苯 |
| D.在测定盐酸和氢氧化钠溶液反应的中和热时,氢氧化钠溶液应过量 |
为了探究的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.的氧化性
将光亮的铁丝伸入溶液中,一段时间后将铁丝取出。为检验溶液中
的氧化产物,将溶液中的
除尽后,进行了如下实验。可选用第试剂
溶液、
溶液、氯水。
(1)请完成下表:
| 操作 |
现象 |
结论 |
| 取少量除尽 |
存在 |
|
| 取少量除尽 |
存在 |
【实验结论】的氧化产物为存在
和
Ⅱ. 的热稳定性性
用下图所示的实验装置A加热固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束以后,试管中残留固体为黑色。

(2)装置B的作用是
(3)经小组讨论并验证该无色气体为,其验证方法是
(4)【查阅资料】和粉末的
均为黑色;
可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:ⅰ;ⅱ.
;ⅲ.
和
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验。
| 实验编号 |
操作 |
现象 |
| a |
加入足量氨水,振荡 |
黑色固体不溶解 |
| b |
加入足量稀硫酸,振荡 |
黑色固体溶解,并有气体产生 |
【实验评价】根据上述实验,不能确定固体产物成分的实验是(填实验编号)。
【实验结论】根据上述实验结果,该小组得出的固体热分解的产物有。
固体硝酸盐加热易分解且产物较复杂。某学习小组以为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:、
、
乙:
、
、
丙:
、
丁:
、
、
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是。
查阅资料得知:2+2
=
+
+
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
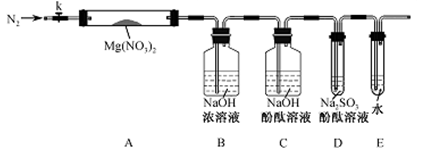
(2)实验过程
①取器连接后,放人固体试剂之前,关闭,微热硬质玻璃管(
),观察到
中有气泡连续放出,表明
②称取固体3 .79
置于
中,加热前通人
以驱尽装置内的空气,其目的是;关闭K,用酒精灯加热时,正确操作是先然后固定在管中固体部位下加热。
③观察到 中有红棕色气体出现,
、
中未见明显变化。
④待样品完全分解, 装置冷却至室温、称量,测得剩余固体的质量为1 . 0
⑤取少量剩余固体于试管中,加人适量水,未见明显现象。
(3)实验结果分析讨论
① 根据实验现象和剩余固体的质量经分析可初步确认猜想是正确的。
② 根据无明显现象,一位同学认为不能确认分解产物中有
,因为若有
,
中将发生氧化还原反应:(填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有
存在,未检侧到的原因是。
③ 小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究。
某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
_____________ 、_____________ 相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为 。
(2)①若用Fe、Cu作电极设计成原电池,以确定Fe、Cu的活动性。试在下面方框中画出原电池装置图,标出原电池的电极材料和电解质溶液。
上述装置中正极反应式为 。
②某小组同学采用Al、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用 。
| A.0.5 mol·L-1氯化亚铁溶液 | B.0.5 mol·L-1氯化铜溶液 |
| C.0.5 mol·L-1盐酸 | D.0.5 mol·L-1氯化亚铁和0.5 mol·L-1氯化铜混合溶液 |
(3)利用提供的试剂和用品:0.1 mol·L-1盐酸溶液、0.1 mol·L-1醋酸溶液、0.5 mol·L-1氯化铝溶液、0.5 mol·L-1氢氧化钠溶液、PH试纸。
请设计最简单实验证明氢氧化铝为弱碱
已知某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有 元素;
假设2 该混合金属粉末中除铝外还含有 元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答)。
(3)实验过程
根据(2)的实验方案,完成实验操作、预期现象和结论的有关问题。
| 编号 |
实验操作 |
预期现象 |
结论 |
| ① |
用药匙取少许样品,加入试管A中,再用滴管取过量NaOH溶液并滴加到试管A中,充分反应后,静置,弃去上层清液,剩余固体备用 |
样品部分溶解,并有气体放出 |
|
| ② |
往试管A的剩余固体中加过量稀硫酸,充分反应后,静置。取上层清液于试管B中,剩余固体备用 |
固体部分溶解,并有气体放出,溶液呈浅绿色 |
可能含 (填元素名称,以下同) |
| ③ |
往试管B中加入少许稀硝酸,再滴加KSCN溶液 |
溶液先变黄色,加KSCN后显 |
结合②可知,一定含 |
| ④ |
往②剩余固体中加入稀硝酸,再滴加NaOH溶液 |
固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有 沉淀产生。 |
一定含 。 |
实验室用NaOH固体配制250 mL 1.25 mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250 mL 1.25 mol/L的NaOH溶液
| 应称取NaOH的质量/g |
应选用容量瓶的规格/mL |
除容量瓶外还需要的其它玻璃仪器 |
| |
|
|
(2)容量瓶上需标有以下五项中的 ;
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A、用30 mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30 mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是 ,溶液注入容量瓶前需恢复到室温,这是因为_____________________________;
(5)下列配制的溶液浓度偏低的是 ;
A、称量NaOH时,砝码错放在左盘
B、向容量瓶中转移溶液时(实验步骤②)不慎有液滴洒在容量瓶外面
C、加蒸馏水时不慎超过了刻度线
D、定容时俯视刻度线
E、配制前,容量瓶中有少量蒸馏水
某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大 ,
原因是 。
(2)哪一段时段的反应速率最小 ,原因是
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率 。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:你认为可行的是(填编号) 。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
下列有关Na2CO3和NaHCO3性质的比较中,正确的是( )
| A.等浓度的溶液中滴入稀盐酸,放出气体的快慢Na2CO3<NaHCO3 |
| B.热稳定性Na2CO3<NaHCO3 |
| C.常温时水溶性Na2CO3<NaHCO3 |
| D.相对分子质量Na2CO3<NaHCO3 |
某研究性学习小组用FeCl3溶液做“腐蚀液”,制作印刷电路板,其反应原理是:2FeCl3+Cu=2FeCl2+CuCl2。
【实验探究】
(1)通过《化学1》的学习,知道了有离子参加的化学反应为离子反应。离子反应可用离子方程式表示。请写出2FeCl3+Cu=2FeCl2+CuCl2反应的离子方程式为: 。
(2)若要溶解电路板上3.2g的铜,则至少需要FeCl3物质的量为 mol。
(3)使用后失效的“腐蚀液”为废液,验证废液中是否存在Fe3+的试剂是 ,加入该试剂后,若出现 现象,说明废液中还存在Fe3+。
(4)废液中的CuCl2可通过加入足量的 ,反应后转化成铜且能使所得溶液中含有单一溶质。
(5)回收Cu后的废液,通入足量的Cl2,可以重新获得FeCl3溶液,其反应的化学方程式为 。
【实验结论】
利用FeCl3溶液做印刷电路板的“腐蚀液”,不仅废液中的铜可以得到回收,经过处理后的废液还可以重新使用。
【知识拓展】
(6)铁元素是维持生命活动不可缺少的微量元素,虽然人体中通常只含有3~5g铁元素,但铁元素在人体中却发挥着重要作用,人体缺铁会引起 疾病。
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。请填空:
(1)D装置中主要反应的离子方程式为 ,F仪器的作用是 。
(2)为验证通入D装置中的气体是Cl2还是SO2过量,兴趣小组的同学准备了以下试剂:
a 氯化铁稀溶液 b 氯化亚铁溶液 c 硫氰化钾溶液
d 苯酚溶液 e 品红溶液 f 酸性高锰酸钾溶液
①若Cl2过量:取适量D中溶液滴加至盛有 (选填一个符号)试剂的试管内,再加入 (选填一个符号)试剂,发生的现象是: ;
②若选用上述试剂中的一种再结合必要的操作就可以验证通入D装置中的气体是Cl2过量还是SO2过量,该试剂是 (选填一个符号)。必要的操作和结论是 。