下列说法正确的是
| A.明矾水解形成的Al(0H)3胶体能杀菌消毒,可用于水的净化 |
| B.镀锡的铁制品比镀锌的铁制品耐用 |
| C.乙醇和乙酸都能溶于水,都是电解质 |
| D.分别与等物质的量的HC1和CH3COOH恰好中和时,消耗NaOH的物质的量相同 |
下列有关钢铁腐蚀与防护的说法正确的是
| A.钢管与电源正极连接,钢管可被保护 |
| B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 |
| C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀 |
| D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-===Fe3+ |
化学与人类生活密切相关。下列说法正确的是
| A.“钡餐”中使用的硫酸钡是弱电解质 |
| B.镀锌铁镀层破损后,铁更容易被腐蚀 |
| C.提倡人们购物时不用塑料袋,是为了防止白色污染 |
| D.推广使用太阳能、风能、海洋能、氢能,不利于缓解温室效应 |
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
| A.4Fe(OH)2+2H2O+O2=4Fe(OH)3 | B.2Fe+2H2O+O2=2Fe(OH)2 |
| C.2H2O+O2+4e-=4OH- | D.Fe-3e-=Fe3+ |
在钢铁的吸氧腐蚀中,发生还原反应的电极上的进行的电极反应是
| A.4 OH- -4e-=2H2O+O2↑ | B.2H++2e-=H2↑ |
| C.2H2O+O2+4e-="4" OH- | D.Fe-2e-= Fe2+ |
下列说法正确的是
| A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS) |
| B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大 |
| C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体 |
| D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀 |
有关金属腐蚀的叙述正确的是
| A.生铁抗腐蚀能力比纯铁强 |
| B.钢瓶在储存液氯前彻底干燥可减缓腐蚀 |
| C.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| D.常温下浓硝酸比浓盐酸更易使铁腐蚀 |
下列关于铁电极的说法中,正确的是
| A.钢铁的吸氧腐蚀中铁是正极 | B.在铁片上镀铜时铁片作阳极 |
| C.电解饱和食盐水时可用铁作阴极 | D.镀锌铁板发生电化学腐蚀时铁是负极 |
如图是模拟电化学反应装置图。下列说法正确的是( )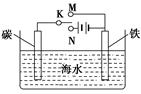
| A.开关K置于N处,则铁电极的电极反应式为:Fe-2e-=Fe2+ |
| B.开关K置于N处,可以减缓铁的腐蚀 |
| C.开关K置于M处,则铁电极的电极反应式为:2Cl--2e-=Cl2↑ |
| D.开关K置于M处,电子从碳棒经开关K流向铁棒 |
下列描述不符合生产、生活实际的是
| A.家用炒锅残留盐溶液时易发生吸氧腐蚀 |
| B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解水制氢气时,用铜作阳极 |
| D.在镀件上电镀锌,用锌作阳极 |
据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是 ( )。
| A.Fe-2e-=Fe2+ |
| B.2H2O+O2+4e-=4OH- |
| C.2H++2e-=H2↑ |
| D.4OH--4e-=2H2O+O2↑ |
写出钢铁生锈的电极反应式(水膜呈中性):
负极___________________________
正极___________________________
下列叙述不正确的是
| A.金属的电化学腐蚀比化学腐蚀更普遍 |
| B.用铝质铆钉铆接铁板,铁板易被腐蚀 |
| C.钢铁在干燥空气中不易被腐蚀 |
| D.用牺牲锌块的方法来保护船身 |
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不会发生的化学反应是( )
| A.Fe-3e-===Fe3+ | B.2Fe+2H2O+O2===2Fe(OH)2 |
| C.2H2O+O2+4e-===4OH- | D.4Fe(OH)2+2H2O+O2===4Fe(OH)3 |
下列叙述的原因不是由于原电池造成的是
| A.运输液氯的铁管被腐蚀 | B.金属在潮湿空气中更容易腐蚀 |
| C.铁与酸反应滴加硫酸铜后反应加快 | D.含杂质的锌比纯锌与酸反应快 |