对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
① 碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是____(用离子方程式表示)。为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的____.。
a.NH3 b.CO2 c.NaOH d.HNO3
② 以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应为____。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生此现象的原因(用离子方程式表示)_____。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极材料的原因是______。
(3)利用下图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于______处。
若X为锌,开关K置于M处,该电化学防护法称为_______。
(1)能源是当今社会发展的三大支柱之一。天然气是一种高效、低耗、污染小的清洁能源,主要成分为甲烷,甲烷燃烧的化学方程式为: ;
; 标准状况下,11.2L甲烷燃烧时,转移电子的物质的量为 mol。
标准状况下,11.2L甲烷燃烧时,转移电子的物质的量为 mol。

 s
s
 在如图构想的物质循环中太阳能最终转化为 能。
在如图构想的物质循环中太阳能最终转化为 能。
 (2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀
(2)钢铁的腐蚀现象非常普遍,电化学腐蚀是造成钢铁腐蚀 的主要原因,某同学按右图进行钢铁腐蚀的模拟,则
的主要原因,某同学按右图进行钢铁腐蚀的模拟,则
负极的电
 极反应式为 ,
极反应式为 , 正极的电极反应式为 。
正极的电极反应式为 。 【提示:电化学的总反应式为2Fe+2H2O+O2=2Fe(OH)2】
【提示:电化学的总反应式为2Fe+2H2O+O2=2Fe(OH)2】 (3)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:
(3)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

 操作①的名称是 ;反应②的离子方程式是 ,下述物质中不可做试剂③的是 。
操作①的名称是 ;反应②的离子方程式是 ,下述物质中不可做试剂③的是 。
| A.乙醇 | B.苯 | C.乙酸 | D.四氯化碳 |
(1)埋在地下的输油铁管道,在下列情况下,①在含铁元素较多的酸性土壤中、②在潮湿疏松透气的土壤中、③在干燥致密不透气的土壤中、④在含碳颗粒较多,潮湿透气的中性土壤中。被腐蚀速率最慢的是
(2)以石墨棒为两极,氯化铜溶液为电解液组成的电解池的
阴极电极反应式是
在化学反应中发生的能量转变形式是
(12分)
本题共有3个小题,回答有关问题:
(1)检验牙膏中含有甘油的试剂是 ,实验现象 ;有关反应的化学方程式 。
(2)在两烧杯中盛有甲、乙两种不同的稀溶液,用铁丝做电化腐蚀实验。实验进行一段时间后,A试管中液面高于烧杯中液面,B试管中液面低于烧杯中液面,试比较pH值大小:
甲 乙(填“<”、“>”或“=”),并写出A中铁丝发生腐蚀时的电极反应式:负极 ,正极 。
(3)已知某溶液中只存在 、H+、
、H+、 、Na+四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
、Na+四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
I:
II:
III:
IV:
①若溶液中只溶解了一种溶质,则该溶质是 ,上述四种离子浓度的大小顺序
为 (填编号)。
②若上述关系中III是正确的,则溶液中溶质为
③若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好呈中性,则混合前两溶液的物质的量浓度大小关系为
 (填“<”、“>”或“=”),混合前
(填“<”、“>”或“=”),混合前 溶液中的
溶液中的
 溶液中的
溶液中的 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
对金属制品进行搞腐蚀处理,可延长其使用寿命。
(1)以下为铝村表面处理的一种方法:

①碱洗的目的是除去铝村表面的自然氧化膜,碱洗衣时候常有气泡冒出,原因是:(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的。
a. b.
c.
d.
②以铝村为阳极,在溶液中电解,铝村表面形成氧化膜,阳极电极反应式为:。取少量废电解液,加入
溶液后产生气泡和白色沉淀,产生沉淀的原因是。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是。
(3)利用下图装置,可以模拟铁的电化学防护。

若为碳棒,为减缓铁的腐蚀,开关K应该置于处。
若为锌,开关
置于
处,该电化学防护法称为。
(9分) 右图所示水槽中试管内有一枚铁钉,放置数天后观察: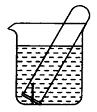
(1)铁钉在逐渐生锈,则铁钉的 腐蚀属于 腐蚀。(填化学腐蚀或电化学腐蚀)
腐蚀属于 腐蚀。(填化学腐蚀或电化学腐蚀)
(2)若试管内液面上升,则原溶液呈 性,发生 腐蚀,正极反应式为 。
(3)若试管内液面下降,则原溶液呈 性,发生 腐蚀,正极反应式为 。
古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重(电化腐蚀)。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,可将土壤中的SO42-还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。
①写出该电化腐蚀的正极反应的电极反应式:
②文物出土前,铁器表面的腐蚀产物可能有(写化学式)
生活中常常有这样的现象:一件普通的铁器,如不精心保管,便会生锈;若不引起注意,锈斑蔓延开来,就会吞噬整个铁器使之变成废物。人们称这种现象为“锈吃铁”。请用相关学科知识解释“锈吃铁”这一自然现象。
如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
| 序号 |
内容 |
实验现象 |
| 1 |
常温下将铁丝放在干燥空气中一个月 |
干燥的铁丝表面依然光亮 |
| 2 |
常温下将铁丝放在潮湿空气中一小时 |
铁丝表面依然光亮 |
| 3 |
常温下将铁丝放在潮湿的空气中一个月 |
铁丝表面已变得灰暗 |
| 4 |
将潮湿的铁丝放在常温的氧气流中一小时 |
铁丝表面略显灰暗 |
| 5 |
将潮湿的铁丝放在高于常温的氧气流中一小时 |
铁丝表面已变得灰暗 |
| 6 |
将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 |
铁丝表面灰暗程度比实验5严重 |
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号);在电化学腐蚀中,负极反应是;正极反应是;
(2)由该实验可知,可以影响铁锈蚀速率的因素是;
(3)为防止铁的锈蚀,工业上普遍采用的方法是(答两种方法)
如图所示,水槽中试管内有一枚铁钉,放置数天观察:
⑴铁钉在逐渐生锈,则铁钉的腐蚀属于 腐蚀。
⑵若试管内液面上升,则原溶液是 性,发生 腐蚀,电极反应:负极: ,正极: 。
⑶若试管内液面下降,则原溶液是 性,发生 腐蚀,电极反应:负极: ,正极: 。
⑷若溶液甲为水,溶液乙为海水,则铁钉在 (填“甲”或“乙”)溶液中腐蚀的速度快。