关于金属腐蚀和防护的说法不正确的是
| A.金属腐蚀过程中发生了化学反应 |
| B.在铁表面镀锌可对铁起保护作用 |
| C.在铁船壳上镶嵌铜块能减缓船体的腐蚀 |
| D.铝制品在空气中不易被腐蚀,是因其表面形成了致密的氧化铝保护层 |
下列金属防腐蚀的方法中,使用外加电流的阴极保护法的是
| A.水中的钢闸门连接电源负极 | B.在锅炉内壁装上镁合金 |
| C.汽车底盘喷涂高分子膜 | D.在铁板表面镀锌 |
由下列实验及现象不能推出相应结论的是( )
| |
实验 |
现象 |
结论 |
| A. |
向 的 溶液中加足量铁粉,振荡,加1滴KSCN溶液 |
黄色逐渐消失,加KSCN溶液颜色不变 |
还原性: |
| B. |
将金属钠在燃烧匙中点燃,迅速伸入集满 的集气瓶 |
集气瓶中产生大量白烟,瓶内有黑色颗粒产生 |
具有氧化性 |
| C. |
加热盛有少量 固体的试管,并在试管口放置湿润的红色石蕊试纸 |
石蕊试纸变蓝 |
显碱性 |
| D. |
向2支盛有 相同浓度银氨溶液的试管中分别加入2滴相同浓度的 和 溶液 |
一只试管中产生黄色沉淀,另一支中无明显现象 |
|
下列说法正确的是
| A.马口铁(锡铁)镀层破损后被腐蚀时,首先是镀层被氧化 |
| B.原电池反应是导致金属腐蚀的主要原因,故不能用于减缓金属的腐蚀 |
| C.钢铁电化学腐蚀的两种主要类型其主要区别在于水膜的pH不同引起负极反应的不同 |
| D.无论哪种类型的金属腐蚀,其实质都是金属被氧化 |
下列说法正确的是
| A.在海轮船壳上镶入锌块保护海轮,利用的是牺牲阳极的阴极保护法 |
| B.加入合适的催化剂,能降低反应活化能,从而改变反应的焓变 |
| C.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 |
| D.稀醋酸中加入少量CH3COONa固体,醋酸的电离程度减小,c(CH3COO-)增大 |
下列与金属腐蚀有关的说法正确的是
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池放电腐蚀主要是由MnO2的氧化作用引起的 |
下列实验与对应结论正确的是
| |
A |
B |
C |
D |
| 装置 |
 |
 |
 |
 |
| 结论 |
Ag2O/Ag极发生 还原反应 |
能证明非金属性Cl > C > Si |
验证铁发生析氢腐蚀 |
白色沉淀是BaSO3 |
下列说法正确的是
| A.氯化钠固体不导电,所以氯化钠是非电解质 |
| B.向纯水中加入碳酸钠能使水的电离平衡正向移动,水的离子积增大 |
| C.如图研究的是铁的吸氧腐蚀,实验中红色首先在食盐水滴的中心出现 |
| D.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) 的△H<0 △S<0 |
下列有关金属防护的说法不正确的是
| A.通过镶嵌锌块保护船体的方法叫牺牲阳极的阴极保护法 |
| B.埋铁制管线时应选择致密、干燥的土壤层 |
| C.青铜器表面覆盖防渗高分子膜,可防止铜绿形成 |
| D.纯银器表面在空气中因电化学腐蚀渐渐变暗 |
化学与生产、生活密切相关,下列有关说法不正确的是
| A.使用含有氯化钠的融雪剂会加快桥梁的腐蚀 |
| B.可溶性铜盐有毒,故人体内不存在铜元素 |
| C.在海轮外壳装上锌块,可减缓船体的腐蚀速率 |
| D.中秋佳节月饼中用小袋包装的铁粉来防止月饼氧化变质 |
下列用来表示物质变化的化学用语中,正确的是( )
| A.钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣=Fe2+ |
B.HS﹣的水解方程式:HS﹣+H2O S2﹣+H3O+ S2﹣+H3O+ |
C.CO32﹣的水解方程式:CO32﹣+H2O HCO3﹣+OH﹣ HCO3﹣+OH﹣ |
| D.AlCl3溶液与Na2CO3溶液混合:2Al3++3CO32﹣=Al2(CO3)3↓ |
原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错误的是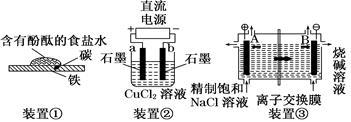
| A.装置①研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e===Fe2+ |
| B.装置②研究的是电解CuCl2溶液,它将电能转化为化学能 |
| C.装置③研究的是电解饱和食盐水,电解过程中B极上发生氧化反应 |
| D.三个装置中涉及的主要反应都是氧化还原反应 |
右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化氢溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
| A.生铁块中的碳是原电池的正极 |
| B.红墨水柱两边的液面变为左低右高 |
| C.两试管中负极电极反应相同 |
| D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
下列关于电化学知识说法正确的是
| A.电解AlCl3、FeCl3、CuCl2的混合溶液,在阴极上依次析出Al、Fe、Cu |
| B.电解CuSO4溶液一段时间后,加入适量Cu(OH)2可以使溶液恢复至原状态 |
| C.铅蓄电池在充电时,连接电源正极的电极发生的电极反应为:PbSO4+2e-=Pb+SO42- |
| D.将钢闸门与直流电源的负极相连,可防止钢闸门腐蚀 |