(2分)现有以下物质①NaCl溶液②干冰(固态的二氧化碳)③冰醋酸(纯净的醋酸)④铜⑤BaSO4固体⑥蔗糖⑦酒精⑧熔融的KNO3,其中属于电解质的是: (填序号)。
某盐溶液中可能含有NH4+、Ba2+、Na+、Fe2+、Cl—、CO32—、NO3—七种离子中的数种。某同学取4份此溶液样品,分别进行了如下实验:(硝酸具有强氧化性,可以氧化Fe2+、I-、S2-、SO32—等等)
①用pH试纸测得溶液呈强酸性;
②加入 过量NaOH溶液,产生有刺激性气味的气体且有沉淀生成;
过量NaOH溶液,产生有刺激性气味的气体且有沉淀生成;
③加入硝酸酸化的AgNO3溶液产生白色沉淀;
④加足量BaCl2溶液,没有沉淀产生,在溶液中加入氯水,再滴加KSCN溶液,显红色
该同学最终确定在上述七种离子中肯定含有NH4+、Fe2+、Cl—三种离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A.①②④ B.①② C.①②③④ D.②③④
(1)食品和药品关系人的生存和健康。
①市场上销售的食盐品种很多。下列食盐中,所添加的元素不属于人体必需微量元素的是 (填字母)。
A.加锌盐 B.加碘盐 C.加钙盐
②纤维素被称为“第七营养素”。食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质。从化学成分看,纤维素是一种 (填字母)。
A.多糖 B.蛋白质 C.脂肪
③某同学感冒发烧,他可服用下列哪种药品进行治疗 (填字母)。
A.麻黄碱 B.阿司匹林 C.抗酸药
(2)材料是人类赖以生存和发展的重要物质基础。
①生产硅酸盐水泥和普通玻璃都需用到的共同的主要原料是 。
②生活中有大量的铝制品。 家用铝锅不能经常用热碱水洗涤去污,原因是(用离子方程式表示) 。
家用铝锅不能经常用热碱水洗涤去污,原因是(用离子方程式表示) 。
③有机玻璃受热时会软化, 易于加工成型。有机玻璃是一种 材料(选填“硅酸盐”或“纤维”或“塑料”)。导电塑料的结构可表示为
易于加工成型。有机玻璃是一种 材料(选填“硅酸盐”或“纤维”或“塑料”)。导电塑料的结构可表示为 ,则其单体的结构简式为 。
,则其单体的结构简式为 。
(3)保护环境、保护地球是人类共同的呼声。
①向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2。发生反应的化学方程式为 。
②天然水中含有的细小悬浮颗粒可以用 做混凝剂(写名称)进行净化处理。工业废水中含有的Cr3+离子,可用熟石灰作沉淀剂,在pH为8~9时生成沉淀而除去,该反应的离子方程式是 。
③城市餐饮业会产生大量污染环境的“地沟油”。“地沟油”的主要成分是油脂。综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和 。生活中会产生大量废弃塑料,将废弃塑料进行 处理,可以获得乙烯、丙烯等化工原料。
(14分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 |
OH-、Cl-、CO32-、NO3-、SO42- |
请根据以下实验事实逐步推出它们的名称并回答问题:
(1)
| 物质鉴定实验 |
推导结论 |
| ①用pH试纸测出A、B溶液呈碱性,C、D、E溶液呈酸性 |
A、B中含有的阴离子为________,C、D、E中含有的阳离子为________ |
| ②A溶液与E溶液反应既有气体又有沉淀产生;A与C反应只有气体产生 |
A为________,C含有的阳离子为________ |
| ③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀 |
D为________ |
(2)写出E溶液与过量的B溶液反应的离子方程式:_____________________________。
(3)在100 mL 0.1 mol/L的E溶液中,逐滴加入35 mL 2 mol/L NaOH溶液,最终得到沉淀的物质的量为__________________。
“走迷宫”是深受大众欢迎的益智游戏,某同学以“盐酸”的身份走人化学迷宫,迷宫里有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。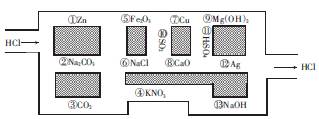
(1)“盐酸”经过的物质序号依次为 。
(2)在(1)中所写物质中,属于电解质的是 (填序号,下同),属于非电解质的是 。
(3)请根据不同的分类标准将图中能与盐酸反应的物质分为两类,结果填在下表中:
(3分)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体⑥蔗糖(C12H22O11) ⑦酒精(C2H 5OH) ⑧熔化K2SO4 ⑨纯水。请回答下列问题(用序号):
5OH) ⑧熔化K2SO4 ⑨纯水。请回答下列问题(用序号):
(1)以上物质中能导电的是__________
(2)以上物质属于电解质的是_____________
(3)以上物质中属于非电解质的是______________
某溶液中可能大量存在下列阴离子中的一种或几种:SO42-、CO32-、CL-。
⑴当溶液中有大量H+存在时,则不可能大量存在 。 ⑵当溶液中有大量Ba2+存在时,则不可能大量存在 和
⑵当溶液中有大量Ba2+存在时,则不可能大量存在 和
⑶当溶液中同时有大量Ba2+和 存在时,上述阴离子都不可能大量存在。
有以下几种物质①乙醇②MgCl2晶体③蔗糖 ④铜⑤食盐水⑥ BaSO4 请填空回答(填序号)。
⑴以上物质中能导电的的是
⑵以上物质中属于电解质的是
⑶以上物质中属于非电解质的是
有下列物质:①铜;②硫酸钡固体;③氢氧化钠固体;④氨水;⑤熔融硝酸钾;⑥乙醇;⑦液态HCl;⑧石墨;⑨二氧化硫;⑩冰醋酸; ⑾硫。
(1)其中能导 电的有________,其水溶液能导电的是________。
电的有________,其水溶液能导电的是________。
(2)属于非电解质的有________,属于强电解质的是________。
有一瓶澄清溶液,可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、NO3-、CO32-、SO42-中的一种或几种。取该溶液进行以下实验:
①用pH试纸检验,表明溶液呈强酸性;
②取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色;
③另取部分溶液,向其中逐滴加入NaOH溶液,使溶液从酸性变为碱牲,在滴加过程中先生成白色沉淀后完全溶解;取部分碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。
④另取部分③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
根据以上实验事实回答下列问题:
(1)该溶液中肯定存在的离子是 ,肯定不存在的离子是 ;
(2)步骤③加入NaOH溶液过程中先生成白色沉淀后完全溶解的离子方程式为 ;
(1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组。
A组显酸性,除H+ 外还有 、 、 离子
B组显碱性,除OH-外还有 、 、 离子
(2)实验室制备氢氧化铁胶体的方法是 ;
反应的化学方程为 。
下列物质: ①Na ②Br2 ③NaCl溶液 ④CO2 ⑤盐酸 ⑥浓硫酸 ⑦Ba(OH)2晶体 ⑧熔融KCl ⑨ 蔗糖
属于电解质的是 (填代号,以下同),
属于非电解质的是 ,能导电的是 。
有一透明溶液甲,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Ba2+、SO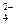 、Cl-、I-、HCO
、Cl-、I-、HCO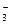 ,现取该溶液实验如下:
,现取该溶液实验如下:
| 实验步骤 |
实验现象 |
| ①取少量甲溶液,滴加几滴甲基橙 |
溶液变红色 |
| ②取少量甲溶液,滴加Ba(NO3)2溶液 |
溶液无明显变化 |
| ③取②中实验后的溶液,滴加AgNO3溶液 |
有白色沉淀生成,且不溶于HNO3 |
| ④取少量甲溶液,滴加NaOH溶液 |
有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
(1)由实验步骤①判断出溶液中肯定不存在的离子是 ,能说明这一实验事实的离子方程式是
(2)实验步骤③的实验结果说明溶液中不存在 离子
(3)欲确定的离子中肯定存在的是 。
(4)为进一步确定其他离子,应该补充的实验是
| A.蒸发 | B.过滤 | C.焰色反应 | D.渗析 |