在H2SO4和Al2 (SO4)3的混合溶液中,铝离子浓度是0.4 mol / L,硫酸根离子浓度是0.7 mol / L,则氢离子浓度约是 ( )
| A.0.1 mol / L | B.0.2 mol / L | C.0.3 mol / L | D.0.4 mol / L |
某溶液中含Fe3+、Cl—、Na+、SO42—,其离子个数比为Fe3+∶Cl—∶Na+∶SO42—=1∶2∶x∶2,则x的值是
| A.1 | B.2 | C.3 | D.4 |
溶液中存在有五种离子,其中各离子个数比Cl-∶SO42-∶Fe3+∶K+∶M=2∶3∶1∶3∶1,则M为( )
| A.CO32- | B.Mg2+ | C.Na+ | D.Ba2+ |
下列物质的电离方程式,错误的是
| A.HCl = H++Cl- | B.H2SO4= 2H++SO42- |
| C.FeCl3= Fe3++Cl- | D.Ca(OH)2= Ca2++2OH- |
某地有甲、乙两个工厂排放污水,污水中各含有下列8种离子中的4种(两厂不含相同离子):Ag+、Ba2+、Fe3+、Na+、Cl-、SO42-、NO3-、OH-。两厂单独排放时,都会造成严重的水污染。如果将两厂的污水按一定比例混合,过滤沉淀后污水就变为无色澄清且只含NaNO3而排放,污染程度大大降低。关于污染源的分析,你认为正确的是
| A.Cl- 和NO3-一定来自不同的工厂 | B.SO42- 和NO3-可能来自同一工厂 |
| C.Ag+ 和Na+ 可能来自同一工厂 | D.Na+ 和NO3-一定来自同一工厂 |
下列物质混合发生化学反应,且反应属于离子反应的是
| A.H2和O2反应生成水 |
| B.锌片投入稀硫酸中 |
| C.KClO3(固体)和MnO2(固体)混合加热制O2 |
| D.NaOH溶液和K2SO4溶液混合 |
将电解质分为强、弱电解质的依据是
| A.在一定条件下的电离程度 | B.属于离子化合物还是共价化合物 |
| C.熔融状态下是否完全电离 | D.溶于水后的导电能力是强还是弱 |
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如右表所示:取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
| 阳离子 |
NH4+、Na+、Mg2+ |
| 阴离子 |
OH-、NO3-、SO42- |
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
| A.①② | B.③④ | C.①⑤ | D.③⑤ |
某无色溶液中只可能含有Na+、Ba2+、Mg2+、Cl—、Br-、SO2-3、SO2-4,对该溶液进行下列实验, 实验操作和现象如下表: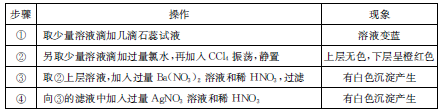
下列结论正确的是
| A.可能含有Cl-、Mg2+、SO2-4 | B.肯定没有Ba2+、Cl-、Br- |
| C.不能确定的离子有Mg2+、SO2-3-、SO2-4 | D.肯定含有Na+、Br-、SO2-3 |
某盐的混合物中含有0.2 mol/L Na+、0.4 mol/L Mg2+、0.4 mol/L Clˉ,则SO42ˉ为
| A.0.1 mol/L | B.0.2 mol/L | C.0.3 mol/L | D.0.4 mol/L |
下列电离方程式书写错误的是
| A.H2SO4 ="==" 2H+ + SO42- | B.AL2(SO4)3 ="==" 2AL3+ + 3 SO42- |
| C.Ba(NO3)2 ="==" Ba2++ 2(NO3)2- | D.Ba(OH)2 ="==" Ba2+ + 2 OH- |
某溶液中含有NH、SO、SiO、Br-、CO、Na+,向该溶液中通入过量的Cl2,下列判断正确的是 ( )
①反应前后,溶液中离子浓度基本保持不变的有NH、Na+
②有胶状沉淀生成
③有气体产生
④溶液颜色发生变化
⑤共发生了2个氧化还原反应
| A.①②③④ | B.②③④ | C.①③⑤ | D.②④⑤ |
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是( )
| A.Na+ | B.SO42- | C.Ba2+ | D.NH4+ |
下列电离方程式正确的是( )
| A.H2SO4= H2+ +SO42- | B. K2CO3 = 2K++CO32- |
| C.Ca(OH)2=Ca2++OH2- | D. Mg(NO3)2 = Mg2++ (NO3-)2 |
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导 率变化可以确定滴定反应的终应。右图是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图。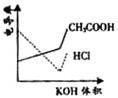
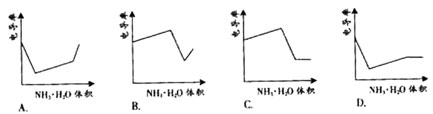
下列示意图中,能正确表示用NH3·H2O溶液滴定 HCl和CH3COOH混合溶液的滴定曲线的是
HCl和CH3COOH混合溶液的滴定曲线的是