按下图装置进行实验,并回答下列问题
(1)锌极为__________极,电极反应式为_________________________
石墨棒C1为______极,电极反应式为________________________
石墨棒C2附近发生的实验现象为_______________________________
(2)当C2极析出224mL气体(标准状态)时,锌的质量减少_________g.
用化学术语回答下列问题:
(1)书写电离方程式:氢氟酸 ;
(2)书写水解离子方程式:硫酸铝 ;
(3)电解硝酸银溶液电极反应式(惰性电极)①阳极: ;②阴极: .
工业制硫酸时,利用催化氧化反应将 是一个关键的步骤。
是一个关键的步骤。
(1)某温度下, 。开始时在100L的密闭容器中加入4.0molSO2(g)和10.0molO2,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=____________。
。开始时在100L的密闭容器中加入4.0molSO2(g)和10.0molO2,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=____________。
(2)一定条件下,向一带活塞的密闭容器中充入2mol mol
mol ,发生反应:
,发生反应: ,达平衡后改变下述条件,
,达平衡后改变下述条件, 气体平衡浓度都比原来增大的是____________(填字母)。
气体平衡浓度都比原来增大的是____________(填字母)。
A.保持温度和容器体积不变,充入2mol |
| B.保持温度和容器体积不变,充入2molN2 |
C.保持温度和容器内压强不变,充入1mol |
| D.移动活塞压缩气体 |
E.升高温度
(3)下列关于 反应的图像中,不正确的是_________。
反应的图像中,不正确的是_________。
(4)同学们学习了电化学知识后大家提出,可以用电解的方法来生产硫酸,可避免产生酸雨,污染环境。于是大家设计了一个以铂为电极,两极分别通入SO2和空气,酸性电解液来实现电解生产硫酸。
①阳极的电极反应为______________________________。
②若电解液为2L0.025mol 的硫酸溶液,当电解过程共转移了0.1mol电子时,理论上消耗SO2的体积为(标准状况)为_________,此溶液的pH="__________" (忽略溶液体积变化)。
的硫酸溶液,当电解过程共转移了0.1mol电子时,理论上消耗SO2的体积为(标准状况)为_________,此溶液的pH="__________" (忽略溶液体积变化)。
③设计此实验的想法得到了老师的充分肯定,但与工业上生产硫酸相比还是有很多不足,请对此实验进行合理的评价____________________________(写出一点即可)。
A、B、C、D、E是原子序数依次增大的5种短周期元素。A、E同主族,B、C是同周期相邻的两种元素。A、C的质子数之和等于D的质子数,A+离子与D2―离子的核外电子数之和等于E+ 离子的核外电子数。请回答下列问题:
(1)A、D元素按1 :1组成的化合物的结构式为_______ 。
(2)常见化合物W由A、D、E三种元素组成,则W中含有的化学键有_______ 。
若以W溶液为电解质溶液,铁棒为电极构成电解池,该电解反应的总反应方程式为: 。
(3)在恒容密闭容器中注入A2、C2两种气体,发生如下反应:3A2(g)+C2(g) 2CA3(g),在某温度下达到平衡时,各物质的浓度分别为:c(A2)=9.00mol/L;(C2)=3.00mol/L,c(CA3)=4.00mol/L。则C2的起始浓度为 mol/L;A2的转化率为_______ %0 。
2CA3(g),在某温度下达到平衡时,各物质的浓度分别为:c(A2)=9.00mol/L;(C2)=3.00mol/L,c(CA3)=4.00mol/L。则C2的起始浓度为 mol/L;A2的转化率为_______ %0 。
(4)A、C、D三种元素按原子个数比4︰2︰3形成的化合物溶于水,所得溶液呈酸性,用离子方程式解释其原因 。
(5)用E2D2在酸性条件下处理含CN―的工业废水,将得到N2及CO2等无污染的物质,请写出该反应的离子方程式_____________________ 。
工业上处理含Cr2O72-的酸性工业废水用以下方法:①往工业废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。试回答:
(1)电解时的电极反应:阳极 阴极: ;
(2)写出Cr2O72-转变成Cr3+的离子反应方程式 ;
(3)电解过程中Cr(OH)3、Fe(OH)3沉淀是怎样产生的? 。
从H+、Na+、Cu2+、Ba2+、Cl—、SO42—离子中,选出恰当的离子组成一种电解质,将电解质溶液按下列要求进行电解(均是惰性电极):
(1)电解时电解质含量减小,水量不变,则所采用的电解质是 ;
(2)电解时电解质的质量保持不变,水量减小,则所采用的电解质是 ;
(3)电解时电解质和水的质量都发生变化,则所采用的电解质是 ;
海水是人类资源的宝库,“海水晒盐”是获取食盐的重要来源。食盐既是一种生活必需品,也是一种重要的工业原料。以食盐为原料可以得到多种产品。工业上主要通过电解饱和氯化钠溶液的方法获得氢氧化钠。
(1)阳极反应式为 ,检验该电极反应产物的方法是: 。
(2)当阴极和阳极上共收集到气体22.4 L时(标准状况下,假设产生的气体完全被收集),则电路中通过电子的个数为 。
(3)电解氯化钠稀溶液可以制备“84”消毒液,若通电时产生的氯气被溶液完全吸收,且最终所得消毒液仅含一种溶质,请写出相应的化学方程式: (用一个方程式表示)。
Li-SOC12电池可用于心脏起搏器,该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2.电池的总反应可表示为:4Li+2SOC12  4LiCl +S+SO2。
4LiCl +S+SO2。
请回答下列问题:
(1)电池的负极材料为_________,发生的电极反应为____________________;
(2) SOCl2易挥发,实验室中常用NaOH溶液吸收SOC12,如果把少量水滴到SOCl2中,反应的化学方程式为__________________________________________;
(3)用此蓄电池电解含有0.1 mol/LCuSO4和0.1 mol/LNaCl的混合溶液100 mL,假如电路中转移了0.02 mole-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是______L,将电解后的溶液加水稀释至1L,此时溶液的pH=______________。
下图是一个化学过程的示意图。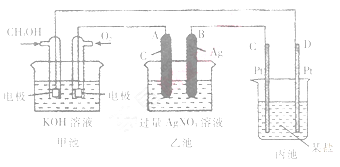
(1)请回答图中甲池是______装置,其中OH-移向________极(填“CH3OH”或“O2”)
(2)写出通入CH3OH的电极的电极反应式_________。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为_________极(填“A”或“B”),并写出此电极反应的电极反应式____________。
(4)乙池中反应的离子方程式为____________。
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是________(若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是_______(填序号).
| A.MgSO4 | B.CuSO4 | C.NaCl | D.AgNO3 |
如右图,A为直流电源,c、d均为石墨电极, B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为________极;
(2)滤纸B上发生的总化学方程式为___________________;
(3)欲在电镀槽中实现铁上镀锌,闭合K键,使c、d两点短路,则电极e上发生的反应为 ,电极f上发生的反应为___________________,槽中放的电镀液可以是 。
【化学——选修化学与技术】
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝一冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝: 下加入冰晶石的作用:____ 。
下加入冰晶石的作用:____ 。
(2)上述工艺所得铝材中往往含有少量Fe和Si筹杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是____
A.铝材 B.石墨 C.铅板 D.纯铝
(3)阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式为 。
(4)在铝阳极氧化过程中,需要不断地调整电压,理由是
(5)下列说法正确的是____。
A.阳极氧化是应用原电池原理进行金属材料表面处理的技术
B.铝的阳极氧化可增强铝表面的绝缘性能
C.铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D.铝的阳极氧化膜富有多孔性,具有很强的吸附陛能,能吸附染料而呈各种颜色
(9分)如下图装置实验,A、B两烧杯分别盛放200 g10%NaOH和足量CuSO4溶液。通电一段时间后,c极上有Cu析出,又测得A杯中溶液的质量减少4.5 g(不考虑水的蒸发)。
请回答下列问题:
(1)电源P极为 极;请分别写出b极和c极上发生的电极反应 式: ;
(2)c极上析出固体铜的质量为 g
(3)若装置中用铅蓄电池作电源,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
假设在a极制得气体0.050 mol,这时电池内消耗的H2SO4的物质的量至少是 mol
化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12。
① N2的电子式为 。
②上述反应离子方程式为___________________________________________________,
其平均反应速率v(NO3-)为 mol·L-1·min-1。
③还原过程中可生成中间产物NO2-,写出3种促进NO2-水解的方法 。
(2)电化学降解NO3-的原理如下图所示。
电源正极为______________(填“A”或“B”),
阴极反应式为_____________________________________。 
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既廉价又环保。利用H2S废气制取氢气来的方法有多种
(1)高温热分解法
已知:H2S(g)  H2(g)+1/2S2(g)
H2(g)+1/2S2(g)
在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为0.2 mol·L-1测定H2S的转化率,结果见右图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985℃时H2S按上述反应分解的平衡常数K=_____________;说明温度的升高,曲线b向曲线a逼近的原因:________________________________________________________
(2)电化学法
该法制氢过程的示意图如右。反应池中反应物的流向采用气、液逆流方式,其目的是___________;反应池中发生反应的化学方程式为_____________________。反应后的溶液进入电解池,电解总反应的离子方程式为_______________________。
(12分)【化学——化学与技术】
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)多级闪蒸法是目前“海水淡化”的主要技术。该法是在一定条件下将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水。由此可判断多级闪蒸法是 (填“物理变化” 或“化学变化”)。
(2)利用海水晒盐的原理是 ;分离食盐晶体后的母液中含有KCl、MgCl2,经过分离、提纯后,可用于 。
(3)“氯碱工业”利用电解饱和食盐水制得重要化工产品。在氯碱工业中,隔膜法电解(如图甲所示)工艺逐渐被离子交换膜电解(如图乙所示)技术取代。
①写出两电极的反应式:阳极 ,阴极 。
②石棉隔膜的作用是 。离子交换膜电解槽中⑥、⑦分别是 、 。